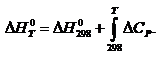Первое начало термодинамики. Закон Гесса как следствие первого начала термодинамики. Термохимические расчеты.
Существует множество формулировок первого закона:
В изолированной системе общий запас энергии сохраняется постоянным.Поскольку работа является одной из форм перехода энергии, то, следовательно, невозможно создание вечного двигателя первого рода (машины, совершающей работу без затраты энергии).Математическая формулировка: 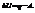 При протекании изобарического процесса:
При протекании изобарического процесса:
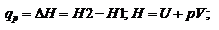
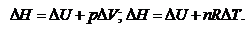
При протекании изохорического процесса:
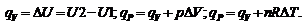
При протекании изотермического процесса:
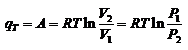
При протекании кругового процесса:
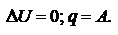
Термохимия – область физич.химии, занимающаяся изучением эн-х эффектов реакций.Если в уравнении указан ее энергетич-й эффект – это термохимическое ур-е.
V=const, 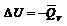
p=const, 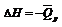
Русский ученый Гесс (1840) дал формулировку основному закону термохимии: тепловой эффект реакции, протекающей при постоянном объеме или при постоянном давлении, не зависит от пути реакции (от ее промежуточных стадий), а определяется только природой и состоянием исходных веществ и продуктов реакции.
Этот закон – прямое следствие первого закона термодинамики.
С помощью закона Гесса можно вычислять теплоты различных реакций, не проводя самих реакций.
Например: 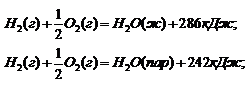
Вывод: теплота испарения одного моля воды равна 44 Дж.
23. Стандартная энтальпия образования. Следствие из закона Гесса.
Русский ученый Гесс (1840) дал формулировку основному закону термохимии: тепловой эффект реакции, протекающей при постоянном объеме или при постоянном давлении, не зависит от пути реакции (от ее промежуточных стадий), а определяется только природой и состоянием исходных веществ и продуктов реакции.Следствия из закона Гесса:1. тепловой эффект реакции равен разности между суммой теплот горения исходных веществ и суммой теплот горения продуктов реакции.Теплота горения – тепловой эффект реакции окисления данного соединения кислородом с образованием высших оксидов.Теплота образования – тепловой эффект реакции образования данного соединения из простых веществ.ю отвечающих наиболее устойчивому состоянию элементов при данных температуре и давлении.
2. тепловой эффект реакции равен разности между теплотами образования всех веществ, указанных в правой части уравнения, и теплотами образования веществ в левой части уравнения, взятых с коэффициентами перед формулами этих веществ в уравнении самой реакции.В настоящее время известны теплоты образования свыше 6000 веществ.Стандартные теплоты образования – величины теплот образования к температуре 298К и давлению 1атм.
24. Зависимость теплового эффекта химической реакции от температуры (закон Кирхгоффа).
.Температурный коэффициент теплового эффекта процесса равен изменению теплоемкости системы, происходящему в результате процесса (закон Кирхгоффа). 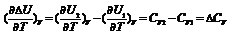
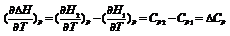
Чтобы подсчитать тепловой эффект процесса при некоторой температуре Т2, нужно знать тепловой эффект процесса при Т1, а также характер изменения теплоемкости системы в интервале температур Т1-Т2.
Обычно в роли Т1 выступает стандартная температура 298К.