Вопрос. Основные термодинамические характеристики.1,2,3 законы термодинамики.
Вопрос. Примеры расчёта эквивалента элемента, оксида, основания, соли, кислоты, окислителя, восстановителя.
- ЭЛЕМЕНТА. Определим эквивалентную массу серы в молекуле серной кислоты. Окислительное число серы в молекуле серной кислоты равно 6. По формуле эквивалентная масса серы равна M/B = 32/6 = 5,33 г/моль.
- ОКСИДА. Определим эквивалентную массу оксида серы. Окислительное число серы в молекуле оксида серы равно 4. По формуле эквивалентная масса серы рана М/В=32/4=8г/моль. Эквивалентная масса оксида по формуле равна ЭS+ЭO=8+8=16г/моль.
- ОСНОВАНИЯ. Определим эквивалентную массу молекулы оксида алюминия. По формуле ЭAl(OH)3=78/3=26г/моль.
- СОЛИ. Определим эквивалентную массу молекулы хлорида алюминия. В молекуле AlCl3 число атомов металла равно 1, а валентность равна 3. По формуле ЭAlCl3=133,5/(1*3)=44,5г/моль.
- КИСЛОТЫ. Определим эквивалентную массу молекулы серной кислоты. Серная кислота двуосновная. По формуле эквивалентная масса серной кислоты равна М/(чз Н)=98/2=49г/моль.
- ОКИСЛИТЕЛЯ.
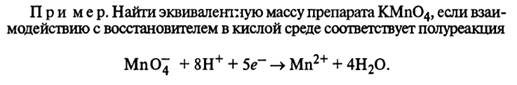

- ВОССТАНОВИТЕЛЯ.Найти эквивалентную массу Zn для данной реакции:
Zn + CuSO4 = ZnSO4 + Cu
Zn -2e → Zn2+-восстановитель
Cu2+ + 2e → Cu-окислитель
ЭZn=M/z=65/2=33
Вопрос. Основные термодинамические характеристики.1,2,3 законы термодинамики.
1. Внутренняя энергия (Δ U)- полная энергия частиц составляющих данные вещества
В химической термодинамике рассматривают системы в состоянии покоя в отсутствии внешнего покоя. В данном случае вся энергия равна внутренней.
Состоит из:
- кинетической энергии молекулярного движения
- энергии межмолекулярного взаимодействия ( притяжения и отталкивание)
- внутримолекулярная
Δ U=U2-U1
U2- конечное состояние системы
U1 - начальное
· Энергия на молекулярном уровне
· Энергия притяжения электронов к ядру
· Энергия отталкивания двух соседних ядер атомов
· Энергия притяжения ядра одного атома и электронов другого
· Энергия отталкивания электронов в двух соседних атомах
2. Энтальпия (Δ H) - теплосодержание системы
Величина равная сумме внутренней энергии и произведения объёма на давление
H=U+p*V
Функция состояния системы
Δ H=H2-H1
3.энтропия (ΔS)- мера беспорядка
Отношение количество тепла к температуре
ΔS = ΔQ/t
Функция состояния системы аддиктивная величина ровна сумме значений энтропии и её компонентов
Если система поглощает теплоту, энтропия увеличивается, а энтропия окружающей среды на столько же уменьшается.
4.Энергия Гиббса (Δ G)
Энергия, которую тело может затратить на совершение максимальной работы.
ΔG=ΔH -T*ΔS
ΔH- энтельпийный фактор
T*ΔS - энтропийный фактор
1 Закон термодинамики
Теплота, сообщенная системе, расходуется на увеличение внутренней энергии системы и на совершенствование этой системной работы.
ΔH=ΔU+p*ΔV
Q= Δ U+w - частный случай закона сокращения и превращения энергии в применении к процессам, протекающих с выделением ,поглощением или преобразованием теплоты.
Qp = Δ Uтр* Δ V= Δ Hдавление не изменяется (с учётом формулы энтольпии)
p* Δ V=- Δ U на теплообмена с окр средой Q=0
Qv= Δ U объём не изменяется V=0 (изохорный процесс)
(Закон сокращения энергии)
2 Закон термодинамики
Самопроизвольно протекают процессы в сторону увеличения энтропии
3 Закон термодинамики
В конденсированных системах при абсолютном нуле и вблизи него процесс протекает без изменения энтропии.
t= -270оС , животное не существует
Вопрос. ОВР. Виды ОВР.
ОВР – реакции, протекающие с изменением степени окисления элемента. (из за отдачи и приема электронов).
Окисление – процесс отдачи электронов.
Восстановление – процесс присоединения электронов.
Виды окислительно-восстановительных реакций:
1) Межмолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах разных веществ, например:
Н2S + Cl2 → S + 2HCl
2) Внутримолекулярные — реакции, в которых окисляющиеся и восстанавливающиеся атомы находятся в молекулах одного и того же вещества, например:
2H2O → 2H2 + O2
3) Диспропорционирование (самоокисление-самовосстановление) — реакции, в которых один и тот же элемент выступает и как окислитель, и как восстановитель, например:
Cl2 + H2O → HClO + HCl
4) Репропорционирование — реакции, в которых из двух различных степеней окисления одного и того же элемента получается одна степень окисления, например:
NH4NO3 → N2O + 2H2O
Вопрос. Примеры расчёта эквивалента элемента, оксида, основания, соли, кислоты, окислителя, восстановителя.
- ЭЛЕМЕНТА. Определим эквивалентную массу серы в молекуле серной кислоты. Окислительное число серы в молекуле серной кислоты равно 6. По формуле эквивалентная масса серы равна M/B = 32/6 = 5,33 г/моль.
- ОКСИДА. Определим эквивалентную массу оксида серы. Окислительное число серы в молекуле оксида серы равно 4. По формуле эквивалентная масса серы рана М/В=32/4=8г/моль. Эквивалентная масса оксида по формуле равна ЭS+ЭO=8+8=16г/моль.
- ОСНОВАНИЯ. Определим эквивалентную массу молекулы оксида алюминия. По формуле ЭAl(OH)3=78/3=26г/моль.
- СОЛИ. Определим эквивалентную массу молекулы хлорида алюминия. В молекуле AlCl3 число атомов металла равно 1, а валентность равна 3. По формуле ЭAlCl3=133,5/(1*3)=44,5г/моль.
- КИСЛОТЫ. Определим эквивалентную массу молекулы серной кислоты. Серная кислота двуосновная. По формуле эквивалентная масса серной кислоты равна М/(чз Н)=98/2=49г/моль.
- ОКИСЛИТЕЛЯ.
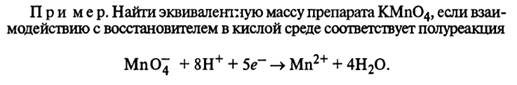

- ВОССТАНОВИТЕЛЯ.Найти эквивалентную массу Zn для данной реакции:
Zn + CuSO4 = ZnSO4 + Cu
Zn -2e → Zn2+-восстановитель
Cu2+ + 2e → Cu-окислитель
ЭZn=M/z=65/2=33
вопрос. Основные термодинамические характеристики.1,2,3 законы термодинамики.
1. Внутренняя энергия (Δ U)- полная энергия частиц составляющих данные вещества
В химической термодинамике рассматривают системы в состоянии покоя в отсутствии внешнего покоя. В данном случае вся энергия равна внутренней.
Состоит из:
- кинетической энергии молекулярного движения
- энергии межмолекулярного взаимодействия ( притяжения и отталкивание)
- внутримолекулярная
Δ U=U2-U1
U2- конечное состояние системы
U1 - начальное
· Энергия на молекулярном уровне
· Энергия притяжения электронов к ядру
· Энергия отталкивания двух соседних ядер атомов
· Энергия притяжения ядра одного атома и электронов другого
· Энергия отталкивания электронов в двух соседних атомах
2. Энтальпия (Δ H) - теплосодержание системы
Величина равная сумме внутренней энергии и произведения объёма на давление
H=U+p*V
Функция состояния системы
Δ H=H2-H1
3.энтропия (ΔS)- мера беспорядка
Отношение количество тепла к температуре
ΔS = ΔQ/t
Функция состояния системы аддиктивная величина ровна сумме значений энтропии и её компонентов
Если система поглощает теплоту, энтропия увеличивается, а энтропия окружающей среды на столько же уменьшается.
4.Энергия Гиббса (Δ G)
Энергия, которую тело может затратить на совершение максимальной работы.
ΔG=ΔH -T*ΔS
ΔH- энтельпийный фактор
T*ΔS - энтропийный фактор
1 Закон термодинамики
Теплота, сообщенная системе, расходуется на увеличение внутренней энергии системы и на совершенствование этой системной работы.
ΔH=ΔU+p*ΔV
Q= Δ U+w - частный случай закона сокращения и превращения энергии в применении к процессам, протекающих с выделением ,поглощением или преобразованием теплоты.
Qp = Δ Uтр* Δ V= Δ Hдавление не изменяется (с учётом формулы энтольпии)
p* Δ V=- Δ U на теплообмена с окр средой Q=0
Qv= Δ U объём не изменяется V=0 (изохорный процесс)
(Закон сокращения энергии)
2 Закон термодинамики
Самопроизвольно протекают процессы в сторону увеличения энтропии
3 Закон термодинамики
В конденсированных системах при абсолютном нуле и вблизи него процесс протекает без изменения энтропии.
t= -270оС , животное не существует
