Изменение свободной энергии равно максимальной полезной работе, которую совершает система в изобарно-изотермическом процессе.
Иными словами, это энергия, которую можно «изъять» из системы в виде полезной работы. Поэтому она и называется «свободной».
Понятие свободной энергии Гиббса является результатом единства первого и второго законов термодинамики.
Направление протекания реакций: Рассмотрим возможность самопроизвольного протекания химической реакции в зависимости от знака энтальпийного и энтропийного членов в выражении изменения свободной энергии. Если изменение свободной энергии меньше нуля, то реакция протекает самопроизвольно. Если ∆G = 0, начальные и конечные состояния могут существовать в равновесии. Если же изменение свободной энергии больше нуля, самопроизвольное протекание реакции невозможно. Самопроизвольно протекает обратная реакция. А так как, согласно уравнению [32], изменение свободной энергии выражается через изменения энтальпии и энтропии (в предположении, что они не зависят от температуры), то их знаки будут определять знак ∆G. В ниже рассмотренных примерах принимается, что парциальные давления всех газообразных участников реакций равны по одной атмосфере, т.е. ∆Gг=∆G°г. В этом случае можно использовать в расчётах стандартные изменения энтальпии и энтропии. Возможны четыре случая.
Первый:когда изменение энтальпии отрицательно, а изменение энтропии положительно, то изменение свободной энергии всегда отрицательно. Такие реакции самопроизвольно протекают в прямом направлении. Примером может служить реакция горения черного пороха, которая протекает по следующему суммарному уравнению:
2 КNO3 + 3С + S =N2 + ЗСО2 + К2S
Для этой реакции:
DГ H0298 = D f H0298 N2 + 3D f H0298 CO2 + D f H0298 K2S - 2D f H0298 KNO3 - 3D f H0298 C - D f H0298 S = - 582,41 кДж,
Dr S = S0298N2 + 3 S0298 CO2 + S0298 K2S - 2 S0298 KNO3 - 3 S0298 C - S0298 S = 630,34Дж/К
Следовательно,
DrG0298 = - 582,41-298ּ630,34ּ10-3 = -770,25 кДж<0,
и реакция протекает самопроизвольно.
Второй:когда изменение энтальпии положительно, а изменение энтропии отрицательно. Эти реакции в прямом направлении самопроизвольно не идут, самопроизвольно протекает обратная реакция. В качестве примера приведем реакцию термического разложения хлористого водорода на простые вещества: 2 НС1Г = Н2,г + С12,г
Изменение энтальпии этой реакции равно двум энергиям разрыва связей Н—С1 и составляет 92,3 х 2 = 184,6 кДж. Изменение энтропии равно:DrS0298 = S0298 H2 + S0298 Cl2 - 2 S0298 HCl = 130,6 + 233 - 2ּ186,7 = -19.8 Дж/К
DrG0298 = 184,6 - 298× (-19,8) ×10~3 = 190,5 кДж > О
Третий:когда как изменение энтальпии, так и энтропии отрицательны. В этом случае направление самопроизвольного процесса определяется температурой. При низкой температуре самопроизвольно идет прямая реакция, так как по абсолютной величине изменение энтальпии больше произведения температуры на изменение энтропии. Например, в реакции образования хлорида аммония из газообразных хлористого водорода и аммиака:
NН3,г + НС1Г =NH4С1К
DгH0298 = Df H0298 NH4Cl - Df H0298 Cl2 - Df H0298 NH3 = -315,4-(-92,3)-(-46,2) = -176,9 кДж
Dr S = S0298 NH4Cl - S0298 NH3 - S0298 HCl = 94,6 – 192,5 – 186,7 = -284,6 Дж/К
Т. к. при равновесии изменение свободной энергии равно нулю (DG = 0), то температура, при которой система находится в равновесии, равна 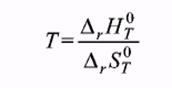 [59]
[59]
И Т = 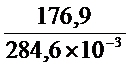 = 621,6К
= 621,6К
Четвертый:когда изменение энтальпии и энтропии положительные. Направление реакции также зависит от температуры: при низкой температуре самопроизвольно будет протекать обратная реакции, а при высокой — прямая.
Это характерно для реакций диссоциации: N2O4 « 2 N02
Для данной реакции Dг H0298= 57,З кДж; Dг S0298 = 176,6 Дж/К и DrG°298 = 4,7 кДж.
Температура, при которой устанавливается состояние равновесия: Т= 324,5 К. Ниже этой температуры самопроизвольно протекает реакция димеризации, а выше — реакция диссоциации.
Следует отметить, что стандартные величины образования изобарно-изотермического потенциала простых веществ (так же как и стандартные энтальпии образования простых веществ) принимаются равными нулю. Например: ΔfG0(H2) = 0.
Скорость химической реакции. Гомогенные и гетерогенные реакции. Факторы, определяющие скорость химических реакций. Закон действия масс. Константа скорости реакции. Влияние температуры на скорость химических реакций. Энергия активации, активированный комплекс. Энергетическая диаграмма и тепловой эффект реакции. Уравнение Аррениуса.
Скорость химической реакции определяется числом взаимодействий в единицу времени в единице объема (для гомогенных реакций) или на единице поверхности раздела фаз веществ для реакций, протекающих в гетерогенной системе. Размерность гомогенной реакции – моль/л*с, гетерогенной – моль/см2*с.
Скорость химической реакции зависит от природы реагирующих веществ, их концентрации, температуры, присутствия катализатора. Для реакций с участием твердых веществ скорость реакции зависит также от степени измельчения, а для газов – от давления.
Скорость реакции, протекающей при постоянной температуре в гомогенной среде, прямо пропорциональна произведению концентраций реагирующих веществ, возведенных в степени их стехиометрических коэффициентов согласно закону действия масс: при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в некоторых степенях.
При гетерогенных реакциях концентрации веществ, находящихся в твердой фазе, обычно не изменяются в ходе реакции и поэтому не включаются в уравнение закона действия масс.
Для реакции типа aA + bB Û cC + dD (вещества находятся в жидкой или газовой фазе) закон действия масс выражается следующим образом:
Для скорости прямой реакции: u=k[A]x[B]y, ( k – константа скорости прямой реакции)
Для скорости обратной реакции: u=k[С]n[B]k, ( k – константа скорости обратной реакции), где степени x, y, n и k для простых (идущих в одну стадию) реакций равны коэффициентам a, b, c и d в стехиометрическом уравнении реакции. Для сложных реакций степени определяются экспериментально, т.к. уравнение реакции не отражает механизм многостадийного процесса.
Зависимость скорости реакции (или константы скорости реакции) от температуры может быть выражена уравнением: ut2/ut1=kt2/kt1=gDt/10 ,
где g - температурный коэффициент скорости реакции, значение которого для большинства реакций лежит в пределах 2-4 (величина температурного коэффициента зависит от природы реагирующих веществ).
Зависимость скорости химической реакции от температуры определяется правилом Вант-Гоффа: при повышении температуры на каждые 10 0С, скорость реакции увеличивается примерно в 2-4 раза.
Уравнение Аррениуса. Зависимость скорости реакции от температуры обычно описывают уравнением Аррениуса, которое в простейшем виде можно записать как v = v0 a = v0e–Ea/RT, где v0 – скорость, которую имела бы реакция при нулевой энергии активации (фактически это частота столкновений в единице объеме). Поскольку v0 слабо зависит от температуры, все определяет второй сомножитель – экспоненциальный: с увеличением температуры этот сомножитель быстро увеличивается, причем тем быстрее, чем больше энергия активации Еа. Указанная зависимость скорости реакции от температуры называется уравнением Аррениуса, оно – одно из важнейших в химической кинетике. Если реакция подчиняется уравнению Аррениуса, логарифм ее скорости (измеренной, например, в начальный момент) должен линейно зависеть от абсолютной температуры, то есть график зависимости lnv от 1/Т должен быть прямолинейным. Наклон этой прямой равен энергии активации реакции. По такому графику можно предсказать, какова будет скорость реакции при данной температуре или же – при какой температуре реакция будет идти с заданной скоростью.
Энергия активации – это, избыточная энергия, которой должны обладать молекулы, для того, чтобы их столкновение могло привести к образованию нового вещества. Молекулы, обладающие такой энергией, называются активными молекулами. Количество активных молекул при повышении температуры резво увеличивается.
