Превращение пирувата в ацетил-КоА
Суммарная реакция:
Пируват + НАД+ + KoA-SH→Ацетил-S-KoA + НАДН + Н+ + СО2
Реакция необратима, так как ΔG = - 33,5 кДж/моль. Окислительное декарбоксилирование пирувата катализируется пируватдегидрогеназным мультиферментнымкомплексом , который объединяет три различных ферментативных активности. На первой стадии происходит декарбоксилирование ПВК при действии фермента пируватдекарбоксилазы, простетической группой которого является производное витамина B1 - тиаминпирофос-
фат.
СН3 Е1 Е1 Н
| | | |
С=О + ТПФ → ТПФ – С – СН3 + СО2
| |
ОН ОН
ТПФ – гидроксиэтил
На второй стадии происходит акцептирование ацильного остатка коферментом A (KoA-SH) и образование ацетил-КоА. Транслокация ацильного остатка катализируется вторым ферментом комплекса – дигидролипоилтрансацетилазой.Переносчиком ацильного остатка является простетическоя группа фермента – липоевая кислота
(витаминоподобное соединение), которая может находиться в двух формах: окисленной и восстановленной .
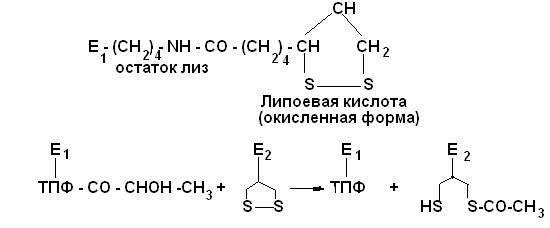
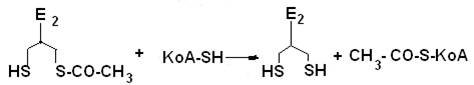
(Восстановленная форма)
На третьей стадии происходит окисление восстановленной формы липоевой кислоты. Акцептором двух атомов водорода является кофермент НАД+. Реакцию окисления катализирует третий фермент - дигидролипоилдегидрогеназа, простетическойгруппой которого является ФАД.
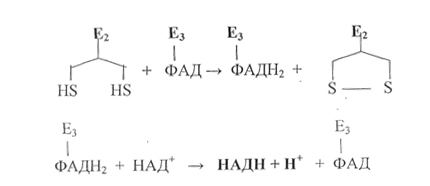 |
НАДН + Н+снабжает дыхательную цепь 2Н+ и 2ē и обеспечивает синтез 3 молей АТФ.
,
Регуляция пируватдегидрогеназного комплекса (ПДГ)
Образование ацетил-КоА из пирувата – необратимая реакция, так как ΔG = - 33,5 кДж/моль. Активность пируватдегидрогеназного комплекса регулируется различными способами: аллостерической регуляцией и путем обратимого фосфорилирования (ковалентная модификация). [АТФ] / [АДФ] и [НАД+ ] / [НАДН] - важнейшие сигналы, отражающие энергетические потребности клетки. ПДГ активен в дефосфорилированной форме. Протеинкиназа ПДГ переводит фермент в неактивную фосфорилированную форму, а фосфатаза поддерживает ПДГ в активном дефосфорилированном состоянии. При насыщении клетки АТФ (повышается молярное отношение [АТФ] / [АДФ] ) активируется протеинкиназа которая ингибирует ПДГ.
АТФ -это удаленный продукт реакции окислительного декарбоксилирования ПВК. Кроме АТФ активируют протеинкиназу продукты реакции: ацетил-КоА и НАДН. При выработке избытка энергии система регуляции блокирует образование Ацетил-КоА и, как следствие, снижает скорость ЦТК и синтеза АТФ.
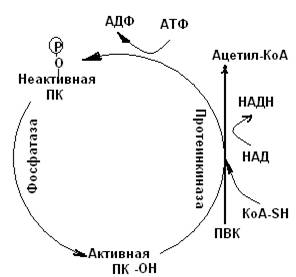
Рис.6-1. Регуляция активности протеинкиназы пируват декарбоксилазы путем
Обратимого фосфорилирования.
Цикл трикарбоновых кислот
Этот цикл называют также цикл Кребса, в честь Ганса Кребса (лауреата Нобелевской премии 1953 г.), определившего последовательность этих реакций. Цикл трикарбоновых кислот (ЦТК) – с одной стороны, является конечным этапом катаболизма белков, углеводов и липидов, который сопровождается генерированием восстановленных коферментов – универсальных энергетических субстратов – ФАДН2, НАДФН+Н+. Восстановленные коферменты далее используются митохондриальной цепью переносчиков электронов для генерации АТФ из АДФ и Фн. С другой стороны, промежуточные продукты ЦТК являются субстратами для биосинтеза эндогенных белковых веществ, соединений углеводной и липидной природы и других соединений.
Катаболическая функция ЦТК.
ЦТК - это последовательность 8 реакций, в результате которых ацетил-КоА (активная уксусная кислота) окисляется до двух молекул СО2 т.е. до конечного продукта метаболизма.
Ацетил-КоА - двууглеродная ацильная группа, характеризуется очень прочной С-С-связью. Непосредственное расщепление С-С-связи в ацетил-КоА представляет собой трудную химическую задачу. В природе существует весьма распространенное решение подобных задач – это циклическое превращение. ЦТК начинается с реакции конденсации ацетил-КоА с оксалоацетатом(ОАА) с образованием цитрата(лимонной кислоты) и заканчивается образованием ОААпри окислении малата,т.е. цикл замыкается. Все ферменты ЦТК локализуются в матриксе митохондрий и являются растворимыми белками. Исключением является сукцинат-дегидрогеназа, локализованная на поверхности внутренней мембраны митохондрий.
Реакция конденсации.
Ацетил-КоА + ОАА+ Н2О→цитрат + KoA-SH
Реакцию катализирует регулируемый фермент – цитратсинтаза.Это необратимая энергозависимая реакция, так как ΔG= - 32,2 кДж/моль. Источником энергии в этой реакции является энергия разрыва тиоэфирной связи в молекуле ацетил-КоА.
Цитрат– трикарбоновая оксикислота. Гидроксильная группа располагается у третичного атома С.По аналогия с третичными спиртами, цитрат не окисляется.
Реакция изомеризации.
В результате этой реакции происходит перемещение гидроксогруппы из 3-го во 2-е положение углеродной цепи цитрата и образование изомера лимонной кислоты - изоцитрата. Аконитаза – фермент, обладающий абсолютной стереоспецифичностью, катализирует последовательное отщепление Н2О, а затем присоединение ее в другое положение.
Цитрат→аконитат → изоцитрат
↓↓
Н2ОН2О
Изоцитрат - изомер лимонной кислоты, у которой ОН-группа располагается у вторичного атома углерода. По аналогии с вторичными спиртами изоцитрат может подвергаться окислению с образованием кетокислоты.
