Окислительно-восстановительные потенциалы и направление
Протекания окислительно-восстановительных реакций
В разделе 9.2 было показано, что при работе гальванического элемента Даниэля-Якоби в нём протекает реакция,
Zn + CuSO4®ZnSO4 + Cu
Zn + Cu2+ ® Zn2+ + Cu
которую можно представить в виде двух электродных процессов (полуреакций), протекающих на электродах:
окисление цинка Zn ® Zn2+ + 2e– 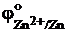 = -0,763 В;
= -0,763 В;
восстановление ионов Cu2+ Cu2+ + 2e– ® Cu 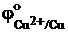 = +0,337 В.
= +0,337 В.
Из сравнения электродных потенциалов этих процессов видно, что система, в которой принимает участие окислитель – ионы Cu2+ (эту систему принято называть окислительной системой) имеет большую алгебраическую величину электродного потенциала. Система, в которой принимает участие восстановитель – металлический цинк (эту систему принято называть восстановительной системой), имеет меньшую алгебраическую величину электродного потенциала. Из этого вытекает общее правило:
В любой окислительно-восстановительной реакции система с большей величиной электродного потенциала является окислительной системой, система с меньшей величиной электродного потенциала является восстановительной системой.
Это правило можно также сформулировать иначе:
окислительно-восстановительная реакция протекает в прямом направлении в том случае, если электродный потенциал окислительной системы больше потенциала восстановительной.
Иногда для краткости говорят, что потенциал окислителя должен быть больше потенциала восстановителя, подразумевая, тем не менее, что соответствующие потенциалы характеризуют окислительную и восстановительную системы.
Например, водород из раствора соляной кислоты восстанавливается металлом 2Me + 2HCl ® 2MeCl + H2
2Me + 2H+ ® 2Me+ + H2
в том случае, если потенциал 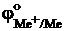 восстановительной системы Me ® Me+ + e– меньше потенциала окислительной системы 2H+ + 2e– ® H2 (
восстановительной системы Me ® Me+ + e– меньше потенциала окислительной системы 2H+ + 2e– ® H2 ( 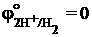 В).
В).
Таким образом, реакция взаимодействия металла и кислоты с выделением водорода будет протекать самопроизвольно, если потенциал металла 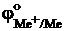 < 0 .
< 0 .
Если все металлы расположить в ряд по возрастанию стандартных электродных потенциалов, отвечающих процессу Men+ + ne– ® Me, то получится так называемый электрохимический ряд напряжений металлов.
Li K Na Mg Al Ti Mn Zn Fe Pb H Bi Cu Ag Pt Au
В этом ряду до водорода находятся металлы с отрицательными потенциалами, т.е. металлы, способные восстанавливать водород из кислот, а после водорода – металлы с положительными потенциалами, не реагирующие с кислотами с выделением водорода.
Чем меньше величина электродного потенциала металла, тем более сильным восстановителем он является. Поэтому любой металл может быть восстановлен из водного раствора своей соли более активным металлом, стоящим в ряду напряжений левее данного металла. Это правило не выполняется для щелочных и щелочноземельных металлов, т.к. катионы этих металлов – более слабые окислители, чем вода, – и, поэтому, они не могут быть восстановлены в водном растворе; вместо них восстанавливается вода и выделяется водород (см. также раздел 9.5.2 данной лекции).
Следует обратить внимание, что в гальваническом элементе всегда окисляется, т.е. является анодом, именно более активный металл. Например, в реакции, протекающей в элементе Даниэля-Якоби, медь вытесняется металлическим цинком
Zn + CuSO4 ® ZnSO4 + Cu
Zn + Cu2+ ® Zn2+ + Cu,
так как потенциал восстановительной системы 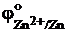 = -0,763 В меньше потенциала окислительной системы
= -0,763 В меньше потенциала окислительной системы 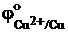 = +0,337 В.
= +0,337 В.
Таким образом, чем больше потенциал электродной системы, тем более сильными окислительными свойствами обладает вещество, принимающее электроны. И, наоборот, чем меньше алгебраическая величина потенциала электродной системы, тем более сильными восстановительными свойствами обладает вещество, отдающее электроны.
Некоторые металлы, например, медь, не способные вытеснять водород из таких кислот, как соляная и разбавленная серная, легко взаимодействуют с разбавленной азотной кислотой. Это связано с тем, что азотная кислота может окислять нитрат-ионами, и поэтому в данном случае потенциал окислительной системы больше, чем потенциал восстановительной:
3Cu + 8 HNO3 ® 3Cu(NO3)2 + 2NO + 4H2O
система
восстановительная: Cu ® Cu2+ + 2e– 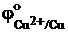 = +0,34 В ;
= +0,34 В ;
система
окислительная: NO3– +4 H+ +3e– ® NO + 2H2O 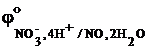 = + 0,96 В.
= + 0,96 В.
В азотной кислоте может также раствориться серебро: 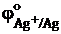 = +0,80 В, но не золото
= +0,80 В, но не золото 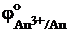 = +1,50 В и не платина
= +1,50 В и не платина 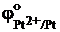 = +1,19 В.
= +1,19 В.
Электролиз
Электролиз – это совокупность электрохимических процессов, происходящих на электродах при прохождении электрического тока через расплав или раствор электролитов. Как и в случае гальванического элемента, электрод, на котором происходит восстановление, называется катодом, а электрод, на котором происходит окисление – анодом. Но при электролизе катод заряжается внешним источником постоянного электрического тока отрицательно, а анод – положительно. Причина этого заключается в том, что процессы, протекающие при электролизе, противоположны процессам, которые происходят при работе гальванического элемента. При электролизе химическая реакция осуществляется за счёт энергии, подводимой извне, в то время как при работе гальванического элемента энергия самопроизвольно протекающей химической реакции превращается в электрическую энергию.
9.5.1 Электролиз расплавов
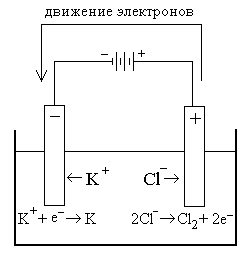 Примером электролиза расплавов может служить электролиз расплава хлорида калия (рис. 9.2). При прохождении тока через расплав KCl катионы калия движутся под действием электрического поля к отрицательно заряженному электроду, где восстанавливаются, взаимодействуя с электронами, приходящими от источника постоянного тока: K+ + e– ® K (катодный процесс).
Примером электролиза расплавов может служить электролиз расплава хлорида калия (рис. 9.2). При прохождении тока через расплав KCl катионы калия движутся под действием электрического поля к отрицательно заряженному электроду, где восстанавливаются, взаимодействуя с электронами, приходящими от источника постоянного тока: K+ + e– ® K (катодный процесс).
Анионы хлора перемещаются к положительному электроду и, отдавая электроны, окисляются: 2Cl– ® Cl2 + 2e– (анодный процесс).
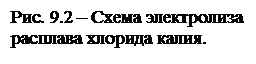 При сложении уравнений процессов, происходящих на электродах, получается суммарное уравнение окислительно-восстановительной реакции: 2 K+ + 2 Cl– ® 2 K + Cl2
При сложении уравнений процессов, происходящих на электродах, получается суммарное уравнение окислительно-восстановительной реакции: 2 K+ + 2 Cl– ® 2 K + Cl2
или в молекулярном виде 2KCl ® 2K + Cl2 .
Эта реакция не может протекать самопроизвольно. Для её осуществления требуется внеш-
няя энергия, поступающая от источника постоянного электрического тока.
9.5.2 Электролиз водных растворов
При рассмотрении процессов, протекающих при электролизе водных растворов, следует учитывать, что на электродах могут окисляться или восстанавливаться не только ионы электролита, но и молекулы воды. Кроме того, в ряде случаев может окисляться материал анода.
Аноды, материал которых не подвергается электрохимическому окислению, называются инертными. Примером инертного анода является графитовый анод. Анод, материал которого способен окисляться при электролизе, называется активным анодом. Как правило, аноды, изготовленные из неблагородных металлов – железа, меди, цинка и др. – являются активными анодами.
Какие именно электрохимические процессы будут протекать на катоде или аноде при электролизе водного раствора зависит от соотношения алгебраических величин электродных потенциалов соответствующих электрохимических систем. Из нескольких возможных окислителей на катоде в первую очередь будет восстанавливаться наиболее сильный окислитель, т.е. тот окислитель, электродная система которого характеризуется наибольшим электродным потенциалом. На аноде в первую очередь будет окисляться наиболее сильный восстановитель из нескольких возможных, т.е. тот восстановитель, электродная система которого характеризуется наименьшим электродным потенциалом.
Пример 9.4 Электролиз водного раствора сульфата натрия с инертным анодом.
В растворе содержатся ионы Na+, SO42– и молекулы H2O. На катоде из двух теоретически возможных процессов восстановления
Na+ + e– ® Na 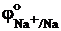 = -2,71 В
= -2,71 В
2H2O + 2e– ® H2 + 2OH– 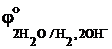 = -0,82 В
= -0,82 В
будет происходить процесс восстановления более сильного окислителя. Поскольку 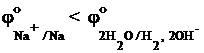 , то молекулы воды являются более сильным окислителем, чем ионы натрия, и на катоде будет происходить восстановление воды. Следует заметить, что потенциал
, то молекулы воды являются более сильным окислителем, чем ионы натрия, и на катоде будет происходить восстановление воды. Следует заметить, что потенциал 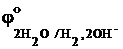 = -0,82 В характеризует систему в стандартных условиях, т.е. когда C(OH–) = 1 моль/л. По уравнению Нернста можно рассчитать, что в нейтральном водном растворе, когда C(OH–) = 10–7 моль/л, значение этого потенциала ещё выше:
= -0,82 В характеризует систему в стандартных условиях, т.е. когда C(OH–) = 1 моль/л. По уравнению Нернста можно рассчитать, что в нейтральном водном растворе, когда C(OH–) = 10–7 моль/л, значение этого потенциала ещё выше: 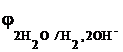 = -0, 41 В.
= -0, 41 В.
Из этого следует очень важный вывод: при электролизе водных растворов солей щелочных, щелочноземельных металлов, магния и алюминия, потенциалы восстановления ионов которых намного меньше потенциала восстановления воды, на катоде никогда не выделяется металл; вместо этого происходит восстановление воды и выделение водорода.
На аноде из двух возможных процессов окисления
2SO42– ® S2O82– + 2e– 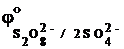 = +2,01 В,
= +2,01 В,
2H2O ® O2 + 4 H+ + 4e– 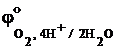 = +1,23 В
= +1,23 В
будет происходить окисление наиболее сильного восстановителя, каковым является вода, т.к. 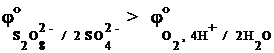 .
.
При электролизе водных растворов солей, содержащих сложные анионы, такие как сульфат-, нитрат-, карбонат-, силикат-, а также фторид-анионы, потенциал окисления которых превышает потенциал окисления воды, на аноде не происходит окисление этих анионов; вместо этого окисляется вода, и выделяется кислород.
Таким образом, электролиз водного раствора сульфата натрия, (а также водных растворов солей, образованных катионами щелочных, щелочноземельных металлов, магния, алюминия и анионами кислородсодержащих кислот или фторид-анионами) сводится к разложению воды.
 катодный процесс: 2H2O + 2e– ® H2 + 2OH– 2
катодный процесс: 2H2O + 2e– ® H2 + 2OH– 2
анодный процесс: 2H2O ® O2 + 4H+ + 4e– 1
 | |||
 |
6H2O ® 2 H2 + 4OH– + 4H+ + O2
 6H2O ® 2H2 + 4H2O + O2 2H2O ® 2H2 + O2
6H2O ® 2H2 + 4H2O + O2 2H2O ® 2H2 + O2
Аналогично можно показать, что электролиз водных растворов серной кислоты, гидроксида натрия и других щелочей также сводится к разложению воды.
Пример 9.5 Электролиз водного раствора KI с инертным анодом.
В растворе KI содержатся ионы К+, I– и молекулы воды. Из двух возможных катодных процессов
K+ + e– ® K 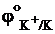 = -2,93 В
= -2,93 В
2H2O + 2e– ® H2 + 2OH– 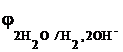 = - 0,41 В (при pH = 7)
= - 0,41 В (при pH = 7)
будет протекать процесс, характеризующийся более высоким значением электродного потенциала, т.е. процесс восстановления воды (см. также пример 9.4).
Из двух возможных анодных процессов
2I– ® I2 + 2e– 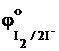 = + 0,55 В
= + 0,55 В
2H2O ® O2 + 4 H+ + 4e– 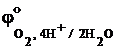 = +1,23 В
= +1,23 В
будет протекать процесс, характеризующийся меньшим электродным потенциалом, т.е. процесс окисления более сильного восстановителя, которым в данном случае являются иодид-ионы.
При электролизе водных растворов бескислородных кислот и их солей (за исключением плавиковой кислоты и фторидов) на аноде происходит окисление аниона и выделение простого вещества (неметалла).
Таким образом, при электролизе водного раствора KI протекает следующая окислительно-восстановительная реакция:
 катодный процесс 2H2O + 2e– ® H2 + 2OH– 1
катодный процесс 2H2O + 2e– ® H2 + 2OH– 1
анодный процесс 2I– ® I2 + 2e– 1
 2H2O + 2I– ® H2 + I2 + 2 OH–
2H2O + 2I– ® H2 + I2 + 2 OH–
2KI + 2H2O ® H2 + I2 + 2KOH
При этом на катоде выделяется водород, а на аноде – йод; в прикатодном пространстве накапливается гидроксид калия.
Пример 9.6 Электролиз водного раствора CuSO4 с инертным анодом.
В растворе CuSO4 содержатся ионы Cu2+ , SO42– и молекулы воды. Из двух возможных катодных процессов
Cu2+ + 2e– ® Cu 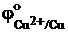 = +0,337 В
= +0,337 В
2H2O + 2e– ® H2 + 2OH– 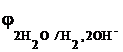 = - 0,41 В (при pH = 7)
= - 0,41 В (при pH = 7)
будет протекать процесс, характеризующийся большим электродным потенциалом, т.е. процесс восстановления ионов Cu2+, которые являются более сильным окислителем, чем молекулы воды.
При электролизе водных растворов солей малоактивных металлов, таких как Bi, Cu, Hg, Ag, Au, Pt, потенциал восстановления ионов которых превышает потенциал восстановления воды, на катоде всегда происходит выделение металла. Если потенциал восстановления металла близок к потенциалу восстановления воды ( 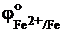 = -0,44 В,
= -0,44 В, 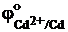 = -0,41 В,
= -0,41 В, 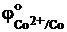 = = -0,28 В,
= = -0,28 В, 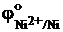 = -0,25 В,
= -0,25 В, 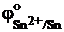 = -0,14 В), то на катоде может происходить одновременное выделение металла и водорода.
= -0,14 В), то на катоде может происходить одновременное выделение металла и водорода.
Из двух возможных анодных процессов
2SO42– ® S2O82– + 2e– 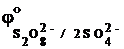 = +2,01 В,
= +2,01 В,
2H2O ® O2 + 4 H+ + 4e– 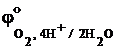 = +1,23 В
= +1,23 В
будет протекать процесс, характеризующийся меньшим электродным потенциалом, т.е. процесс окисления воды, которая является более сильным восстановителем, чем сульфат-ионы (см также пример 9.4).
Таким образом, при электролизе водного раствора CuSO4 на катоде выделяется металлическая медь, на аноде происходит выделение кислорода, а в прианодном пространстве накапливается серная кислота.
 катодный процесс: Cu2+ + 2e– ® Cu 2
катодный процесс: Cu2+ + 2e– ® Cu 2
анодный процесс: 2H2O ® O2 + 4H+ + 4e– 1
 2 Cu2 + 2 H2O ® 2 Cu + O2 + 4H+
2 Cu2 + 2 H2O ® 2 Cu + O2 + 4H+
2CuSO4 + 2H2O ® 2Cu + O2 + 2H2SO4
Пример 9.7 Электролиз водного раствора CuSO4 с активным (медным) анодом.
Как уже было показано в примере 9.6, на катоде восстанавливаются ионы меди: Cu2+ + 2e– ® Cu.
Случай электролиза с активным анодом отличается от случаев электролиза с инертным анодом тем, что материал анода также может окисляться. Например, при электролизе водного раствора сульфата меди с медным анодом на аноде, в принципе, могли бы протекать три конкурирующих процесса:
2H2O ® O2 + 4 H+ + 4e– 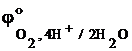 = +1,23 В;
= +1,23 В;
2SO42– ® S2O82– + 2e– 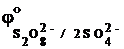 = +2,01 В;
= +2,01 В;
Cu ® Cu2+ + 2e– 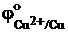 = +0,337 В.
= +0,337 В.
Сопоставление электродных потенциалов показывает, что меньшим потенциалом характеризуется процесс окисления меди. Таким образом, металлическая медь является наиболее сильным восстановителем из трёх возможных (H2O, SO42–, Cu). Поэтому на аноде происходит окисление металлической меди, которая переходит в раствор в виде ионов: Cu ® Cu2+ + 2e–, на катоде происходит восстановление ионов меди до металла Cu2+ + 2e– ® Cu, и весь процесс сводится к переносу меди с анода на катод.
Этот процесс применяется для электролитической очистки (рафинирования) меди, которое заключается в том, что к аноду электролизёра присоединяют загрязнённую примесями медную болванку, а на катоде происходит выделение чистой меди, перешедшей с анода на катод в результате протекающих электрохимических процессов; нерастворимые примеси при этом осаждаются на дно электролизёра.
9.5.3 Применение электролиза в промышленности
1. Получение щелочных, щелочноземельных металлов, алюминия электролизом расплавов их солей.
2. Электроэкстракция металлов. Руду металла подвергают обработке определёнными реагентами, в результате чего металл переходит в раствор. После очистки раствора от примесей металл выделяют электролизом.
3. Электролитическое рафинирование (см. пример 9.7).
4. Гальваностегия – нанесение путём электролиза на поверхность металлических изделий слоёв других металлов с целью защиты этих изделий от коррозии и в декоративных целях.
5. Гальванопластика – получение точных металлических копий с рельефных предметов электроосаждением металла. Методом гальванопластики изготавливают матрицы для прессования различных изделий.
