Пирометаллургия, гидрометаллургия и электрометаллургия.
 Способы получения металлов обычно разделяют на три типа:
Способы получения металлов обычно разделяют на три типа:
· пирометаллургические (восстановление при высоких температурах);
· гидрометаллургические (восстановление из солей в растворах);
· электрометаллургические (электролиз раствора или расплава).
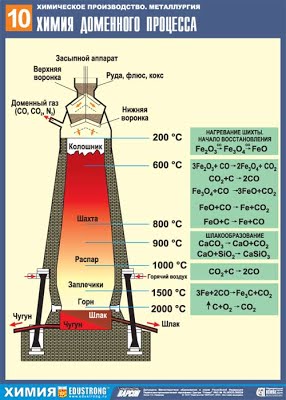
Пирометаллургически получают (методы извлечения металлов из руд под действием высоких температур. Оксидные руды и оксиды восстанавливают углем, оксидом углерода (II), более активным металлами (алюминий, магний)): чугун, сталь, медь, свинец, никель, хром и другие металлы.
FeO + C –> Fe + CO
Fe2O3 + 2Al –> 2Fe + Al2O3
Гидрометаллургически получают (методы получения металлов, основанные на химических реакциях, протекающих в растворах): золото, цинк, никель и некоторые другие металлы.
CuSO4 + Fe –> FeSO4 + Cu
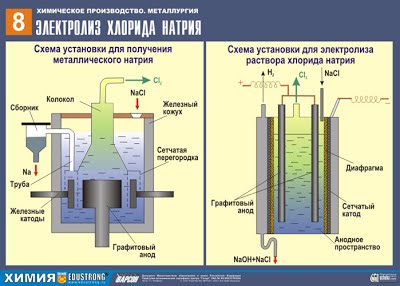
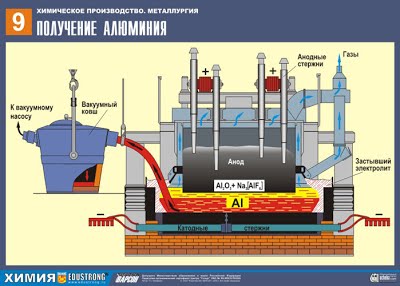
Электрометаллургически получают (выделение металлов из их солей и оксидов под действием электрического тока): щелочные и щёлочноземельные металлы, алюминий, магний и другие металлы.
При разработке технологии получения химических веществ используются законы термодинамики, кинетики, теплотехники, физико-химического анализа и др. Учитываются, естественно, и экономические условия. В случае, если реакция обратима, применяется принцип Ле Шателье:
Если на систему, находящуюся в равновесии, воздействовать извне, то равновесие в системе сместится в сторону той реакции (прямой или обратной), которая приводит к частичной компенсации этого воздействия.
Химические методы применяются и при очистке выбросов, а также сточных вод химических производств.
Коррозия.
Коррозия наносит прямой ущерб, ежегодно от неё теряется около 1/3 произведённого за год во всём мире металла, но и косвенно разрушает конструкции, на которые был затрачен труд (машины, крыши, памятники архитектуры, мосты…) Тратятся ежегодно огромные средства на борьбу с этим явлением. Коррозия не щадит памятники архитектуры: Царь-пушку (1586 г.), Царь-колокол (1735 г.), медный всадник в Санкт-Петербурге, Памятник Минину и Пожарскому в Москве, только в этом случае налёт тёмно-зелёный, его называют патиной. Неизлечимо больна Эйфелева башня – символ Парижа, она изготовлена из обычной стали и необратимо ржавеет и разрушается. Башню красили 18 раз, отчего её масса (9.00 тонн) каждый раз увеличивается на 70 тонн.
В результате коррозии уменьшается прочность, блеск, снижается электропроводность, возрастает трение между деталями.
Учебник Г.Е.Рудзитис, Ф.Г.Фельдман, Химия 11 класс, страница 1108 - 111.
1. Что такое коррозия?
2. Виды коррозии – химическая и электрохимическая.
3. Методы защиты от коррозии.
Сплавы черные и цветные.
Работа с учебником, заполнение таблицы.
Учебник Г.Е.Рудзитис, Ф.Г.Фельдман, Химия 11 класс, страница 150 – 154.
| Сплав | Состав | Свойства | Область применения |
Демонстрация. В процессе обсуждения областей применения сплавов учитель демонстрирует образцы из коллекции «Металлы и сплавы», отмечая при этом их физические свойства, стойкость к коррозии, преимущества сплавов.
| Название, состав. | Свойства. | Применение. |
| Алюминевые сплавы (Al,Mg,Zn,Mn,Be) | Легкость, высокая электро и тепло проводность, коррозионная стойкость,высокая удельная прочность. | В авиации, в машиностроении, электротехнические устройства. |
| Железоуглеродистые сплавы (чугун, сталь), ферросплавы (С,Р,S, Mn,Fe,W). | Механическая прочность, твердость. Упругость, коррозионная устойчивость. | Конструкционные материалы для всех областей техники. |
| Медные сплавы(Cu,Zn,Al,Sn,Ni,P). | Прочность,высокая электропроводность и коррозионная стойкость, пластичность. | Теплотехническая аппаратура, подшипники, втулки, пружины,декаративно-прикладные изделия. |
| Твердые сплавы (сталь, Со,Ni,Mo). | Высокая твердость, тугоплавкость, износоустойчивость. | Рабочие части буровых инструментов, инструмент для обработки металлов. |
| Типографские сплавы (Pb,Sb,Sn и др.) | Низкие температуры плавления и хорошие литейные свойства. | Элементы наборов шрифта, полиграфическая промышленность. |
| Титановые сплавы (Мn,W,Ni,Cu,Mo). | Легкость, высокая прочность, коррозионная стойкость. | Ракетостроение, авиация, химическая аппаратура. |
Учащиеся отвечают на вопросы учебника на странице 154:
Доменное производство чугуна, записать химические уравнения в тетрадь и на доске.
7. Лабораторная работа № 10
