Химическая кинетика. Скорость химической реакции. Химическое равновесие. Правило Ле Шателье-Брауна.
Характер смещения под влиянием внешних воздействий можно прогнозировать, применяя принцип Ле Шателье: если на систему, находящуюся в равновесии оказывается воздействие извне, то равновесие в системе смещается так, чтобы ослабить внешнее воздействие.
1. Влияние концентраций.
Повышение концентрации одного из реагирующих веществ смещает равновесие в сторону расходования вещества. Понижение концентрации – в сторону образования вещества.
2. Влияние температуры.
Повышение температуры смещает равновесие в сторону реакции, идущей с поглощением теплоты (эндотермической), а понижение температуры смещает равновесие в сторону реакции, идущей с выделением теплоты (экзотермической).
3. Влияние давления.
Повышение давления смещает равновесие в сторону реакции, идущей с уменьшением объема и, наоборот, понижение давления – в сторону реакции, идущей с увеличением объема.(2).
Пример 1. Как сместится химическое равновесие при синтезе аммиака в экзотермической реакции?
Решение. При повышении температуры в экзотермической реакции
3H2(г) + N2(г) = 2NH3(г);
ΔH0 = -92,4 кДж
реакция протекает с выделением теплоты, равновесие должно сдвигаться влево (в сторону исходных веществ).
Скорость реакции:
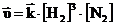 ;
;
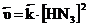 .
.
При увеличении давления в три раза концентрация веществ увеличивается также в три раза:
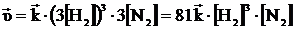 ;
;
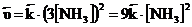 .
.
Такое изменение концентрации увеличивает скорость прямой реакции в 81 раз, а обратное в 9 раз, т.е. при увеличении давления в три раза состояние равновесия достигается быстрее в 81 : 9 = 9 раз. В левой части уравнения участвуют в реакции 3 + 1 = 4 моль веществ, а в правой части уравнения получается 2 моль, поэтому увеличение давления приводит к повышению выхода целевого продукта, что подтверждает принцип Ле Шателье(2).
Пример 2. При синтезе аммиака N2(г) + 3H2(г)  2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ,
2NH3(г) равновесие установилось при следующих концентрациях реагирующих веществ, 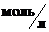 : [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
: [N2] = 4; [H2] = 2; [NH3] = 6. Рассчитайте константу равновесия этой реакции и исходные концентрации азота и водорода.
Решение. Константа равновесия реакции
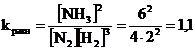 .
.
Начальная концентрация вещества складывается из равновесной концентрации этого вещества и количества вещества, израсходованного на образование равновесной концентрации продукта реакции. На основе уравнения реакции определяем количество израсходованного N2(2):
на образование 2 моль NH3 расходуется 1 моль N2;
на образование 6 моль NH3 расходуется x моль N2.
Отсюда 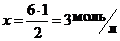 .
.
Начальная концентрация азота
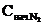 = [N2] + x = 4 + 3 = 7
= [N2] + x = 4 + 3 = 7  .
.
Аналогично составим пропорцию:
на образование 2 моль NH3 расходуется 3 моль H2;
на образование 6 моль NH3 расходуется y моль H2.
Отсюда 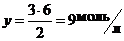
Начальная концентрация водорода
 = [H2] + y = 2 + 9 = 11
= [H2] + y = 2 + 9 = 11  .
.
Ответ: начальные концентрации 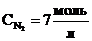 ;
; 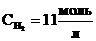
Тема№3. Дисперсные системы. Растворы.
Концентрации растворов
Пример 1. В водном растворе хлорида бария объемом 0,800 л с плотностью 1,20 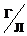 содержится BaCl2 массой 192 г. Вычислите массовую долю и молярную концентрацию.
содержится BaCl2 массой 192 г. Вычислите массовую долю и молярную концентрацию.
Решение. а) Массовая доля (w), выраженная в процентах, показывает, сколько граммов растворенного вещества содержится в 100 г раствора.
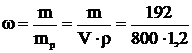 = 0,2 или 20%,
= 0,2 или 20%,
где m – масса ВаСl2;
mp – масса раствора, г (mp = V·ρ = 800·1,2 = 960 г);
V – объем раствора, мл (0,8 л = 800 мл);
ρ – плотность раствора, 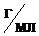 .
.
б) Молярная концентрация показывает число молей растворенного вещества в 1 л раствора и выражается в 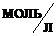 . Массу ВаСl2 в 1 л раствора находят из соотношения
. Массу ВаСl2 в 1 л раствора находят из соотношения
в 800 мл раствора содержится 192 г ВаСl2
в 1000 мл раствора содержится x г ВаСl2
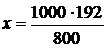 = 240 г BaCl2
= 240 г BaCl2
Молярная масса ВаСl2 равна (М(ВаСl2) = 137 + (35,5·2)) = 208 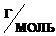 , следовательно, число молей ВаСl2, содержащихся в 1 л раствора, равно
, следовательно, число молей ВаСl2, содержащихся в 1 л раствора, равно
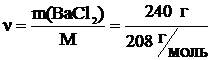 = 1,15 моль.
= 1,15 моль.
Молярная концентрация
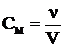 = 1,15
= 1,15 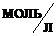 .
.
Пример 2. Какой объем раствора (1) KOH с массовой долей ω1 = 34,9% (ρ1 = 1,34 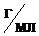 ) следует взять для приготовления раствора (2) объемом V2 = 250 мл с ω2 = 11,0% (ρ2 = 1,1
) следует взять для приготовления раствора (2) объемом V2 = 250 мл с ω2 = 11,0% (ρ2 = 1,1 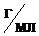 ). Чему равна молярная концентрация С2 , полученного раствора?
). Чему равна молярная концентрация С2 , полученного раствора?
Решение. К решению нужно подойти, исходя из неизменности в исходном и полученном растворах: 1) массы КОН, г; 2) количества КОН, моль. Более рационален второй подход.
Количество КОН
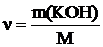
где m – масса КОН;
М – молярная масса КОН.
Учитывая, что m = V2·ρ2·ω2, получаем
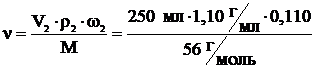 = 0,539 моль.
= 0,539 моль.
Молярная концентрация
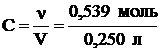 = 2,16
= 2,16 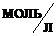
(обратите внимание на соответствие размерностей величин).
Для исходного раствора
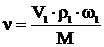 ,
,
Отсюда объем исходного раствора равен
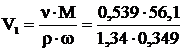 = 64,7 мл.
= 64,7 мл.
