М.А.Молявко, Л.Е.Салова, А.Т.Чанышева
ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ»
М.А.Молявко, Л.Е.Салова, А.Т.Чанышева
УЧЕБНОЕ ПОСОБИЕ
ПО КОЛИЧЕСТВЕННОМУ
ХИМИЧЕСКОМУ АНАЛИЗУ
Рекомендовано Министерством образования
Республики Башкортостан в качестве учебного пособия для студентов технических университетов
Уфа 2005
УДК 513.062
ББК 24.46
М 75
Рецензенты:
Заведующий кафедрой аналитической химии химического факультета
Башкирского государственного университета, доктор химических наук,
профессор Ф.Х. Кудашева
Директор Уфимского представительства ЗАО «Петон», руководитель
регионального центра журнала «Химическая технология»,
доктор химических наук, профессор Н.Л. Егуткин
Молявко М.А., Салова Л.Е., Чанышева А.Т.
М.75 Учебное пособие по количественному химическому анализу:
Учеб. пособие.-Уфа: Изд-во УГНТУ, 2005.-111 с.
ISBN 5-7831-0678-X
В данном пособии по химическому количественному анализу, состоящем из четырех частей, рассматриваются следующие методы: кислотно-основное титрование, редоксиметрия (перманганатометрия и иодометрия), комплексонометрия и гравиметрия. Содержит изложение теоретических основ, лабораторные работы и методики их проведения, включает вопросы и задачи, а также необходимые приложения. Пособие составлено в соответствии с программой по аналитической химии и рекомендуется для студентов химико-технологических специальностей технических университетов.
УДК 513.062
ББК 24.46
ISBN 5-7831-0678-X © Уфимский государственный нефтяной
технический университет, 2005
© Молявко М.А., Салова Л.Е.,
Чанышева А.Т., 2005
В B E Д Е Н И Е
Аналитическая химия – это наука, разрабатывающая теоретические основы, методы и средства химического анализа, определения химического состава исследуемого вещества и его строение.
Химический анализ широко используется для контроля производства и качества продукции ряда отраслей народного хозяйства – химической, нефтеперерабатывающей, пищевой, фармацевтической, биотехнологии и т.д.
Создание и совершенствование методов, средств и методик анализа – это основы аналитической химии.
Методы – это универсальные и теоретически обоснованные способы определения состава безотносительно к определенному компоненту и к анализируемому объекту.
Средства – приборы, реактивы, стандратные образцы, программы для компьютеров и т. д.
Методика анализа – это подробное описание анализа данного объекта с использованием выбранного метода.
В аналитической химии наряду с другими анализами можно выделить качественный и количественный анализы.
Качественный анализ решает вопрос о том, какие компоненты включает анализируемый объект.
Количественный анализ – дает сведения о количественном содержании всех или отдельных компонентов.
Методы определения можно классифицировать по характеру измеряемого состава или по способу регистрации составляющего сигнала. Методы определения можно условно разделить: на химические, физические и биологические.
Химические методы базируются на химических (в том числе электрохимических) реакциях.
Физические методы основаны на физических явлениях и процессах (взаимодействие вещества с потоком энергии), биологические – на явлении жизни. Основные требования к методам аналитической химии: правильность и хорошая воспроизводимость результатов, избирательность, экспрессность, простота анализа, возможность его автоматизации.
В основе химического метода обнаружения и определения лежат химические реакции трех типов: кислотно-основные, окислительно-восстановительные и комплексообразования. Наибольшее значение среди химических методов имеют гравиметрический, титриметрический или объемный. Они называются классическими методами анализа.
ТИТРИМЕТРИЧЕСКИЕ МЕТОДЫ АНАЛИЗА.
СУЩНОСТЬ ТИТРИМЕТРИИ
Вещества реагируют между собой в эквивалентных количествах (n1=n2). Так как n = С(1/z A)·V, где С(1/z A) - молярная концентрация эквивалента, а V - объем, в котором растворено вещество, то для двух стехиометрически реагирующих веществ справедливо соотношение
С1(1/z1 A)·V1 = С2(1/z2 В)·V2 (1)
из этого соотношения можно найти неизвестную концентрацию одного из веществ (пусть это будет С2(1/z2В)), если известны объем его раствора, объем и концентрация прореагировавшего с ним вещества. Если известна молярная масса эквивалента М2(1/z2 В), находят массу вещества:
m2 = C2(1/z2 B)·M2(1/z2 B)
Чтобы зафиксировать конец реакции, который называется точкой эквивалентности или точкой стехеометричности (ТЭ), раствор с известной концентрацией вещества (его называют титрантом, Т) постепенно, небольшими порциями, добавляют к раствору определяемого вещества А до ТЭ. Этот процесс называют титрованием.
Реакция, применяемая в титриметрическом методе, должна отвечать следующим требованиям:
1. проходить с достаточной скоростью;
2. быть строго стехеометричной;
3. протекать количественно (константа равновесия должна быть высокой);
4. должен существовать способ фиксирования точки эквивалентности.
Конец титрования экспериментально устанавливают по изменению цвета индикатора или какого-либо физико-химического свойства раствора. Эта точка называется «конечная точка титрования (КТТ)», которая обычно не совпадает с теоретически рассчитанной точкой эквивалентности.
В титриметрическом анализе используют реакции всех типов – с переносом протона, электрона, электронной пары, а также процессы осаждения (табл. 1). Методы титриметрического анализа можно классифицировать по характеру эмпирической реакции, лежащей в основе определения, и по способу титрования.
Таблица 1
Классификация титриметрических методов по характеру реакции.
| Метод титрования, тип реакции | Подгруппы методов | Вещества, применяемые для приготовления титрантов |
| I. кислотно-основные (метод нейтрализации) Н3О+ + ОН- = 2Н2О | 1) Ацидиметрия (Н3О+) 2) Алкалиметрия (ОН-) | HCl |
| NaOH, Na2CO3, Na2B4O7∙10H2O | ||
| Продолжение табл.1 | ||
 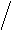    II. окислительно-восстановительные (метод редоксиметрии) аОх1 + bRed(2) = aRed(1) bOх2 II. окислительно-восстановительные (метод редоксиметрии) аОх1 + bRed(2) = aRed(1) bOх2 | 1) Перманганатометрия 2) Иодометрия 3) Дихроматометрия 4) Броматометрия 5) Иодатометрия 6) Цериметрия 7) Ванадатометрия 8) Титанометрия 9) Хромометрия 10) Аскорбинометрия | KMnO4 I2 K2Cr2O7 KВrO3 KIO3 Ce(SO4)2 NH4VO3 TiCl3 CrCl3 НО–С= С–ОН О=С СН-СН-СН2ОН О ОН |
| III. комплексонометрическое M + L = ML | 1) Меркуриметрия 2) Комплексонометрия | Hg(NO3)2 ЭДТА (этилендиаминтетраацетат) |
| IV. методы осаждения M + X = MX¯тв | Аргентометрия Меркурометрия | AgNO3 Hg2(NO3)2 |
Титрование как при определении концентраций рабочих растворов, так и при выполнении анализов, можно проводить двумя различными способами: методом пипетирования и методом отдельных навесок.
1. Метод пипетирования: Навеску анализируемого вещества растворяют в мерной колбе, разбавляют водой до метки и тщательно перемешивают раствор. Пипеткой отбирают отдельные порции (аликвоты), и титруют их.
2. Метод отдельных навесок: Берут отдельные навески анализируемого вещества, растворяют каждую из них в произвольном объёме воды и целиком титруют получаемые при этом растворы.
Метод отдельных навесок, при котором объём измеряют только один раз (бюреткой) выдаёт более точные, воспроизводимые результаты, чем метод пипетирования, при котором объём измеряют три раза (мерной колбой, пипеткой и бюреткой). Однако метод пипетирования требует меньше времени.
По способу титрования различают следующие методы: прямое, обратное и по методу замещения.
Прямое титрование
Титрант (Т) непосредственно добавляют к раствору титруемого вещества.
Пример: Для определения миллиграмового содержания NaOH в контрольном объёме методом пипетирования поступают следующим образом:
а) готовят титрованный раствор HCl;
б) в х. ч. мерную колбу переносят навеску щёлочи или приливают контрольный объём раствора щёлочи из бюретки, прибавляют дистиллированную воду до метки по нижнему мениску, закрывают пробкой и тщательно перемешивают;
в) в две х. ч. колбы для титрования приливают пипеткой (учитывая все правила) аликвоты контрольного раствора щёлочи, добавляют по одной капле индикатора (метилового оранжевого);
г) бюретку заполняют (по всем правилам) титрованным (рабочим) раствором HCl;
д) титруют кислотой щёлочь до перехода жёлтой окраски индикатора в оранжево – розовую от одной капли HCl;
е) Рассчитывают среднеарифметический объём и далее производят расчёты. Объёмы параллельных титрований (V1, V11) не должны отличаться друг от друга более чем на 0,2 мл.
Обратное титрование
(титрование по остатку)
Этот метод применяют, когда нет подходящего индикатора, или когда основная реакция протекает медленно, наблюдаются побочные эффекты при работе с неустойчивыми веществами, или невозможно зафиксировать ТЭ.
В этом случае к определяемому веществу приливают точно измеренный избыточный объем промежуточного вещества (титрант – Т1), доводят реакцию до конца, а затем находят количество непрореагировавшего титранта Т1, титрованием его реагентом (рабочим раствором Т2) с концентрацией С2 (1/z).
На определяемое вещество затрачивается количество титранта Т1 равное разности Ст1·Vт1 - Ст2·Vт2.
Например, для определения СаСО3:
а) навеску вещества обрабатывают избытком титрованного раствора соляной кислоты (промежуточное вещество Т1), доводят реакцию до конца
СаСО3 + 2HCl = СaCl2 + CO2 + H2O + (HCl)
избыток остаток
б) оставшуюся после реакции HCl титруют раствором NaOH (Т2) и тем самым определяют количество HCl, не вошедшее в реакцию с СаСО3 (или V1HCl (Т2)).
в) если концентрация Т1 неизвестна, то проводят контрольное титрование, т. е. определяют объём Т2 пошедший на титрование VHCl, введённого в реакцию с СаСО3;
г) затем находят V211NaOH (Т2) пошедший на титрование HCl, вошедшего в реакцию с СаСО3:
VT211 – VT21 = V2111Т2
Рассчитывают объём промежуточного вещества, вошедшего в реакцию с определяемым веществом;
д) Далее рассчитывают, г:
CаСО3 = (V2111Т2·С(1/z2T2)·М(1/z)СаСО3)/1000
Метод замещения
Этот метод применяют тогда, когда трудно определить точку эквивалентности, например, при работе с неустойчивыми веществами.
Например, при определении Сr2+, который легко окисляется кислородом воздуха поступают следующим образом: к определённому объёму соли хрома (II) прибавляют избыток титрованного раствора соли железа (III). В результате реакции:
Cr2+ + Fe3+ → Cr3+ + Fe2+
образуется количество Fe2+, эквивалентное взятому Cr2+, а далее Fe2+ оттитровывают в кислой среде рабочим раствором перманганата калия и определяют количество Cr2+.
Формулы для расчетов
Единицы количества вещества.
Один моль – единица количества вещества. Это такое количество вещества, которое содержит столько условных частиц, сколько атомов содержится в 0,012 кг углерода – 12, т.е. 6,02045·1023. Условной частицей может быть молекула, ион, электрон, группа частиц (радикал, функциональная группа, часть молекулы). Для обозначения количества молей вещества используется символ «n».
Молярная масса имеет размерность: г/моль.
*Например: n(1/5 КMnO4 или n(e)=1 моль=6,02045·1023 электронов.
Молярная масса (М) – это масса одного моля вещества. Если имеется вещество с массой m, то
М=m/n
Численно молярная масса равна относительной молекулярной массе.
Относительная молярная масса Mr – безразмерная величина, её вычисляют по таблицам атомных масс элементов.
Молярный объём Vo – это объём одного моля вещества при нормальных условиях (Р=101,3 кПа, Т=298 К).
Vo используют при расчётах с газами.
Vo = 22,4 л·моль-1.
Молярная концентрация – отношение числа молей растворённого вещества к объёму раствора. Молярную концентрацию выражают в моль·дм-3 или моль·л-1 (моль растворённого вещества в литре раствора сокращённо обозначают М).
*Например: n(1/5 KMnO4)=0,05 моль=6,02045∙1023∙0,05 условных частиц 1/5 KMnO4 или n(ē)=1 моль=6,02045·1023 электронов.
В объемных методах количественного анализа концентрацию удобно выражать в единицах нормальности, титра и титра по определяемому веществу.
Нормальность C(I/ZA) – число молей эквивалентов растворенного вещества А в одном литре раствора (моль/л).
Титр [Т(А)] – масса растворенного вещества А в граммах в одном миллилитре раствора этого вещества (г/мл).
Титр по определяемому веществу В – ТА/В, показывает, сколько граммов вещества В можно оттитровать одним миллилитром рабочего раствора вещества А.
Массу растворенного вещества А в граммах (m(А)) можно выразить следующим образом:
m(A)=(C(1/Z·A)·V(A)·M(1/Z·A))/1000=Т(А)·V(A)=(C(A)·V(A)·M(A))/1000= =(ω(A)·V(A)·ρ)/100=(C1/Z2B)·(VB)·M(1/Z1A)/1000,
где ω(А)-процентная концентрация раствора вещества А;
ρ – плотность раствора вещества А, г/мл;
С(А) – молярная концентрация раствора, моль/л.
Для перевода одних способов выражения концентраций растворов в другие можно пользоваться следующими формулами:
1) С(А)=(ω·ρ·10)/МА;
2) С(1/Z·A)=ω(A)ρ·10)/M(1/ZA);
3) Т(A)=C(1/ZA)·M(1/ZA)/1000;
4) Т(A/B)=Т(А)·М(1/Z2·B)/M(1/Z1·A)=C(1/Z1·A)·M(1/Z2·B)/1000;
5) C(1/Z·A)=Z·C(A).
Лабораторная работа № 1
Лабораторная работа № 2
Определение миллиграммового содержания NaOH и Na2CO3
При совместном присутствии
I. Теоретическое обоснование работы
Это определение основывается на методе фиксирования двух точек эквивалентностина кривой титрования.
Вследствие поглощения углекислого газа из воздуха раствор едкого натра всегда содержит примесь соды Na2CO3. На практике очень часто нужно знать содержание NaOH и Na2CO3 в растворе.
При титровании кислотой Na2CO3 сначала превращается в NaНCO3, а затем - в Н2CO3. На кривой титрования образуется две точки эквивалентности. Одна из них соответствует образованию NaНCO3 (рН = (рК1 + рК2)/2 = 8,34), другая - Н2CO3 (рН = 4). Вследствие этого раствор соли Na2CO3 различно титруется с фенолфталеином и метиловым оранжевым. Интервал перехода фенолфталеина находится в пределах рН = 8 - 10. Для рН ≤ 8 наблюдается окраска кислотной формы индикатора - бесцветная, а для рН ≥ 10 наблюдается окраска щелочной формы - малиновая. В интервале от рН = 10 до рН = 8 малиновая окраска постепенно изменяется до бледно-розовой. Значит с фенолфталеином титрование заканчивается в тот момент, когда весь Na2CO3 превратится в NaНCO3:
СО32- + Н+ → НСО3- (I)
Когда же Na2CO3 титруется с метиловым оранжевым, то порозове-ние индикатора наблюдается при рН = 4, когда вся соль оттитрована полностью до Н2CO3:
СО32- + 2Н+ → Н2СО3 (2)
Из сравнения приведенных уравнений (1) и (2) видно, что при титровании Na2CO3 с фенолфталеином на один моль соли затрачивается один моль соляной кислоты, а с метиловым оранжевым - два моля. Раствор NaOH титруется одинаково и с метиловым оранжевым и с фенолфталеином. Таким образом,с фенолфталеином оттитровывается ½Na2CO3 и вся щелочь, а после добавления метилового оранжевого оттитровывается вторая половина Na2CO3 (рисунок).
| NaOH | Na2CO3 | |
    | ||
| фенолфталеин | метилоранж | |
    | ||
Используя результаты титрования с двумя индикаторами, вычисляют содержание NаОН и Na2CO3, когда они находятся в одном растворе. Так как отношение К1 : К2 для H2CO3 примерно равно 104, то скачок рН около точки эквивалентности, соответствующей образованию NaHCO3, невелик, поэтому это определение не слишком точное. Точность определения понижается также из-за поглощения СО2 из воздуха или из воды, которой разбавляется раствор, когда часть NaOH превращается в Na2CO3.
Внимание! Учитывая вышеcказанное, при проведении анализа следует соблюдать следующие условия:
а) получив контрольную задачу, раствор закрыть пробкой;
б) тотчас же титровать взятый объем раствора;
в) в конце титрования с фенолфталеином прибавлять кислоту медленно, чтобы предотвратить образование вместо NaHCO3 свободной H2CO3;
г) избегать сильного перемешивания раствора, способствующего поглощению СО2 из воздуха.
2. Техника безопасности
При попадании раствора щелочи на кожу нужно промыть пораженное место большим количеством воды, а затем слабым раствором уксусной кислоты.
3. План работы
3.1. Заполнить бюретку титрованным раствором соляной кислоты.
3.2. В химически чистую мерную колбу на 100,0 мл получить контрольный объем смеси NаОН и Na2CO3; довести объем раствора дистиллированной водой до метки по нижнему мениску, закрыть колбу пробкой и перемешать раствор (пробку придерживать пальцем).
3.3. Внимание! Пипетку ополоснуть дважды раствором, который приготовили.
В две колбы для титрования пипеткой на 10,0; 15,0 или 20,0 мл прилить аликвоту контрольной задачи и закрыть пробками.
3.4. В первую колбу прилить 8-9 капель фенолфталеина (цвет раствора в колбе становится ярко-малиновым).
3.5. Раствор в первой колбе титровать соляной кислотой до тех пор, пока цвет раствора в колбе не станет бледно-розовым от одной капли HCI (титрование проводить медленно, соляную кислоту приливать по каплям, чтобы избежать образования H2CO3.
3.6. Записать по бюретке объем кислоты, пошедший на титрование 1/2 Na2CO3 и всей щелочи (V1).
3.7. Затем к этому оттитрованному раствору прилить одну каплю метилового оранжевого (при этом раствор в колбе окрасится в желтый цвет) и, не доливая раствор в бюретку до "0", продолжить титрование до неисчезающей оранжевой окраски раствора.
3.8. Записать объем соляной кислоты по бюретке от нулевой метки, пошедший на титрование всего количества соды и щелочи (V2).
3.9. Определение в том же порядке повторить и с контрольным раствором во второй колбе. Записать объемы кислоты V1 и V2.
3.10. Рассчитать массу (мг) соды и щелочи следующим образом:
Из данных титрования по двум колбам найти среднее арифметическое (V1сред.) между V1 и V11, а также V2сред. между V2 и V21.
Рассчитать объем соляной кислоты (V3), пошедший на титрование ½ количества соды V3 = V2сред. – V1сред.
Рассчитать объем кислоты V4, пошедшей на титрование всей соды:
V4 = 2V3
Рассчитать объем кислоты V5, пошедшей на титрование щелочи:
V5= V2сред. - V4
Рассчитать массу соды в мг в объеме мерной колбы по формуле:
m (Na2CO3) = (V4·C(HCl)·M(1/2 Na2CO3)·Vм.к.)/Vпип.
Рассчитать массу щелочи в мг в объеме мерной колбы:
m (NaOH) = (V5·C(HCl)·M(NaOH)·Vм.к.)/ Vпип.
4. Контрольные вопросы.
1. Контрольный объем щелочи оставили на некоторое время открытым. Как это скажется на результате количественного определения щелочи?
2. Увеличится или уменьшится масса (мг) Na2CO3 при совместном присутствии со щелочью, если титровать контрольный объем кислотой при сильном перемешивании?
3. Как оттитровать К2CO3 и КНCO3 с метиловым оранжевым и с фенол-фталеином? Можно ли в присутствии этих индикаторов определить содержание карбоната и бикарбоната, если они присутствуют совместно?
4. Почему при приготовлении рабочего раствора щелочи его очищают от примеси карбоната? Нужно ли это делать, если данным раствором щелочи предполагают титровать только сильные кислоты?
5. Написать формулу для расчета титра раствора NаОН по H3PO4 при титровании с фенолфталеином.
6. Какие методики - прямое или обратное кислотно-основное титрование - используются при определении содержания Na2CO3 и СаСО3?
7. Раствор, в котором может находиться одно из веществ NаОН, NаНСО3, Na2CO3 - или одна из смесей (NаОН + Na2CO3), (NaHCO3+ Na2CO3), титруется раствором HCl с фенолфталеином и метиловым оранжевым, применяемыми последовательно. Какое вещество или какая смесь титруется, если объем израсходованной кислоты составляет :
| Вариант | ||||||||||
| HCl (ф-ф) | - | - | ||||||||
| HCl (м-о) | - |
Лабораторная работа № 3
И примесей в пищевой соде
I. План работы
1.1. Заполнить бюретку титрованным раствором соляной кислоты.
1.2. Взять навеску исследуемой пищевой соды m (навески) около 1 г (взвесить точно на аналитических весах), растворить в мерной колбе на 100,0 мл, довести до метки дистиллированной водой, перемешать .
1.3. Взять пипеткой на 10,0, 15,0 или 20,0 мл (предварительно ополоснуть ее этим раствором) аликвоту исследуемого раствора в две колбы для титрования и закрыть их пробками.
1.4. В первую из них прилить 8÷10 капель фенолфталеина (цвет раствора - малиновый).
1.5. Сразу же титровать раствор по каплям соляной кислотой до слабо-розовой окраски (рН = 8,5).
1.6. Замерить по бюретке объем соляной кислоты V1, пошедшей на титрование ½ Na2CO3.
1.7. Рассчитать объем соляной кислоты, пошедшей на титрование всего количества карбоната натрия; он равен 2·V1.
1.8. В эту же колбу (первую) прилить 1-2 капли метилового оранжевого (цвет раствора в колбе станет желтым) и продолжать титровать раствор до оранжевого цвета.
1.9. Замерить объем соляной кислоты по бюретке, пошедшей на титрование Na2CO3 и NaHCO3 (V2).
1.10. Рассчитать объем соляной кислоты, пошедшей на титрование NaНСО3 V3 в мл:
V3 = V2 – 2V1
1.11. Повторить определение в том же порядке и с контрольным раствором во второй колбе.
1.12. Рассчитать среднее арифметическое из двух титрований: V1сред. и V2сред.
| ½ Na2CO3 | ½ Na2CO3 + NaНCO3 |
| фенолфталеин | метилоранж |
  V1 V1 | |
  V2 V2 |
1.13. Рассчитать процентное содержание Na2CO3 в данной навеске по формуле:
ω(Na2CO3)% = (2· V1·С(HCl)·M(½ Na2CO3)·Vм.к.·100)/(mнавески·1000·Vпип.),
где M(½ Na2CO3) – молярная масса эквивалента Na2CO3;
1.14. Рассчитать процентное содержание NаНСО3 в данной навеске:
ω(NaНCO3)% = (V3·С(HCl)·M(NaHCO3)·Vм.к.·100)/(mнавески·1000·Vпип.)
1.15. Рассчитать процентное одержание примесей в соде:
ω(примесей)% = 100 – (ω(Na2CO3) + ω(NaНCO3))
Лабораторная работа № 4
Лабораторная работа № 5
Пример: Вычислить концентрации ионов водорода и гидроксид-
иона, если рН = 9,5.
Решение: рН = 9,5; 9,5 = - lg[Н+]; или lg[Н+] = -9,5: превращаем мантиссу логарифма в положительную величину, а характеристику оставляем со знаком минус: -9,5 = 10,5. Находим антилогарифм 0,5 = 3; следовательно концентрация [H+] = 3 * 10 –10 моль/л;
[OH-] = 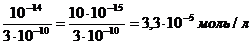
Ответ: [H+] = 3 * 10-10 моль/л; [OH-] = 3,3 * 10 –5 моль/л.
III Вычислить рН и рОН растворов, если:
1) См(СH3COOH) = 5×10-1 моль/л;
2) См(HIO3) = 2×10-2 моль/л;
3) См(NH4OH) = 5×10-3 моль/л;
4) См(HCOOH) = 2×10-3 моль/л;
5) См(HCN) = 1×10-2 моль/л;
6) См(H2SO3) = 1×10-5 моль/л;
7) См(H2CO3) = 1×10-5 моль/л;
8) См(HCOOH) = 2 моль/л;
9) См(CH3COOH) = 2 моль/л;
10) См(NH4OH) = 2×10-1 моль/л;
11) См(HF) = 2×10-1 моль/л;
12) См(HNO2) = 1×10-3 моль/л;
13) См(H2S) = 2×10-3 моль/л;
14) См(HNO2) = 5×10-2 моль/л;
15) См(H2C2O4) = 2×10-1 моль/л;
Пример: Вычислить рН и рОН раствора слабой кислоты
Пример: Вычислить рН и рОН раствора, если смешали 20,0 мл
Пример: Вычислить рН и рОН раствора, если смешали 15 мл
0,1 н раствора НСl и 20 мл. 0,1 н. NH4ОН.
Решение: так как слабое основание взято в избытке, то в растворе в результате образуется щелочная буферная смесь
HCl + NH4ОН ® NH4Cl+ Н2О + (NH4ОН)
0,1*15 0,1*20 0,1*15 избыток
рН этой смеси расчитывается по формуле:
рН = 14 - рК NH4ОН + lg(Cосн/Ссоли)
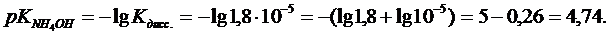
Так как под логарифмом стоит отношение концентраций, то вместо этих концентраций логично поставить объемы.
рН = 14 - 4,74 + lg(5/15) = 9,26 + lg3,3*10-1 = 9,26 - 0,48 = 8,78,
где lg3,3*10-1 = (lg3,3 + lg10-1) = -1 + 0,52 = - 0,48
рОН = 14 - 8,78 = 5,22
Ответ: рН = 8,78; рОН = 5,22
Пример 1: Выбрать индикатор для титрования 0,01 н. раствора
NaОН 0,01 М раствором HСl.
Решение: рабочий раствор - сильная кислота и определяемое вещество - сильное основание.
Для выбора индикатора нужно на кривой титрования найти рН двух точек - начала скачка и конца скачка.
а) начало скачка на кривой титрования - недотитровано 0,1% от объема титруемого раствора NaОН. Так как объем не задан, то берем 100 мл. В начале недотитрована щелочь, поэтому находим концентрацию [ОН-]:
[ОН-] = ( 0,01·100 - 0,01· 99,9)/ 100 = 1*10-5 моль
( принебрегаем изменением объема смеси )
рОН = 5; рН = 14 - 5 = 9
б) конец скачка - раствор перетритирован на 0,1% от объёма раствора NaOH, в избытке сильная кислота, находим концентрацию ионов водорода:
[Н+] = (0,01*100,1 - 0,01*100) / 100 =1*10-5 моль/л.
рН =5
Величина скачка от 9 до 5. В этом интервале происходит изменение окраски индикаторов: фенол-фталеина (рТ = 8), метилового красного (рТ=5,5, лакмуса (рТ=7). Каждый индикатор можно использовать для данного титрования.
Пример 2: Выбрать индикатор для титрования 0,1 М раствора
NH4ОН 0,1 м. раствором НCl.
Решение: рабочий раствор - сильная кислота, определяемое вещество - слабое основание.
а) Начало скачка на кривой титрования - в избытке раствор аммиака
NH4ОН + НCl = NH4Cl+ H2О + (NH4ОН)
100 мл. 99,9 мл. 99,9 мл. 0,1 мл. (избыток)
образуется аммиачная буферная смесь
рН = 14 - рК NH4ОН + lg(Сосн/Ссоли)
рН = 14 - 4,74 + lg(0,1/99,9) = 9,26 - 3 = 6,26
б) конец скачка - в избытке сильная кислота. Находим концентрацию ионов водорода:[Н+] = (0,1·100,1 - 0,1 ·100)/100 = 10-4 моль/л, рН = 4
Интервал скачка рН от 6,26 до 4.
4. В этом интервале происходит изменение окраски индикаторов метилового красного (рТ = 5,5) и метилового оранжевого (рТ = 4).
VII Вычислить эквивалентную массу вещества (А), которое
Титруется рабочим раствором (Б) в присутствии
индикатора (В):
1) (А) Na3PO4 ; (Б) HCl; (В) Метиловый оранжевый;
2) (А) Na3PO4; (Б) HCl; (В) Фенолфталеин;
3) (А) H3PO4; (Б) NaOH; (В) Метиловый оранжевый;
4) (А) H3PO4; (Б) NaOH; (В) Фенолфталеин;
5) (А) Na2CO3 ; (Б) HCl; (В) Метиловый оранжевый;
6) (А) Na2CO3 ; (Б) HCl; (В) Фенолфталеин;
7) (A) Na2B4O7; (Б) HCl ; (В) Метиловый оранжевый;
8) (А) К2CO3; (Б) HCl; (В) Фенолфталеин;
9) (А) К2CO3; (Б) HNO3; (В) Метиловый оранжевый;
10) (А) К2CO3; (Б) HNO3; (В) Фенолфталеин;
11) (А) Na3PO4 ; (Б) H2SO4 ; (В) Метиловый оранжевый;
12) (А) K3PO4; (Б) H2SO4 ; (В) Фенолфталеин;
13) (A) K3PO4; (Б) HNO3; (В) Метиловый оранжевый;
14) (А) Na2B4O7 * 10 H2O ; (Б) HNO3; (В) Фенолфталеин;
15) (А) Na2CO3 ; (Б) H2SO4 ; (В) Фенолфталеин;
Пример: Вычислить эквивалентную массу кислоты Н3РО4, если
Раствора HCl?
Решение: Определение ведётся методом отдельных навесок. Процентное содержание чистой буры определяется по формуле:
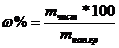
Находим сначала массу чистой буры (mчист.) по результатам титрования:
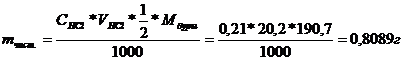
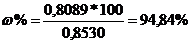 Ответ: 94,84 %.
Ответ: 94,84 %.
Содержит сталь?
Решение: При титровании с фенолфталеином вольфрамовая кислота титруется как одноосновная до кислой соли:
H2WO4 + NaOH = NaHWO4 + H2O
ZH2WO4 = 1; Эквивалентная масса H2WO4 равна М(H2WO4).
Эквивалентная масса вольфрама равна его атомной массе (183,85 г/моль). Находим массу чистого вольфрама:
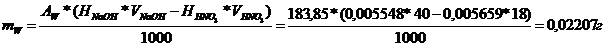
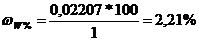
Ответ: 2,21%.
Метод перманганатометрии
В данном методе рабочим раствором является перманганат калия KMnO4. Ион перманганата (MnO4-) окисляет в кислой, щелочной и в нейтральной средах. В объемном анализе наибольшее применение имеет окисление в кислой среде, когда перманганат-ион восстанавливается до иона Mn2+ по уравнению:
MnO4- + 8H+ + 5e = Mn2+ + 4H2O
Молярная масса перманганата калия М(KMnO4) = 158,03 г/моль, а молярная масса эквивалента М(1/5KMnO4) = 1/5·М(KMnO4) = 31,61 г/моль. Окислительно-восстановительный потенциал данной системы находится по уравнению:
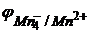 = 1,52 +0,059/5
= 1,52 +0,059/5 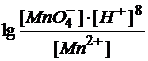
Видно, что величина потенциала зависит не только от концентраций ионов MnO4- и Mn2+, но и сильно зависит от концентрации ионов водорода.
Молярная масса эквивалента перманганата калия в нейтральной или слабо щелочной средах находится на основании уравнения:
MnO4- + 3H2О +3e = MnО(ОН)2 + 4OН- (5)
Т.е. MnO4- восстанавливается до MnO2, точнее до ее гидрата MnO(ОН)2, выпадающего в виде бурого осадка. Следовательно, молярная масса эквивалента KMnO4 равна 1/3·М(KMnO4) = 52,68 г/моль. Стандартный потенциал пары MnO4-/Mn2+ (1,52 В) гораздо выше стандартного потенциала пары MnO4-/MnО2 (0,59 В), поэтому окислительная сила перманганата в кислой среде выше, чем в нейтральной.
Титрование перманганатом может осуществляться прямым и косвенным способом. Прямым методом титрования определяют многие восстановители, которые легко и без потерь окисляются перманганатом. Обратное титрование обычно применяют для анализа восстановителей, которые взаимодействуют с перманганатом медленно. Для анализа окислителей методом перманганатометрии их предварительно восстанавливают до соединений низших степеней окисления.
Метод перманганатометрии имеет следующие достоинства:
1. Так как раствор перманганата окрашен в красно-фиолетовый цвет, то титрование можно проводить без индикатора. Точку эквивалентности фиксируют по появлению розовой окраски титруемого раствора при определении прямым методом или по исчезновению розовой окраски при титровании обратным методом.
2. Титрование перманганатом осуществляется в кислой или в щелочной средах.
3. Имея высокий окислительно-восстановительный потенциал, перманганат может окислять многие восстановители.
Недостатки метода:
1. Перманганат калия трудно получить в химически чистом состоянии, поэтому невозможно приготовить его раствор точной нормальности по навеске. Нормальность перманганата устанавливают по исходным веществам или готовят его раствор из фиксанала.
2. Растворы перманганата неустойчивы, со временем меняют свою нормальность в результате разложения KMnO4.
3. Титрование перманганатом, как правило, не рекомендуется проводить в присутствии хлорид-ионов, окисляющихся им до хлора.
4. Состояние динамических равновесий, устанавливающихся в процессе титрования перманганатом, зависит от различных факторов, поэтому определение необходимо проводить при строго определенных условиях, рекомендуемых методикой анализа.
Приготовление и хранение раствора KMnO4
Обычно при титровании перманганатом применяют 0,05н его раствор. Для приготовления 1 л 0,05н раствора перманганата калия, предназначенного для титрования в кислой среде, навеска рассчитывается по формуле:
m(KMnO4) = 1/5M(KMnO4)·0,05 = 1,5803 г
Если рабочий раствор KMnO4 предназначается для слабо щелочных или нейтральных растворов, то навеска его рассчитывается по формуле:
m(KMnO4) = 1/3M(KMnO4)·0,05 = 2,64 г
Навеску перманганата взвешивают на технических весах в стеклянном бюксе, растворяют в 1 л дистилированной воды, нагревают до кипения, охлаждают и оставляют в темной колбе с притертой пробкой до следующего занятия. Если в колбе при хранении образуется осадок MnO2, то раствор осторожно сливают с осадка или фильтруют через стеклополотно.
Точную нормальность раствора перманганата устанавливают по одному из исходных веществ: H2C2O4·2H2O; Na2C2O4; As2O3; K4[Fe(CN)6]·3H2O. Наиболее удобным является щавелевокислый натрий (оксалат натрия) (Na2C2O4). Очистка его легко достигается перекристаллизацией.
Техника безопасности
1. При выполнении работ, связанных с применением серной кислоты, соблюдать обычные меры предосторожности при работах с кислотами:
а) при попадании кислоты на кожу быстро смыть проточ
