Тема 1. Классы неорганических соединений.
Демонстрационные тесты
Д1. Формулы нерастворимых основания, соли и кислоты соответственно указаны в ряду:
| 1) Mg(OH)2, HCl, Ca(NO3)2 | 3) Fe(OH)2, BaSO4, H2SiO3 |
| 2) Cu(OH)2, H2SiO3, FeS | 4) NaOH, Na2SO4, H2SO3 |
Ответ: 3
Д2. Сокращенное ионное уравнение Al(OH)3 + 3H+ = Al3+ + 3H2O
соответствует взаимодействию
| а) Al(OH)3 и H2CO3 | в) Al(OH)3 и H2S |
| б) Al(OH)3 и CH3COOH | г) Al(OH)3 и HNO3 |
Ответ: 4
Д3.Система – это группа тел, которые
а) находятся в окружающей среде и отделены от окружающей среды поверхностью
б) взаимодействуют друг с другом и изменяются в результате взаимодействия с окружающей средой
в) находятся во взаимодействии и мысленно или фактически обособлены от окружающей среды
г) находятся во взаимодействии, обособлены от окружающей среды и совершают работу против внешних сил
Ответ: в
Д4. Изохорный процесс протекает при постоянном
| а) давлении | в) объеме |
| б) количестве вещества | г) температуре |
Д5. Мгновенную скорость гомогенной реакции вычисляют по формуле
а) 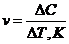 | б) 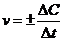 | в) 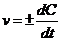 | г) 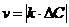 |
Ответ: в
Д6. Скорость прямой реакции CO2(Г) + СТВ " 2CO(Г) ... , если увеличить давление в 4 раза.
| а) увеличится в 4 раза | в) увеличится в 2 раза |
| б) увеличится в 16 раз | г) уменьшится в 2 раза |
Ответ: а
Д7. В какой системе увеличение концентрации водорода смещает химическое равновесие влево?
| а) C(ТВ) + 2H2(Г) D CH4(Г) | в) 2H2(Г) + O2(Г) D 2H2O(Г) |
| б) 2NH3(Г) D N2(Г) + 3H2(Г) | г) FeO(ТВ) + H2(Г) D Fe(ТВ) + H2O(Г) |
ответ: б
Д8.В какой системе при повышении давления химическое равновесие сместится в сторону исходных веществ?
а) N2(Г) + 3H2(Г) D 2NH3(Г) + Q
б) C(ТВ) + 2H2(Г) D CH4(Г)
в) CO2(Г) + H2(Г) D CO(Г) + H2O(Г) + Q
г) N2O4(Г) D 2NO2(Г) – Q
Ответ: г
Д9. Какая электронная конфигурация внешнего энергетического уровня соответствует атому элемента VА группы?
| а) 3s23p6 | б) 2s22p5 | в) 4s13d5 | г) 4s24p3 |
Ответ 4
Д10. В каком ряду химические элементы расположены в порядке возрастания их атомного радиуса?
| а) Li, Be, B, C | в) Mg, Si, Cl, Ar |
| б) Sb, As, P, N | г) O, S, Se, Te |
Ответ: 4
Д11. Кислотные свойства водородных соединений усиливаются в ряду:
| 1) HI – HBr – HCl – HF | 3) HF – NH3 – H2O – CH4 |
| 2) HCl – H2S – PH3 – SiH4 | 4) H2O – H2S – H2Se – H2Te |
Ответ: 4
Д12. Вещества с ковалентной полярной связью находятся в ряду:
| а) CO, HF, N2 | в) NH3, SF6, H2S |
| б) KF, HF, CF4 | г) SO2, NO2, Cl2 |
Ответ: 3
Д13.Низшую степень окисления хром проявляет в соединении:
| а) К2Cr2O7 | в) Cr2O3 |
| б) Na[Cr(H2O)2F4] | г) Cr(OH)2 |
Ответ: 4
А14. Оксид серы (IV) является восстановителем в реакции
| 1) SO2 + CaO = CaSO3 | 3) SO2 + 2H2S = 3S + 2H2O |
| 2) 2SO2 + O2 = 2SO3 | 4) SO2 + 2NaOH = Na2SO3 + H2O |
Ответ: 2
Д15. Среда раствора карбоната лития
| а) щелочная | в) слабокислая |
| б) кислая | г) нейтральная |

Схема 1. Общая схема гидролиза солей
Ответ: 1
Д16. Установите соответствие между формулой соли и типом гидролиза этой соли.
| ФОРМУЛА СОЛИ | ТИП ГИДРОЛИЗА |
| а) (NH4)2CO3 | 1) по катиону |
| б) NH4Cl | 2) по аниону |
| в) Na2CO3 | 3) по катиону и аниону |
| г) NaNO2 |
Ответ: 3122
Д17. Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора.
| ФОРМУЛА СОЛИ | ПРОДУКТ НА АНОДЕ |
| а) Al(NO3)3 | 1) H2 |
| б) LiBr | 2) O2 |
| в) Ca(NO3)2 | 3) NO2 |
| г) KCl | 4) NO |
| 5) Cl2 | |
| 6) Br2 |
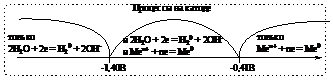
Схема 2. Катодный процесс при электролизе и положение металла в ряду активности.
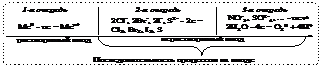
Схема 3. Последовательность процессов окисления на аноде
Ответ: 2625
Д18. Какие из металлов – алюминий, никель, серебро, магний – можно использовать для защиты железа от атмосферной коррозии? Приведите электронные и молекулярные уравнения протекающих процессов.
| а) алюминий | б) серебро | в) магний | г) никель |
Ответ: а, в.
Д19. Анодный процесс, протекающий при коррозии железных пластин, скрепленных алюминиевыми заклепками, во влажном воздухе, описывается уравнением
| а) Al0 – 3e = Al3+ | г) Fe0 – 2e = Fe2+ |
| б) O2 + 2H2O + 4e = 4OH– | д) Fe2+ + 2e = Fe0 |
| в) Al3+ + 3e = Al0 | е) O2 + 4e = 2O2– |
Ответ: а
Тема 5. Химическая связь.
5-1. Атомы в молекуле удерживают силы:
| а) гравитационные | в) магнитные |
| б) электрические | г) ядерные |
5-2. Ионная связь осуществляется в молекуле
| а) O2 | б) H2O | в) Li2 | г) NaCl |
5-3. Ковалентная неполярная связь осуществляется в молекуле
| а) H2 | б) H2S | в) Na2 | г) KCl |
5-4. Ковалентная полярная связь осуществляется в молекуле
| а) CaCl2 | б) O2 | в) Li2 | г) HCl |
5-5. Характеристики химической связи
| а) энергия ионизации | в) валентный угол | д) сродство к электрону |
| б) длина связи | г) энергия связи |
5-6. Металлические связи образуются в твердых веществах между
| а) атомами металлов | в) атомами металлов и неметаллов |
| б) атомами неметаллов | г) молекулами воды |
5-7. Вещество, имеющее высокую температуру плавления, блеск, ковкость, теплопроводность, электропроводность и пластичность, образовано связью
| а) ковалентной полярной | г) металлической |
| б) ковалентной неполярной | д) водородной |
| в) ионной |
5-8. Валентность – это
а) число неспаренных электронов в атоме
б) число электронов на внешнем электронном слое атома
в) число химических связей, образованных атомом
г) формальный заряд атома в молекуле
5-9. Ковалентные связи образуются между
| а) молекулами простых веществ | в) атомами металлов и неметаллов |
| б) атомами неметаллов | г) между молекулами воды |
5-10. Водородные связи образуются между
| а) атомами металлов | в) атомами металлов и неметаллов |
| б) атомами неметаллов | г) между молекулами воды |
5-11. Прочность химической связи зависит от
| а) длины связи | г) дипольного момента |
| б) кратности связи | д) насыщаемости связи |
| в) валентного угла |
5-12. Валентность атома по обменному механизму равна
| ¯ | | | ||||||
| s | p | d |
| а) 1 | б) 2 | в) 3 | г) 4 |
5-13. Наиболее короткой является связь
| а) K – Cl | б) K – Br | в) K – I | г) K – F |
5-14. Наиболее длинной является связь
| а) Na – Cl | б) Na – Br | в) K – I | г) Na – F |
5-15. Последовательность соединений по возрастанию энергии связи
| а) Na – I | б) Na – Br | в) Na – Cl | г) Na – F |
5-16. Гибридная орбиталь:
| а) |  | б) | 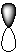 | в) | 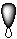 | г) | 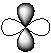 |
5-17. Ковалентная связь – это связь, которая возникает в результате электростатического притяжения между
а) общей электронной парой и положительно заряженными ядрами атомов
б) электронами и катионами, находящимися в узлах кристаллической решетки
в) атомом водорода и атомом сильно электроотрицательного элемента
г) катионом металла и анионом неметалла
5-18. Образование молекулы по обменному механизму показано на рисунке
| а) |  |
| б) | 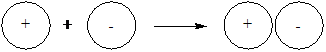 |
| в) | 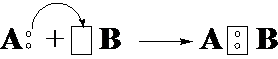 |
| г) | 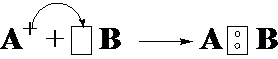 |
5-19. Образование молекулы по донорно-акцепторному механизму показано на рисунке
| а) |  |
| б) | 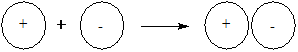 |
| в) | 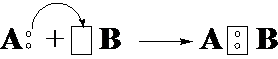 |
| г) | 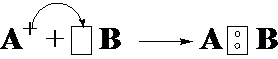 |
5-20. Последовательность возрастания энергии связи
| а) K – I | б) K – Br | в) K – Cl | г) K – F |
5-21. Атом будет проявлять
| ¯ | | | |
| s | p |
| а) донорные свойства | в) донорно-акцепторные свойства |
| б) акцепторные свойства | г) дипольные свойства |
5-22. Атом алюминия в возбужденном состоянии может проявлять
| а) донорно-акцепторные свойства | в) акцепторные свойства |
| б) донорные свойства | г) электроноакцепторные свойства |
5-23. Соответствие формулы соединения и вида химической связи:
| 1) | KCl | а) | ионная |
| 2) | H2 | б) | ковалентная неполярная |
| 3) | HCl | в) | ковалентная полярная |
| 4) | Zn | г) | металлическая |
| д) | водородная |
5-24. Донорно-акцепторная связь имеется в
| а) NH3 | б) NH4+. | в) CO2 | г) O2 |
5-25. Атом углерода в молекуле CH4 имеет гибридизацию
| а) sp | б) s2p | в) sp2 | г) sp3 |
5-26. Атом бериллия в молекуле BeCl2 имеет гибридизацию
| а) sp | б) sp2 | в) sp3 | г) s2p |
Тема 8. Дисперсные системы
8-1. Пенопласт – это дисперсная система с
а) твердой дисперсионной средой и газообразной дисперсной фазой
б) жидкой дисперсионной средой и газообразной дисперсной фазой
в) газообразной дисперсионной средой и твердой дисперсной фазой
г) твердой дисперсионной средой и твердой дисперсной фазой
8-2. Конденсационно-кристаллизационные структуры образуются
а) путем связывания частиц дисперсной фазы через прослойки воды
б) в результате химического взаимодействия между частицами дисперсной фазы
в) при осуществлении механических воздействий
г) в результате проявления эффекта Тиндаля
8-3. Основной фактор стабилизации концентрированных эмульсий
а) структурирование систем
б) существование двойного электрического слоя
в) образование адсорбционно-сольватного слоя на поверхности капель
г) добавление электролитов
8-4. Коагуляционные структуры образуются
г) в результате проявления эффекта Тиндаля
б) в результате химического взаимодействия между частицами дисперсной фазы
в) при осуществлении механических воздействий
г) путем связывания частиц дисперсной фазы через прослойки воды
8-5. В качестве пеногасителя используют
| а) изоамиловый спирт | в) крахмал |
| б) серную кислоту | г) сахар |
6) Связнодисперсные системы по видам взаимодействия между частицами подразделяются на
а) конденсационно-кристаллизационные и коагуляционные структуры
б) коагуляционные и кинетические структуры
в) гидрофильные и кинетические структуры
г) кинетические и конденсационно-кристаллизационные структуры
8-6. Структурообразование в дисперсной системе происходит в результате
г) осуществления механических воздействий
б) осуществления броуновского движения
в) изотермической перегонки
г) образования пространственной сетки из частиц дисперсной фазы
8-7. Установить соответствие между объектом и его определением.
| Понятие | Определение |
| 1. фаза | а) часть системы одного состава, одинаковых физических свойств |
| 2. дисперсионная среда | б) ограниченная от других частей поверхностью раздела |
| 3. дисперсная фаза | в) сплошная часть системы |
| г) раздробленная часть системы |
8-8. Установить соответствие между дисперсной системой и образующими её фазами.
| Дисперсная система | Фазы |
| 1. суспензии | а) т/ж |
| 2. эмульсии | б) ж/ж |
| 3. пены | в) г/ж |
8-9. Установите соответствие между веществом и дисперсной системой.
| Вещество | Дисперсная система |
| 1. молоко | а) эмульсия |
| 2. цементный раствор | б) суспензия |
| 3. табачный дым | в) аэрозоль |
8-10. Установите соответствие между веществом и его свойствами.
| Вещество | Свойства системы |
| 1. цементный раствор | а) тиксотропными свойствами обладает |
| 2. схватившийся цементный раствор | б) тиксотопными свойствами не обладает |
| 3. раствор желатины | |
| 4. раствор глины | |
| 5. раствор сахара |
8-11. Установите соответствие между веществом и дисперсной системой.
| Вещество | Дисперсная система |
| 1. млечный сок растений | а) эмульсия |
| 2. глиняный раствор | б) суспензия |
| 3. туман | в) аэрозоль |
| г) пена | |
| д) аэрозоль | |
| е) истинный раствор |
8-12.Установите соответствие между дисперсной системой и составляющими её фазами.
| Система | Описание фаз |
| 1. эмульсии | а) и дисперсионная среда, и дисперсная фаза являются жидкими |
| 2. суспензии | б) дисперсионная среда – жидкая, дисперсная фаза – твердая |
| 3. пены | в) дисперсионная среда – жидкая, дисперсная фаза – газообразная |
8-13. Установите соответствие между веществом и дисперсной системой.
| Вещество | Дисперсная система |
| 1. цементный порошок | а) аэрозоль |
| 2. цементный раствор | б) суспензия |
| 3. нефть | в) эмульсия |
Демонстрационные тесты
Д1. Формулы нерастворимых основания, соли и кислоты соответственно указаны в ряду:
| 1) Mg(OH)2, HCl, Ca(NO3)2 | 3) Fe(OH)2, BaSO4, H2SiO3 |
| 2) Cu(OH)2, H2SiO3, FeS | 4) NaOH, Na2SO4, H2SO3 |
Ответ: 3
Д2. Сокращенное ионное уравнение Al(OH)3 + 3H+ = Al3+ + 3H2O
соответствует взаимодействию
| а) Al(OH)3 и H2CO3 | в) Al(OH)3 и H2S |
| б) Al(OH)3 и CH3COOH | г) Al(OH)3 и HNO3 |
Ответ: 4
Д3.Система – это группа тел, которые
а) находятся в окружающей среде и отделены от окружающей среды поверхностью
б) взаимодействуют друг с другом и изменяются в результате взаимодействия с окружающей средой
в) находятся во взаимодействии и мысленно или фактически обособлены от окружающей среды
г) находятся во взаимодействии, обособлены от окружающей среды и совершают работу против внешних сил
Ответ: в
Д4. Изохорный процесс протекает при постоянном
| а) давлении | в) объеме |
| б) количестве вещества | г) температуре |
Д5. Мгновенную скорость гомогенной реакции вычисляют по формуле
а) 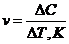 | б) 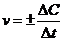 | в) 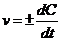 | г) 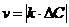 |
Ответ: в
Д6. Скорость прямой реакции CO2(Г) + СТВ " 2CO(Г) ... , если увеличить давление в 4 раза.
| а) увеличится в 4 раза | в) увеличится в 2 раза |
| б) увеличится в 16 раз | г) уменьшится в 2 раза |
Ответ: а
Д7. В какой системе увеличение концентрации водорода смещает химическое равновесие влево?
| а) C(ТВ) + 2H2(Г) D CH4(Г) | в) 2H2(Г) + O2(Г) D 2H2O(Г) |
| б) 2NH3(Г) D N2(Г) + 3H2(Г) | г) FeO(ТВ) + H2(Г) D Fe(ТВ) + H2O(Г) |
ответ: б
Д8.В какой системе при повышении давления химическое равновесие сместится в сторону исходных веществ?
а) N2(Г) + 3H2(Г) D 2NH3(Г) + Q
б) C(ТВ) + 2H2(Г) D CH4(Г)
в) CO2(Г) + H2(Г) D CO(Г) + H2O(Г) + Q
г) N2O4(Г) D 2NO2(Г) – Q
Ответ: г
Д9. Какая электронная конфигурация внешнего энергетического уровня соответствует атому элемента VА группы?
| а) 3s23p6 | б) 2s22p5 | в) 4s13d5 | г) 4s24p3 |
Ответ 4
Д10. В каком ряду химические элементы расположены в порядке возрастания их атомного радиуса?
| а) Li, Be, B, C | в) Mg, Si, Cl, Ar |
| б) Sb, As, P, N | г) O, S, Se, Te |
Ответ: 4
Д11. Кислотные свойства водородных соединений усиливаются в ряду:
| 1) HI – HBr – HCl – HF | 3) HF – NH3 – H2O – CH4 |
| 2) HCl – H2S – PH3 – SiH4 | 4) H2O – H2S – H2Se – H2Te |
Ответ: 4
Д12. Вещества с ковалентной полярной связью находятся в ряду:
| а) CO, HF, N2 | в) NH3, SF6, H2S |
| б) KF, HF, CF4 | г) SO2, NO2, Cl2 |
Ответ: 3
Д13.Низшую степень окисления хром проявляет в соединении:
| а) К2Cr2O7 | в) Cr2O3 |
| б) Na[Cr(H2O)2F4] | г) Cr(OH)2 |
Ответ: 4
А14. Оксид серы (IV) является восстановителем в реакции
| 1) SO2 + CaO = CaSO3 | 3) SO2 + 2H2S = 3S + 2H2O |
| 2) 2SO2 + O2 = 2SO3 | 4) SO2 + 2NaOH = Na2SO3 + H2O |
Ответ: 2
Д15. Среда раствора карбоната лития
| а) щелочная | в) слабокислая |
| б) кислая | г) нейтральная |

Схема 1. Общая схема гидролиза солей
Ответ: 1
Д16. Установите соответствие между формулой соли и типом гидролиза этой соли.
| ФОРМУЛА СОЛИ | ТИП ГИДРОЛИЗА |
| а) (NH4)2CO3 | 1) по катиону |
| б) NH4Cl | 2) по аниону |
| в) Na2CO3 | 3) по катиону и аниону |
| г) NaNO2 |
Ответ: 3122
Д17. Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора.
| ФОРМУЛА СОЛИ | ПРОДУКТ НА АНОДЕ |
| а) Al(NO3)3 | 1) H2 |
| б) LiBr | 2) O2 |
| в) Ca(NO3)2 | 3) NO2 |
| г) KCl | 4) NO |
| 5) Cl2 | |
| 6) Br2 |
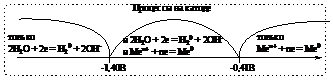
Схема 2. Катодный процесс при электролизе и положение металла в ряду активности.
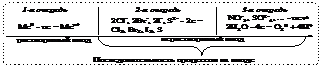
Схема 3. Последовательность процессов окисления на аноде
Ответ: 2625
Д18. Какие из металлов – алюминий, никель, серебро, магний – можно использовать для защиты железа от атмосферной коррозии? Приведите электронные и молекулярные уравнения протекающих процессов.
| а) алюминий | б) серебро | в) магний | г) никель |
Ответ: а, в.
Д19. Анодный процесс, протекающий при коррозии железных пластин, скрепленных алюминиевыми заклепками, во влажном воздухе, описывается уравнением
| а) Al0 – 3e = Al3+ | г) Fe0 – 2e = Fe2+ |
| б) O2 + 2H2O + 4e = 4OH– | д) Fe2+ + 2e = Fe0 |
| в) Al3+ + 3e = Al0 | е) O2 + 4e = 2O2– |
Ответ: а
Тема 1. Классы неорганических соединений.
1-1. Хлороводородная кислота
| а) HCl | б) HClO | в) HClO3 | г) HClO4 |
1-2. Серная кислота
| а) H2S | в) H2SO4 | д) H2S2O7 |
| б) H2SO3 | г) H2S2O3 |
1-3. Азотная кислота – вещество
| а) HN3 | б) NH3 | в) HNO2 | г) HNO3 |
1-4.Ортофосфорная кислота
| а) HPO3 | б) H3PO4 | в) H4P2O7 | г) H3PO3 |
1-5. Гидроксид натрия
| а) NaH | б) NaOH | в) NaHCO3 | г) Na2CO3 |
1-6. Сернистая кислота
| а) H2S | в) H2SO4 | д) H2S2O7 |
| б) H2SO3 | г) H2S2O3 |
1-7. Сероводородная кислота
| а) H2S | в) H2SO4 | д) H2S2O7 |
| б) H2SO3 | г) H2S2O3 |
1-8. Метафосфорная кислота
| а) HPO3 | б) H3PO4 | в) H4P2O7 | г) H3PO3 |
1-9. Двухосновными кислотами являются
| а) H2S2O7 | г) NaHCO3 | ж) HClO4 |
| б) NaOH | д) Cu(OH2 | з) HPO3 |
| в) K2CO3 | е) H2S | и) CuOHCl |
1-10. Бескислородными кислотами являются
| а) H2S2O7 | г) NaHCO3 | ж) HCl |
| б) NaOH | д) Cu(OH)2 | з) HPO3 |
| в) K2CO3 | е) H2S | и) CuOHCl |
1-11. Солями являются
| а) H2S2O7 | г) NaHCO3 | ж) HClO4 |
| б) NaOH | д) Cu(OH)2 | з) HPO3 |
| в) K2CO3 | е) H2S | и) CuOHCl |
1-12. Кислые соли –
| а) H2S2O7 | г) NaHCO3 | ж) HClO4 |
| б) NaOH | д) Cu(OH)2 | з) HPO3 |
| в) K2CO3 | е) Ca(HS)2 | и) CuOHCl |
1-13. Основные соли –
| а) Fe(OH)2NO3 | г) NaHCO3 | ж) HClO4 |
| б) NaOH | д) Cu(OH)2 | з) HPO3 |
| в) K2CO3 | е) Ca(HS)2 | и) CuOHCl |
1-14. Основания –
| а) Fe(OH)2NO3 | г) NaHCO3 | ж) Cu(OH)2 |
| б) NaOH | д) HClO4 | з) HPO3 |
| в) K2CO3 | е) Ca(HS)2 | и) CuOHCl |
1-15. Щелочи –
| а) Fe(OH)2NO3 | г) NaHCO3 | ж) Al(OH)3 |
| б) NaOH | д) Cu(OH)2 | з) HPO3 |
| в) KOH | е) Ba(OH)2 | и) CuOHCl |
1-16. Соответствие между названием вещества и его формулой
| 1) | Ортофосфорная кислота | а) | H3PO4 |
| 2) | Карбонат натрия | б) | Na2CO3 |
| 3) | Гидроксид железа (II) | в) | Fe(OH)2 |
| 4) | Гидрокарбонат натрия | г) | NaHCO3 |
| д) | HPO3 | ||
| е) | Fe(OH)3 |
1-17. Соответствие между формулой вещества и его названием:
| 1) | Na2SO4 | а) | сульфат натрия |
| 2) | H2SO4 | б) | серная кислота |
| 3) | NaHCO3 | в) | гидрокарбонат натрия |
| г) | карбонат натрия | ||
| д) | сернистая кислота |
1-18. Реакцией нейтрализации будет
а) Na2O + 2HNO3 " 2NaNO3 + H2O
б) NaOH + HNO3 " NaNO3 + H2O
в) Na2CO3 + HNO3 " 2NaNO3 + CO2# + H2O
г) Na2CO3 + Ca(NO3)2 " 2NaNO3 + CaCO3$
1-19. Формулы кислотных оксидов
| а) CaO | в) CO2 | д) Na2O |
| б) SiO2 | г) Fe2O3 | е) NO2 |
1-20. Щелочи –
| а) NaOH | в) LiOH | д) Ba(OH)2 |
| б) Ni(OH)2 | г) Fe(OH)2 | е) Co(OH)2 |
1-21. Бескислородные кислоты –
| а) HF | в) H3PO4 | д) HBr |
| б) H2SO4 | г) HCN | е) H3BO3 |
1-22. Амфотерными называются соединения, которые способны реагировать
| а) только с кислотами | в) и с кислотами, и со щелочами |
| б) только со щелочами | г) и с кислотами, и с гидроксидами |
1-23. Химические соединения NaNO3, KCl, CaCO3 относятся к
| а) основным оксидам | в) кислородосодержащим кислотам |
| б) средним солям | г) основаниям |
1-24. Соответствие оксидов и кислот:
| 1) | SO3 | а) | H2SO4 |
| 2) | P2O5 | б) | H3PO4 |
| 3) | CO2 | в) | H2CO3 |
| 4) | SO2 | г) | H2SO3 |
| д) | H2S2O3 |
1-25. Соответствие формул солей и названий:
| 1) | Na2CO3 | а) | карбонат натрия |
| 2) | KCl | б) | хлорид калия |
| 3) | LiNO3 | в) | нитрат лития |
| 4) | (NH4)2SO4 | г) | сульфат аммония |
| д) | сульфид аммония | ||
| е) | гидрокарбонат натрия |
1-26. Неэлектролитами являются
| а) SO3 | г) NaHCO3 | ж) HClO4 |
| б) NaOH | д) CuO | з) HPO3 |
| в) K2CO3 | е) Fe2O3 | и) CuOHCl |
1-27. Электролитами являются
| а) SO3 | г) NaHCO3 | ж) HClO4 |
| б) KOH | д) CuO | з) HPO3 |
| в) CO2 | е) Fe2O3 | и) N2 |
1-28. Уравнение полной диссоциации H3PO4
| а) H3PO4 D H+ + HPO4– | в) H3PO4 D 3H+ + PO43– |
| б) H3PO4 D 2H+ + HPO42– | г) H3PO4 D 3H+ + PO42– |
1-29. Уравнение реакции нейтрализации
а) 2NaOH + K2SO4 = Na2SO4 + 2KOH
б) CoCl2 + 2NaOH = 2NaCl + Co(OH)2
в) H2SO4 + 2NaOH = Na2SO4 + 2H2O
г) 2NaOH + Zn(OH)2 = Na2[Zn(OH)4]
1-30. Амфотерное соединение
| а) Ca(OH)2 | б) H2SO4 | в) Zn(OH)2 | г) Cu(OH)Cl |
1-31. Формулы основных солей:
| а) CaOHCl | б) ZnCl2 | в) Al(OH)2NO3 | г) KHSO4 |
1-32. Молекулярному уравнению реакции
KCl + AgNO3 = AgCl $+ KNO3 соответствует сокращенное ионное уравнение
а) K+ + NO3– = KNO3
б) Cl– + Ag+ = AgCl
в) K+ + 3NO– = KNO3
г) K+ + Cl– + Ag+ + NO3– = AgCl$ + K+ + NO3–
1-33. Молекулярному уравнению реакции CuO + 2HNO3 = Cu(NO)2 + H2O
соответствует сокращенное ионное уравнение:
а) CuO + 2HNO3 = Cu2+ + 2NO3– + H2O
б) CuO + 2H+ + 2NO3– = Cu2+ + 2NO3– + H2O
в) CuO + 2H+ = Cu2+ + H2O
г) Cu2+ + O2– + 2H+ = Сu2+ + H2O
д) O2– + 2H+ = H2O
1-34. Молекулярному уравнению реакции Zn(OH)2$ + H2SO4 = ZnSO4 + 2H2O соответствует сокращенное ионное уравнение
а) Zn(OH)2 + 2H+ + 4SO2– = Zn2+ + SO42– + 2H2O
б) Zn2+ + 2OH– + 2H+ + SO42– = Zn2+ + SO42– + 2H2O
в) Zn 2++ 2OH– + H2SO4 = ZnSO4 + 2H2O
г) Zn(OH)2 + 2H+ = Zn2+ + 2H2O
1-35. Сумма коэффициентов в сокращенном ионном уравнении реакции Zn(OH)2$ + H2SO4 = ZnSO4 + 2H2O равна
| а) 10 | б) 7 | в) 6 | г) 11 |
1-36. Сумма коэффициентов в сокращенном ионном уравнении реакции
CuO + 2HNO3 = Cu(NO)2 + H2O
| а) 5 | б) 6 | в) 7 | г) 9 |
1-37. Сумма коэффициентов в сокращенном ионном уравнении реакции
Na2CO3 + 2HNO3 = 2NaNO3 + CO2# + H2O
| а) 3 | б) 5 | в) 7 | г) 9 |
1-38. Соединения, принимающие участие в процессе
FeS$ + 2HCl = FeCl2 + H2S, которые в ионном уравнении реакции записываются в молекулярном виде
| а) FeS$ и HCl | в) HCl и H2S | д.) FeS$ и H2S |
| б) FeS$, FeHl2 и H2S | г) FeS$ , HCl и H2S |
1-39. Соединения, принимающие участие в процессе
CaCO3$ + 2HNO3 = Ca(NO)2 + CO2# + H2O, которые в ионном уравнении реакции записываются в молекулярном виде
| а) CaCO3$ , HNO3 , Ca(NO)2 и CO2# | в) CaCO3$ , HNO3 CO2# , H2O |
| б) CaCO3$ , Ca(NO)2 , CO2# H2O, HNO3 | г) CaCO3$ , CO2# и H2O |
1-40. Сумма коэффициентов в полном ионном уравнении, соответствующем реакции Ca(NO3)2 + Na2CO3 = CaCO3$ + 2NaNO3
| а) 12 | б) 11 | в) 10 | г) 9 |
1-41. Сумма коэффициентов в сокращенном ионном уравнении, соответствующем реакции CO2 + 2NaOH = Na2CO3 + H2O
| а) 11 | б) 10 | в) 9 | г) 5 | д) 4 |
1-42. Сумма коэффициентов в полном ионном уравнении, соответствующем реакции CO2 + 2NaOH = Na2CO3 + H2O
| а) 11 | б) 10 | в) 9 | г) 5 |
1-43. Реакции нейтрализации соответствует сокращенное ионное уравнение:
| а) H+ + OH– = H2O | г) 2H+ + CO32– = H2O + CO2 |
| б) Co2+ + 2OH– = Co(OH)2 | д) 3H+ + 3OH– = 3H2O |
| в) Ag+ + Cl– = AgCl |
