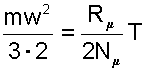Внутренняя энергия идеального газа.
Основные уравнение молекулярно-кинетической теории идеального газа. Средняя кинетическая энергия поступательного движения молекулы.
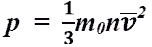 - основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
- основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
Это же уравнение в другой записи:
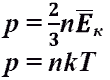
Средняя кинетическая энергия поступательного движения молекулы идеального газа
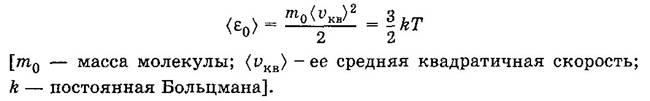
Молекулярно-кинетический смысл температуры.
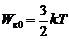
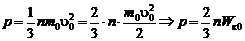
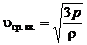
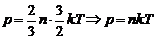
Внутренняя энергия идеального газа.
Исходя из определения идеального газа, в нем отсутствует потенциальная составляющая внутренней энергии (отсутствуют силы взаимодействия молекул, кроме ударного). Таким образом, внутренняя энергия идеального газа представляет собой только кинетическую энергию движения его молекул.
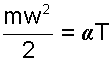 .
. 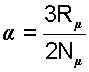 .
. 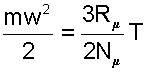 .
. 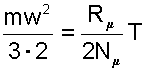
Теплоёмкость идеального газа при постоянном объёме и давлении.
При нагревании жидких и твердых тел их объем практически не изменяется, и работа расширения оказывается равной нулю. Поэтому все количество теплоты, полученное телом, идет на изменение его внутренней энергии. В отличие от жидкостей и твердых тел, газ в процессе теплопередачи может сильно изменять свой объем и совершать работу. Поэтому теплоемкость газообразного вещества зависит от характера термодинамического процесса. Обычно рассматриваются два значения теплоемкости газов: CV – молярная теплоемкость в изохорном процессе (V = const) и Cp – молярная теплоемкость в изобарном процессе (p = const).
В процессе при постоянном объеме газ работы не совершает: A = 0. Из первого закона термодинамики для 1 моля газа следует
|
Для процесса при постоянном давлении первый закон термодинамики дает:
|
Средняя, среднеквадратичная и наиболее вероятная скорости газовых молекул.
Сопоставляя все три скорости:
1) наиболее вероятную 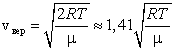 ,
,
2) среднюю 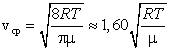 ,
,
3) среднюю квадратичную 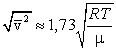 , – видим, что наименьшей из них является наиболее вероятная, а наибольшей – средняя квадратичная. Относительное число быстрых и медленных молекул мало (рис. 3.4).
, – видим, что наименьшей из них является наиболее вероятная, а наибольшей – средняя квадратичная. Относительное число быстрых и медленных молекул мало (рис. 3.4).
Основные уравнение молекулярно-кинетической теории идеального газа. Средняя кинетическая энергия поступательного движения молекулы.
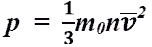 - основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
- основное уравнение МКТ идеального газа. Выведено в предположении, что давление газа есть результат ударов его молекул о стенки сосуда.
Это же уравнение в другой записи:
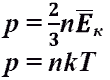
Средняя кинетическая энергия поступательного движения молекулы идеального газа
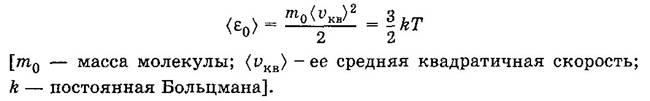
Молекулярно-кинетический смысл температуры.
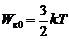
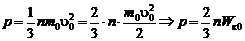
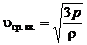
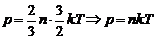
Внутренняя энергия идеального газа.
Исходя из определения идеального газа, в нем отсутствует потенциальная составляющая внутренней энергии (отсутствуют силы взаимодействия молекул, кроме ударного). Таким образом, внутренняя энергия идеального газа представляет собой только кинетическую энергию движения его молекул.
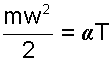 .
. 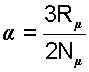 .
. 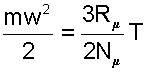 .
.