Устойчивость и коагуляция дисперсных систем
Характерной чертой дисперсных систем является их агрегативная неустойчивость.
Коагуляция– это процесс распада коллоидного раствора на осадок дисперсной фазы (коагулят) и дисперсионную среду, происходящий вследствие слипания частичек дисперсной фазы. Вытянутые частички дисперсной фазы при коагуляции превращаются в гель.
Свежеполученные коагуляты во многих случаях способны вновь переходить в состояние золя. Такой изотермический переход коагулят → золь называют пептизацией, а вызывающие его вещества – пептизаторами.
Способность раздробленных систем сохранять присущую им степень дисперсности называют агрегативной устойчивостью. Предотвращение агрегации первичных дисперсных частиц возможно в результате действия трех факторов устойчивости дисперсных систем: 1) кинетического; 2) электрического и 3) структурно-механического.
1. Кинетический фактор. Необходимым условием слипания двух частиц дисперсной фазы является их сближение, достаточное для проявления сил притяжения. Если частота столкновения коллоидных частиц мала, то дисперсная система будет устойчивой. Это возможно при очень малой концентрации дисперсных частиц или при очень высокой вязкости дисперсионной среды.
2. Электрический фактор. Большинство устойчивых дисперсных систем кроме дисперсной фазы и дисперсионной среды содержат третий компонент, являющийся стабилизатором дисперсности. Им могут быть как ионы, так и молекулы, в связи с чем различают два механизма стабилизации дисперсных систем: электрический и молекулярно-адсорбционный.
а) электрическая стабилизация связана с возникновением двойного электрического слоя на границе раздела фаз в полярной среде, например, в воде. Коллоидные мицеллы имеют одинаковый знак заряда и поэтому электростатически отталкиваются друг от друга.
Коагуляция коллоидов возможна при добавлении электролитов к раствору, поскольку противоионы вытесняются из диффузной части в адсорбционную, толщина двойного электрического слоя уменьшается и происходит слипание частичек, т.е. коагуляция.
Коагулирующее действие электролитов характеризуется порогом коагуляции – т.е. наименьшей концентрацией электролита, вызывающего коагуляцию. Порог коагуляции для большинства электролитов лежит в пределах от 10-5 до 0,1 моля в литре золя. Он зависит от заряда коагулирующего иона электролита, т.е. иона, заряд которого противоположен по знаку заряду коллоидной частицы: чем больше заряд иона, тем меньше порог коагуляции.
б) молекулярно-адсорбционная стабилизация дисперсных систем происходит в результате образования вокруг коллоидных частиц адсорбционных слоев из молекул дисперсионной среды и растворенных в ней веществ, которые создают механическое препятствие сближению коллоидных частиц.
3. Структурно-механический фактор стабилизации имеет место при добавлении к дисперсным системам поверхностно-активных веществ и высокомолекулярных соединений, образующих защитные пленки на поверхности коллоидов. Эти вещества называют защитными коллоидами. К ним относятся мыла щелочных металлов, белки, крахмал, каучуки.
Пример 1.
К каким дисперсным системам относятся мыльная пена, зубной порошок, рубин? Запишите схематические формулы этих дисперсных систем.
Решение. Мыльная пена – это дисперсия газа в жидкости, причем жидкость вырождается до тонких пленок, разделяющих пузырьки газа. Следовательно, дисперсионная среда – жидкая, дисперсная фаза – газообразная. Схематическая формула этой системы Ж1-Г2.
Зубной порошок, как и все порошки, представляет собой части твердой дисперсной фазы, разделенные газообразной средой. Схематическая формула системы Г1-Т2.
Драгоценный камень рубин представляет собой дисперсию оксида хрома Cr2O3 в оксиде алюминия Al2O3. В данном случае оба вещества находятся в твердой фазе, следовательно, схематическая формула этой дисперсной системы Т1-Т2, где дисперсионная среда Т1 – Al2O3, а дисперсная фаза Т2 – Cr2O3.
Пример 2.
Рассчитайте суммарную площадь поверхности 1 см3 вещества, раздробленного до кубических частиц с длиной ребра 1 мкм. Как изменятся суммарная площадь поверхности и удельная поверхность при дальнейшем дроблении вещества до кубических частиц коллоидной дисперсности с длиной ребра 10-6 см? Вычислите степень дисперсности вещества.
Решение. Рассчитаем удельную поверхность вещества до дробления:
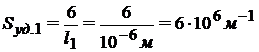 , т.к. 1 мкм = 10-6 м.
, т.к. 1 мкм = 10-6 м.
Суммарная площадь поверхности 1 см3 вещества составит:
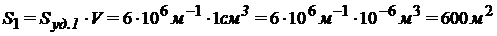 , т.к. 1 см = 10-2 м.
, т.к. 1 см = 10-2 м.
При дроблении вещества
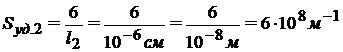
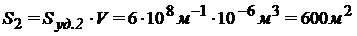
Следовательно, при дроблении вещества суммарная площадь поверхности и удельная поверхность увеличились в 100 раз:
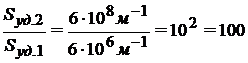 ;
;
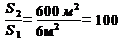 .
.
Вычислим степень дисперсности 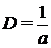 , для кубических частиц a = l:
, для кубических частиц a = l:
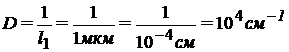 , т.к. 1 мкм = 10-4 см;
, т.к. 1 мкм = 10-4 см;
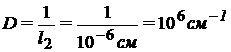 .
.
Пример 3.
Изобразите схему строения коллоидной мицеллы, полученной при взаимодействии сильно разбавленных растворов CH3COOAg и NaCl при небольшом избытке в первом случае CH3COOAg, во втором случае – NaCl.
Решение. При взаимодействии растворов CH3COOAg и NaCl происходит следующая реакция:
CH3COOAg + NaCl → AgCl ↓ + CH3COONa
Нерастворимое вещество будет образовывать ядро коллоидной частицы. Поскольку в первом случае в избытке находится CH3COOAg, значит именно это вещество будет являться стабилизатором золя, образуя следующие ионы:
СН3СООAg → CН3COO- + Ag+
На поверхности ядра в первую очередь будут сорбироваться ионы Ag+, идентичные ионам, образующим кристаллическую решетку ядра, а затем уже ионы CН3COO-, формирующие две части слоя противоионов – адсорбционную и диффузную:

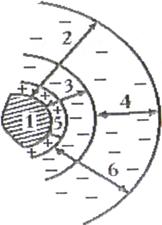 | 1 – ядро; |
| 2 – двойной электрический слой; | |
| 3 – его адсорбционная часть; | |
| 4 – его диффузная часть; | |
| 5 – потенциалопределяющий слой (Ag+); | |
| 6 – слой противоионов (CН3COO-). |
Формула коллоидной мицеллы будет иметь следующий вид:
{mAgCl · nAg+ · (n - х) CН3COO- }х CН3COO-.
Во втором случае, при избытке NaCl, функцию стабилизатора будет выполнять NaCl:
NaCl → Na++ Cl--.
Ядро коллоидной мицеллы также будет состоять из ассоциатов молекул нерастворимого вещества AgCl, однако во втором случае потенциалопределяющий слой образуют ионы Cl-, а слой противоионов – Na+:
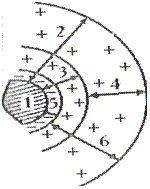 1 - ядро;
1 - ядро;
2 - двойной электрический слой;
3 - его адсорбционная часть;
4 - его диффузная часть;
5 - потенциалопределяющий слой (Cl-);
6 - слой противоионов (Na+).
Формула коллоидной мицеллы:
{mAgCl · nCl- · (n - х)Na+ }х Na+
Пример 4.
В три колбы с золем AgBr (стабилизатор КВr) прилили одинаковые количества следующих растворов: в первую – раствор NaCl, во вторую – раствор AlCl3, в третью – раствор Na3PO4. Что произойдет в каждой колбе? Ответ мотивировать.
Решение. Все три раствора – NaCl, AlCl3, Na3PO4 – являются электролитами и, следовательно, вызовут коагуляцию золя. Однако их коагулирующее действие будет различаться.
Запишем формулу данного золя:
{mAgBr · nBr- · (n - х)K+ }х K+.
Заряд коллоидных частиц будет отрицательным:
{mAgBr · nBr- · (n - х)К+}Х-.
Коагуляцию такого золя могут вызвать ионы противоположного знака: Na+ и А13+. Сильнее коагуляция будет выражена при действии иона, обладающего большой величиной заряда, т.е. при приливании раствора, содержащего А13+. Следовательно, быстрее и более полно произойдет коагуляция во второй колбе, содержащей раствор AlCl3. В первой и третьей колбе коагуляцию вызовет один и тот же ион Na+, следовательно, степень коагуляции золя в этих колбах будет одинакова.
Вопросы и задачи
1. Что такое аэрозоль? Запишите схематическую формулу аэрозоля и приведите примеры. Возможно ли существование аэрозоля Г1 - Г2? Ответ мотивируйте.
2. Что такое эмульсия? Запишите схематическую формулу эмульсии и приведите примеры. Что такое Ж1 - Т2 и чем эта дисперсная система отличается от эмульсии?
3. Что такое золь? Запишите схематическую формулу золя и приведите примеры. Что такое Т1 - Ж2 и чем эта дисперсная система отличается от золя?
4. Что такое суспензия? Запишите схематическую формулу суспензии и приведите примеры. Что такое Т1 - Т2 и чем эта дисперсная система отличается от суспензии?
5. Что такое пена? Запишите схематическую формулу пены и приведите примеры. Что такое T1 - Г2 и чем эта дисперсная система отличается от пен?
6. Что такое твердые пены? Запишите их схематическую формулу и приведите примеры. Что такое Ж1- Г2 и чем эта дисперсная система отличается от твердых пен?
7. Что общего и отличительного у суспензий и золей? Запишите их схематические формулы и приведите примеры.
8. Какие дисперсные системы могут образовывать газы? Запишите их схематические формулы и приведите примеры.
9. Какие дисперсные системы могут образовывать жидкости? Запишите их схематические формулы и приведите примеры.
10. Какие дисперсные системы могут образовывать твердые вещества? Запишите их схематические формулы и приведите примеры.
11. Какие дисперсные системы могут образовывать газ и жидкость друг с другом? Запишите их схематические формулы и приведите примеры.
12. Какие дисперсные системы могут образовывать друг с другом газ и твердое вещество? Запишите их схематические формулы и приведите примеры.
13. Какие дисперсные системы могут образовывать жидкость и твердое вещество друг с другом? Запишите их схематические формулы и приведите примеры.
14. Перечислите дисперсные системы, в которых дисперсная фаза представлена газом. Запишите их схематические формулы и приведите примеры.
15. Перечислите дисперсные системы, в которых дисперсная фаза представлена жидкостью. Запишите их схематические формулы и приведите примеры.
16. Перечислите дисперсные системы, в которых дисперсная фаза представлена твердым веществом. Запишите их схематические формулы и приведите примеры.
17. Сахар растворили в а) воде; б) этиловом спирте; в) бензине. В каком случае может быть получена дисперсная система? Запишите схематическую формулу этой системы и укажите ее название. Ответ мотивируйте.
18. Хлорид натрия растворили в а) воде; б) керосине; в) бензоле. В каких случаях может быть получена дисперсная система? Запишите схематическую формулу этой системы и укажите ее название. Ответ мотивируйте.
19. К каким дисперсным системам относятся туман, сплавы металлов, морская пена? Запишите схематические формулы этих дисперсных систем.
20. К каким дисперсным системам относятся пыль, коровье молоко, пемза? Запишите схематические формулы этих дисперсных систем.
21. К каким дисперсным системам относится лондонский смог (туман с пылью и дымом)? Запишите их схематические формулы.
22. К каким дисперсным системам относятся нефть, облака, бетон? Запишите схематические формулы этих дисперсных систем.
23. К как 
 им дисперсным системам относятся зубная паста, перламутр, противопожарная пена? Запишите схематические формулы этих дисперсных систем.
им дисперсным системам относятся зубная паста, перламутр, противопожарная пена? Запишите схематические формулы этих дисперсных систем.
24. К каким дисперсным системам относятся пенопласт, стиральный порошок, речной ил? Запишите схематические формулы этих дисперсных систем.
25. К каким дисперсным системам относятся хлебобулочные изделия, газированная вода, дым костра? Запишите схематические формулы этих систем.
 26-39. Рассчитайте суммарную площадь поверхности 1 см3 вещества, раздробленного до кубических частиц с длиной ребра, равной ℓ1. Как изменятся суммарная площадь поверхности и удельная поверхность при дальнейшем дроблении вещества до кубических частиц коллоидной дисперсности с длиной ребра ℓ2? Вычислите степень дисперсности вещества.
26-39. Рассчитайте суммарную площадь поверхности 1 см3 вещества, раздробленного до кубических частиц с длиной ребра, равной ℓ1. Как изменятся суммарная площадь поверхности и удельная поверхность при дальнейшем дроблении вещества до кубических частиц коллоидной дисперсности с длиной ребра ℓ2? Вычислите степень дисперсности вещества.
26. ℓ1 = 2 мкм; ℓ2 = 10-5 см
27. ℓ1 = 2 мкм; ℓ2 = I0-6 см
28. ℓ1 = 2 мкм; ℓ2 = 10-7см
29. ℓ1 = 2,5 мкм; ℓ2 = 10-5 см
30. ℓ1 = 2,5 мкм; ℓ2 = 10-6 см
31. ℓ1 = 2,5 мкм; ℓ2 = 10-7 см
32. ℓ1 = 5 мкм; ℓ2 = 10-5 см
33. ℓ1 = 5 мкм; ℓ2 = 10-6 см
34. ℓ1 = 5 мкм; ℓ2 = 10-7 см
35. ℓ1 = 10 мкм; ℓ2 = 10-5 см
36. ℓ1 = 10 мкм; ℓ2 = 10-6 см
37. ℓ1 =10 мкм; ℓ2 = 10-7 см
38. ℓ1 = 1 мкм; ℓ2 = 10-5 см
39. ℓ1 = 1 мкм; ℓ2 = 10-7 см
40-50. Рассчитайте суммарную площадь поверхности 1 см3 вещества, раздробленного до сферических частиц с радиусом r1. Как изменятся суммарная площадь поверхности и удельная поверхность при дальнейшем дроблении вещества до сферических частиц коллоидной дисперсности с радиусом r2? Вычислите степень дисперсности вещества.
40. r1 = 1 мкм; r2 = 10-5 см
41. r1 = 1 мкм; r2 = 10-6 см
42. r1 = 1 мкм; r2 = 10-7 см
43. r1 = 2 мкм; r2 = 10-5 см
44. r1 = 2 мкм; r2 = 10-6 см
45. r1 = 2 мкм; r2 = 10-7 см
46. r1 = 2,5 мкм; r2 = 10-5 см
47. r1 = 2,5 мкм; r2 = 10-6 см
48. r1 = 2,5 мкм; r2 = 10-7 см
49. r1 = 0,5 мкм; r2 = 10-5 см
50. r1 = 0,5 мкм; r2 = 10-7 см
51-75. Изобразите схему строения коллоидной мицеллы, полученной при взаимодействии сильноразбавленных растворов первого вещества со вторым при небольшом избытке в первом случае первого вещества, во втором случае – второго вещества. Запишите формулы коллоидных мицелл.
51. AgNO3 и NaBr.
52. FeSO4 и NaOH.
53. FeCI3 и КОН.
54. FeSO4 и К2СО3.
55. AgNO3 и КСl.
56. CuSO4 и NaOH.
57. CaCl2 и Na2СО3.
58. MgSO4 и Na2SiO3.
59. MgCl2 и Na2СО3.
60. SrCl2 и К2СО3.
61.CН3COOAg и NaI.
62. ZnSO4 и Na2СО3.
63. AlCl3 и Na3РО4.
64. CH3COOAg и KBr.
65. Pb(NO3)2 и Na2SO4.
66. Pb(СН3СОО)2 и K2SO4.
67. MnCl2 и Na2S.
68. CrCl3 и КОН.
69. BaCl2 и (NH4)2SO4.
70. ZnCl2 и NaOH.
71. BaCl2 и MnSO4.
72. Cu(NO3)2 и Na2S.
73. Fe(NO3)3 и K2S.
74. SnCl2 и КОН.
75. MnCl2 и Ва(ОН)2.
76. Что такое дисперсные системы? В чем различие между моно- и полидисперсными, свободно- и связнодисперсными системами? К каким дисперсным системам относится почва? Из скольких фаз состоит почва как дисперсная система?
77. В чем отличие растворов от дисперсных систем, истинных растворов от коллоидных? Может ли хлорид натрия образовывать истинные и коллоидные растворы? Ответ мотивировать.
78. Чем различаются золь и гель? Возможен ли переход из золя в гель и обратно? Ответ подтвердить примерами.
79. Что такое коллоиды? коагуляция коллоидов? В чем причина коагуляции коллоидов? Что может вызвать коагуляцию коллоидов? Ответ подтвердить примерами.
80. Что такое пептизация коллоидов? Как гидроксид железа (III) можно перевести из коагулята в золь и золь в коагулят?
81. Что известно о коагулирующем действии электролитов? Какая из солей - NaCl, Na2SO4, Na3PO4 - оказывает большое воздействие на коагуляцию коллоидов? Ответ мотивировать.
82. Что такое порог коагуляции? Как он будет изменяться в ряду солей NaCl – BaCl2 – FeCl3? Ответ мотивировать.
83. В три колбы с золем Аl(ОН)3 (стабилизатор АlСl3) прилили следующие растворы: в первую - раствор KNO3, во вторую – FeCl3, в третью – K2SO4. Что произойдет в каждой колбе? Ответ мотивируйте.
84. В три колбы с золем AgCl (стабилизатор КС1) прилили следующие растворы солей в одинаковом количестве: в первую колбу - раствор NaNO3, во вторую – A1(NO3)3, в третью – Na3PO4. Что произойдет в каждой колбе? Ответ мотивировать.
85. В три колбы с золем H2SiО3 (стабилизатор Na2SiО3) прилили одинаковые количества следующих растворов: в первую колбу – раствор NaCl, во вторую – А1С13, в третью – Na2SO4. В каких колбах произойдет коагуляция золя и где она будет выражена сильнее? Ответ мотивируйте.
86. В три колбы с золем Fe(OH)3 (стабилизатор FeCl3) прилили одинаковые количества следующих растворов: в первую колбу – раствор NaCl, во вторую – Na2SO4, в третью – А1С13. В каких колбах произойдет коагуляция золя и где она будет выражена сильнее? Ответ мотивируйте.
87. В три колбы с золем МnО2 (стабилизатор КМnО4) прилили одинаковые количества следующих растворов: в первую колбу – раствор NaCI, во вторую – FeCl3, в третью – Na3PO4. В каких колбах произойдет коагуляция золя и где она будет выражена сильнее? Ответ мотивируйте.
88. В три колбы с золем добавили раствор электролита в таких количествах, что концентрация электролита в первой колбе составила 10-6 моль/л, во второй – 10-3 моль/л, в третьей – 1 моль/л. Что будет при этом наблюдаться в каждой колбе? Ответ мотивируйте.
89. Что такое электрокинетический потенциал? Как он изменяется при добавлении к коллоидному раствору электролита? Ответ мотивируйте.
90. В одну из пробирок с золем Al(OH)3 (стабилизатор AlCl3) прилили золь AgBr (стабилизатор КВг), а во вторую – золь BaSO4 (стабилизатор ВаС12). Что произойдет в каждой пробирке? Ответ мотивируйте.
91. В одну из пробирок с золем AgCl (стабилизатор NaCl) прилили золь Сu(ОН)2 (стабилизатор СuС12), а во вторую – золь PbSO4 (стабилизатор Pb(NO3)2. Что произойдет в каждой пробирке? Ответ мотивируйте.
92. В одну из пробирок с золем СаСО3 (стабилизатор Na2CO3) прилили золь Mg(OH)2 (стабилизатор MgCl2), а во вторую – золь Н2SiO3 (стабилизатор Na2SiO3). Что произойдет в каждой пробирке? Ответ мотивируйте.
93. Как можно стабилизировать дисперсные системы? Что такое стабилизатор? Какие виды стабилизации дисперсных систем существуют? Приведите примеры.
94. Что произойдет, если к золю AgCl прилить раствор Na3PO4? Изменится ли результат, если к золю предварительно добавить раствор крахмала? Ответ мотивировать.
95. В две колбы с золем МnО2 прилили следующие растворы: в первую – раствор NaCl, во вторую – сначала раствор мыла, а затем NaCl. Что произойдет в каждой колбе? Ответ мотивируйте.
96. В две колбы с золем Al(OH)3 прилили следующие растворы: в первую – раствор K2SO4, во вторую – сначала раствор желатина, а затем K2SO4. Что произойдет в каждой колбе? Ответ мотивируйте.
97. В три колбы с золем Н2SiO3 добавили следующие растворы: в первую – раствор Na2SO4, во вторую – раствор крахмала, в третью – дистиллированную воду. Как изменится устойчивость золя в каждой колбе? Ответ мотивируйте.
98.В три колбы с золем Fe(OH)3 добавили следующие растворы: в первую – раствор мыла, во вторую – дистиллированную воду, в третью – раствор K2SO4. Как изменится устойчивость золя в каждой колбе? Ответ мотивируйте.
99. Что такое сорбция? хемосорбция? Написать уравнения хемосорбционных процессов поглощения углекислого газа водой и оксидом кальция, а также поглощения аммиака водой.
100. К каким видам сорбции относятся процесс растворения кислорода в воде, поглощение углекислого газа раствором гидроксида кальция, поглощение отравляющих веществ активированным углем, поглощение катионов почвой? Ответ мотивируйте.
КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
Комплексными называются такие соединения, которые характеризуются наличием хотя бы одной ковалентной связи, возникшей по донорно-акцепторному механизму.
Согласно координационной теории Вернера, молекула комплексного соединения содержит центральный ион, несущий обычно положительный заряд и называемый комплексообразователем. Последний удерживает (координирует) в непосредственной близости от себя некоторое число ионов с противоположным зарядом или полярных молекул, называемых лигандами.
Ион-комплексообразователь и лиганды составляют вместе внутреннюю координационную сферу соединения. Остальные,более удаленные от комплексообразователя ионы, образуют внешнюю сферу. В формулах комплексных соединений внутреннюю сферу отделяют от внешней квадратными скобками. Число ионов или полярных молекул, координируемое комплексообразователем во внутренней сфере, называют координационным числом. Чаще всего оно имеет значение 4 и 6. Ниже приводятся значения координационных чисел для некоторых ионов-комплексообразователей.
