Химические свойства классов органических соединений
| Алканы CnH2n+2 | 1. Реакции по С–H-связи: 1.1. Реакции свободнорадикального замещения (свет, нагрев): CH4 + Cl2 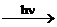 CH3Cl + HCl CH3Cl + Cl2 CH3Cl + HCl CH3Cl + Cl2 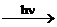 CH2Cl2 + HCl 1.2. Нитрование: С6H14 + HNO3 CH2Cl2 + HCl 1.2. Нитрование: С6H14 + HNO3 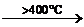 C6H13NO2 + H2O 1.3. Дегидрогенизация: С4H10 C6H13NO2 + H2O 1.3. Дегидрогенизация: С4H10 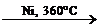 C4H8 + H2 2. Реакции окисления 2.1. Горение: CH4 + 2O2 → CO2 + 2H2O 2.2. Каталитическое окисление (промышленное): CH4 C4H8 + H2 2. Реакции окисления 2.1. Горение: CH4 + 2O2 → CO2 + 2H2O 2.2. Каталитическое окисление (промышленное): CH4 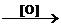 CH3OH CH4 CH3OH CH4 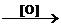 HCOH + H2O 3. Реакции по С–С-связи (крекинг): CH4 HCOH + H2O 3. Реакции по С–С-связи (крекинг): CH4 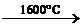 HC≡CH + H2 C4H10 HC≡CH + H2 C4H10 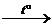 C2H6 + C2H4 C2H6 + C2H4 |
| Алкены CnH2n | 1. Горение: H2C=CH2 + 3O2 → 2CO2 + 2H2O 2. Реакции электрофильного присоединения по связи С=С: H3C–CH=CH2 + HBr → H3C–CHBr–CH3 H2C=CH2 + Br2 → BrCH2–CH2Br 3. Радикальная полимеризация: nH2C=CH2 → (–CH2–CH2–)n 4. Гидратация: H2C=CH2 + H2O 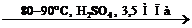 CH3–CH2–OH 5. Окисление: 3H2C=CH2 + 2KMnO4 + 4H2O → 3OH–CH2–CH2–OH + 2KOH + 2MnO2↓ 6. Гидрогенизация: H2C=CH2 + H2 CH3–CH2–OH 5. Окисление: 3H2C=CH2 + 2KMnO4 + 4H2O → 3OH–CH2–CH2–OH + 2KOH + 2MnO2↓ 6. Гидрогенизация: H2C=CH2 + H2 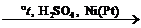 H3C–CH3 7. Радикальное галогенирование: CH3CH=CH2 H3C–CH3 7. Радикальное галогенирование: CH3CH=CH2 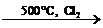 Cl–CH2CH=CH2 + HCl Cl–CH2CH=CH2 + HCl |
| Диеновые углеводороды CnH2n-2 | 1. Реакции электрофильного присоединения H2C=CH–CH=CH2 + Br2 → Br–CH2–CH=CH–CH2–Br H2C=CH–CH=CH2 + Br2 → CH2=CH–CHBr–CH2–Br 2. Реакция полимеризации nH2C=CH–CH=CH2 → (–CH2–CH=CH–CH2–)n |
| Алкины CnH2n-2 | 1. Реакции электрофильного присоединения по С≡С-связи: 1.1. Галогенирование: H–C≡C–H + Br2 → BrHC=CHBr + Br2 → Br2HC=CHBr2 1.2. Гидрогалогенирование: H–C≡C–H + HBr → BrHC=CH2 + HBr → Br2HC=CH3 1.3. Гидратация: H–C≡C–H + H2O 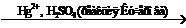 H2C=CHOH → CH3–COH 1.4. Гидрирование: H–C≡C–H + H2 H2C=CHOH → CH3–COH 1.4. Гидрирование: H–C≡C–H + H2 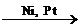 H2C=CH2 + H2 → H3C–CH3 1.5. Полимеризация: 3H–C≡C–H H2C=CH2 + H2 → H3C–CH3 1.5. Полимеризация: 3H–C≡C–H 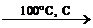 С6H6 1.6. Окисление: H–C≡C–H + [O] С6H6 1.6. Окисление: H–C≡C–H + [O]  HOOC–COOH → HCOOH + CO2 HOOC–COOH → HCOOH + CO2 |
| Арены (ароматические углеводороды) | 1. Реакции электрофильного замещения: C6H6 + Br2 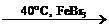 C6H5Br + HBr С6H6 + CH3Br C6H5Br + HBr С6H6 + CH3Br 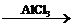 C6H5–CH3 + HBr C6H6 + HNO3 C6H5–CH3 + HBr C6H6 + HNO3 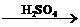 C6H5–NO2 + H2O 2. Реакции присоединения: С6H6 + 3H2 C6H5–NO2 + H2O 2. Реакции присоединения: С6H6 + 3H2 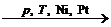 C6H12 C6H6 + 3Cl2 C6H12 C6H6 + 3Cl2 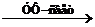 C6H6Cl6 C6H6Cl6 |
| Спирты | 1. Реакции с участием водородного атома OH–-группы: 1.1. Взаимодействие с металлами: 2R–OH + 2Na = 2R–ONa + NaOH 1.2. Реакция этерификации (с кислотами): CH3COOH + HOCH3 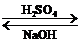 CH3–CO–O–CH3 + H2O 2. Взаимодействие с галогеноводородами: R–OH + HBr CH3–CO–O–CH3 + H2O 2. Взаимодействие с галогеноводородами: R–OH + HBr 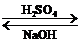 R–Br + H2O 3. Окисление спиртов: CH3–CH2–OH + СuO → CH3–COH + H2O + Cu 4. Дегидратация: CH3–CH2–OH R–Br + H2O 3. Окисление спиртов: CH3–CH2–OH + СuO → CH3–COH + H2O + Cu 4. Дегидратация: CH3–CH2–OH 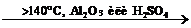 CH2=CH2 + H2O 2CH3–CH2–OH CH2=CH2 + H2O 2CH3–CH2–OH 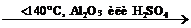 CH3–CH2–O–CH2–CH3 + H2O H3C–CH(OH)–CH2–CH3 → CH3–CH=CH–CH3 + H2O CH3–CH2–O–CH2–CH3 + H2O H3C–CH(OH)–CH2–CH3 → CH3–CH=CH–CH3 + H2O |
| Фенолы | 1. Взаимодействие с металлами: 2C6H5–OH + 2Na → 2C6H5–ONa + H2↑ 2. Взаимодействие со щелочами: C6H5–OH + NaOH → C6H5–ONa + H2O 3. Взаимодействие со спиртами: С6H5–OH + C2H5–OH → C6H5–O–C2H5 + H2O 4. Галогенирование: С6H5–OH + 3Br3(водн) → С6H2Br3–OH + 3HBr 5. Взаимодействие с азотной кислотой (нитрование): C6H5–OH + 3HNO3 (разб.) 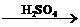 C6H2(NO2)3 + 3H2O 6. Реакция поликонденсации: nC6H5–OH + nHCOH → nOH–C6H4–CH2–OH nOH–C6H4–CH2–OH + C6H5OH → (–C6H4(OH)–CH2– C6H4(OH)–)n + H2O C6H2(NO2)3 + 3H2O 6. Реакция поликонденсации: nC6H5–OH + nHCOH → nOH–C6H4–CH2–OH nOH–C6H4–CH2–OH + C6H5OH → (–C6H4(OH)–CH2– C6H4(OH)–)n + H2O |
| Альдегиды и кетоны CnH2nO | 1. Реакции окисления: R–COH + Ag2O → R–COOH + 2Ag CH3–COH + 2Cu(OH)2 → CH3COOH + Cu2O + 2H2O 2. Поликонденсация с фенолом – смотри выше. 3. Реакции восстановления водородом: CH3–CO–CH3 + H2 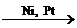 CH3–CH(OH)–CH3 CH3–CH(OH)–CH3 |
| Амины | 1. Взаимодействие с кислотами: CH3NH2 + HCl → [CH3–NH3]Cl 2. Взаимодействие с алкилгалогенидами: CH3NH2 + CH3I 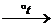 (CH3)2NH + HI → [(CH3)2NH2]I 3. Взаимодействие с органическими кислотами и ангидридами: CH3COOH+CH3NH2→[CH3COO]–[CH3NH3]+ →CH3–CO–NH-CH3+H2O 4. Гидролиз аминов: CH3NH2 + H2O (CH3)2NH + HI → [(CH3)2NH2]I 3. Взаимодействие с органическими кислотами и ангидридами: CH3COOH+CH3NH2→[CH3COO]–[CH3NH3]+ →CH3–CO–NH-CH3+H2O 4. Гидролиз аминов: CH3NH2 + H2O 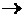 CH3NH3+ + OH– 5. Горение: 4CH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2 6. Бромирование анилина: C6H5–NH2 + 3Br2 → C6H2Br3 + 3HBr CH3NH3+ + OH– 5. Горение: 4CH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2 6. Бромирование анилина: C6H5–NH2 + 3Br2 → C6H2Br3 + 3HBr |
Контрольные вопросы
1. Опишите, как классифицируются органические соединения в зависимости от структуры углеродного скелета. Чем отличаются карбоциклические и гетероциклические соединения?
2. Как распределяются по классам органические соединения с различными функциональными группами?
3. Сформулируйте правила номенклатуры органических соединений.
4. Что такое субстрат и реагент? Дайте определение электрофильному и нуклеофильному реагентам.
5. Приведите примеры реакций электрофильного и нуклеофильного замещения как гетеролитических реакций.
5. Рассмотрите гомолитические реакции на примере реакции радикального замещения.
6. Дайте определение и приведите пример реакции элиминирования.
7. Приведите пример реакции перегруппировки. Какими могут быть реакции перегруппировки?
Примеры выполнения заданий
Пример 1. Составьте структурную формулу вещества: 4-амино-2-хлор-2-бутеновая кислота.
По номенклатуре ИЮПАК в основу названия положена углеродная цепь, содержащая максимальное число функциональных групп. Начало цепи определяет наиболее старшая функциональная группа. Порядок старшинства следующий:
COOH > C≡N > CHO > C=O > OH > NH2 > NO2 > Hal.
Кратную связь также можно рассматривать как функцию. Углеводороды, содержащие кратные связи подразделяются на: алкены (>С=С<), алкины ( –С≡С– ), диены (>С=С=С<).
Главная функция обозначается в названии суффиксом: гидроксильная группа -ол; альдегидная -аль;кетонная -он; двойная связь -ен; тройная связь -ин и т.д., остальные – префиксами.
В предложенном примере нумерация атомов начинается с карбоксильной группы (первый атом углерода). Всего в главной цепи 4 атома углерода, что следует из корня в названии кислоты. У второго атома углерода имеется заместитель атом галогена –Cl. Второй атом углерода соединяется с третьим двойной связью, на что указывает суффикс -ен (бутеновая). Четвертый атом углерода имеет заместитель – амино-группу.
Структурная формула: H2N–CH2–CH=CCl–COOH.
Пример 2. Составьте структурные формулы всех изомеров предложенного вещества: пентин-1.
Вещество принадлежит к гомологическому ряду ацетилена, на что указывает суффикс -ин. Тройная связь находится между первым и вторым атомами углерода. Изомерия этого вещества может быть связана с положением тройной связи и разветвлением углеродной цепи:
CH3–CH2–CH2–C≡CH пентин-1;
CH3–CH2–C≡C–CH3 пентин-2;
CH3–CH(CH3) –C≡CH 3-метил-бутин-1.
Пример 3. Напишите уравнения реакций следующих превращений, укажите тип реакции:
CH3–CH2–CH3 → CH3–CH=CH2 → CH3–CHBr–CH3
↓
(–CH2–CH–)n
│
CH3
1) Реакция дегидрирования при высокой температуре:
CH3–CH2–CH3 → CH3–CH=CH2 + H2.
2) Реакция электрофильного присоединения галогеноводорода по правилу Марковникова:
CH3–CH=CH2 + HBr → CH3–CHBr–CH3.
3) Получение полипропилена реакцией полимеризации:
CH3–CH=CH2 → (–CH2–CH–)n
│
CH3
Задания для самостоятельной работы
Задание 1. Составьте структурные формулы веществ:
| № вар. | Названия веществ |
| 3-этилгептан, 4,5-диметил-гексен-3-он-2 | |
| 2,4-диметилгексан; 4-амино-2-бутеновая кислота | |
| 2-метил-3-этилгептан; 2-хлорбутановая кислота | |
| 3-метил-5-этилгептан; 2-метилпропаналь | |
| 2,2-диметилпропан; 2,4-дихлорфенол | |
| 2,3-диметилпентан; трихлоруксусная кислота | |
| 2-метил-4-этилгексан; пропионат натрия | |
| 3-метил-6-этилоктан; 3-метилбутаналь | |
| 2-метилпропен; 3,3-диметилпентанол-2 | |
| 2-метилбутен-1; 2-метилпропанол-2 | |
| метилциклопентан; 2-метилпропанол-1 | |
| Этилциклогексан; 1,2-диметил-4-этилбензол | |
| 3-метилбутин-1; 1-метил-3-этилбензол | |
| 4-метилгексин-1; 1,2-диметилбензол | |
| пентадиен-2,3; этилбензол |
Задание 2.Составьте структурные формулы всех изомеров предложенных веществ, дайте им названия:
| Вариант | |||||
| Вещество | гексен-1 | гексин-1 | гексан | гептан | пентадиен-1,2 |
| Вариант | |||||
| Вешество | пентанол-1 | гексанон | гептин-1 | гексанол-1 | гексадиен1,2 |
| Вариант | |||||
| Вещество | пентаналь | гептаналь | бутаналь | бутанол-1 | пентанон-2 |
Задание 3. Решите расчетную задачу:
1. Сколько литров оксида углерода (IV) образуется при сгорании 3 моль этилена?
2. Вычислите относительную плотность тетрахлорметана по воздуху. Объясните негорючесть этого вещества.
3. Найдите молекулярную формулу вещества, содержащего 82,8% углерода и 17,2% водорода, плотность вещества (при н.у.) 2,59 г/л.
4. При сжигании 8,8 г углеводорода образовалось 26,4г оксида углерода (IV) Плотность вещества (при н.у.) 1,96 г/л. Найдите его молекулярную формулу.
5. Сколько литров воздуха, измеренного (при н.у.), потребуется для полного сжигания смеси 3 моль метана и 20 л этана?
6. При пропускании этилена через жидкий бром масса склянки с бромом увеличилась на 7 г. Сколько литров (при н.у) этилена поглотилось при этом? Сколько г дибромэтана получилось?
7. Продукт взаимодействия непредельного углеводорода с хлором имеет молекулярную массу 113. Найдите формулу этого углеводорода.
8. Какой объем водорода могут присоединить: а) 200 мл пропена, б) 70 г пентена?
9. Найдите молекулярную формулу газообразного углеводорода, если при сжигании 10,2 л его (н.у) было получено 33,6 л оксида углерода (IV) и 27 г воды.
10. Какое максимальное количество брома может вступить в реакцию с 3,36 л бутадиена (при н.у)?
11. Составьте уравнение полного сгорания ацетилена и рассчитайте объем кислорода (при н.у.), необходимый для сжигания 39 г ацетилена.
12. Какое максимальное количество брома (в граммах) может вступить в реакцию с 5,6 л ацетилена?
13. Сколько литров ацетилена (при н.у.) можно получить из 1 кг технического карбида кальция, содержащего 20% примесей?
14. Какой максимальный объем водорода (при н.у.) может быть вытеснен натрием из 46 г этилового спирта?
15. Какой объем воздуха необходим для сжигания 11,5 г этилового спирта? Сколько молей оксида углерода (IV) и воды при этом получится?
Задание 4. Напишите уравнения реакций следующих превращений, укажите тип реакции:
1. СН4 → С2Н2 → С6Н6 → С6Н5–NO2
2. CaC2 → C2H2 → CH2=CH → (–CH2–CH–)n
│ │
Cl Cl
3. C2H2 → C6H6 → С6Н5–NO2 → С6H5–NH2
4. СН4 → С2Н2 → CH2=CH2 → (–CH2–CH2–)n
5. С2Н2 → CH2=CH2 → C2H5OH → CH3CO–O–C2H5
6. СН4 → С2Н2 →CH3–CHO → CH3COOH
7. C2H6 → C2H5Br → C2H5OH → CH3–CHO
8. C2H5OH → CH3–CHO → CH3COOH → CH3CO–O–C2H5
9. CH3COOH → ClCH2–COOH→H2N–CH2–COOH → (–NH–CH2–CO–)n
10. (C6H10O5)n → C6H12O6→ C2H5OH → CO2
11. CaC2 → C2H2 → CH3–CHO → (–C6H5–CH2–)n
│
OH
12. C2H6 → C2H5Br → C2H5OH → C2H5–O–C2H5
13. CH3–CHO → C2H5OH → CH2=CH2 → (–CH2–CH2–)n
14. CaC2 → C2H2 → CH3–CHO → CH3COOH
15. C3H8 → C3H7Cl →C3H7OH → CH3–CH=CH2
Тестовые задания для самоконтроля
1. К алифатическим спиртам относится…
1) CH3–CH2–CH2OH,
2) CH3–CH2–CH2–CH3,
3) CH3–CH2–CH2–COOH.
2. Ациклическим аминоспиртом является…
1) CH2OH–CH2–CH2–COOH,
2) CH2OH – CH2– CH2– NH2,
3) CH3–CH2–CH(NH2)–COOH.
3. Правильное название соединения: H2ClC–CH2–C–CH3 -
║
O
1) 4-хлор-бутанол-2,
2) 1-хлор-бутанон-3,
3) 4-хлор-бутанон-2.
4. К диеновым углеводородам относится…
1) CH3–CH=CH–CH2–CH3,
2) CH3–CH=CH–CH=CH2,
3) CH3–C≡C–CH3.
5. Правильное название соединения:CH2=C–CH2–CH3 -
│
CH3
1) 2-метилбутен-1,
2) 3-метилбутен-3,
3) метилбутен.
6. Правильное название соединения:
OH
│
CH3–C–CH2–CH3
│
CH3
1) 2-метилбутанол-3,
2) 2-метилбутанон-2,
3) 2-метилбутанол-2.
7. К нуклеофильным реагентам относится
1) H+,
2) OH–,
3) Cl.
8. К электрофильным реагентам относится
1) H+,
2) CN–,
3) Cl.
9. К радикальным частицам относится…
1) H+,
2) CN–,
3) Cl·.
10. Реакция CH3–CH2–Br + OH– → CH3–CH2–OH + Br– относится к типу реакций…
1) электрофильного замещения,
2) нуклеофильного замещения,
3) нуклеофильного присоединения.
11. Реакция CH3–CH=CH2 + Cl2 → CH3–CHCl–CH2Cl относится к типу реакций…
1) электрофильного присоединения,
2) нуклеофильного присоединения,
3) электрофильного отщепления.
Ключи к тестовым заданиям
| № вопроса | |||||||||||
| № ответа |
Лабораторная работа № 13
Химические свойства органических соединений некоторых классов
Цель работы: изучение химические свойства некоторых органических соединений.
Реактивы: растворы K2Cr2O7, FeCl3, CuSO4, Na2CO3, NaCl, NaOH; H2SO4 (конц.); C6H5OH (р-р), HCOH (р-р), C2H5OH (96%), CH3COOH (конц.), NaHCO3 (сода), мыло, изоамиловый спирт.
Оборудование: пробирки и штатив для них, горелка, держатель, микрошпатель, стеклянная палочка, стеклянные стаканы, водяная баня.
Ход работы
Опыт 1. Окисление спирта в альдегид
Налейте в пробирку 1-2 мл раствора K2Сr2О7, добавьте 5-6 капель H2SO4 (конц.) и прилейте 3-5 капель этилового спирта. Оранжевая окраска раствора изменится на зеленую – цвет ионов Сr3+. При этом спирт окисляется в альдегид, который обнаруживается по его характерному запаху. Напишите уравнение окисления спирта в альдегид.
Опыт 2. Реакция фенола с хлорным железом (качественная реакция на фенол)
Налейте в пробирку 1-2 мл раствора фенола, добавьте 1-2 капли раствора FeCl3. Происходит образование фенолята железа, который окрашивает раствор в фиолетовый цвет. Напишите уравнение реакции.
Опыт 3. Восстановительные свойства альдегидов
Налейте в пробирку 1 мл формалина, прилить 4-5 мл раствора NaOH. Взболтайте содержимое пробирки. Прилейте по каплям раствор CuSO4 до появления осадка Сu(ОН)2. Затем нагрейте пробирку на горелке и наблюдать образование красного осадка закиси меди Сu2О. Напишите уравнение окисления формальдегида в муравьиную кислоту.
Опыт 4. Реакция уксусной кислоты с содой
Налейте в пробирку соды и прилейте уксусную кислоту. Какая протекает реакция, какой газ выделяется? Напишите уравнение реакции.
Опыт 5. Получение карбоновых кислот из мыла
В пробирку налейте наполовину воды и внесите несколько стружек мыла. Для ускорения растворения мыла пробирку нагрейте. К полученному раствору прилейте 1-2 мл раствора H2SO4 и нагрейте пробирку до кипения. В результате реакции на поверхности появляется слой органических кислот, которые после охлаждения затвердевают. Напишите уравнение реакции мыла (C17H35COONa) c H2SO4.
Опыт 6. Получение уксусно-изоамилового эфира
Налейте в пробирку по 2 мл конц. уксусной кислоты, изоамилового спирта и H2SO4 (конц.). Поместите пробирку на несколько минут в водяную баню. Вылейте содержимое пробирки в стакан с раствором NaCl. Ввиду малой растворимости эфира, он всплывает на поверхность. Напишите уравнение реакции.
Глава 14. ПОЛИМЕРЫ
После усвоения материала Главы 14 студент должен:
Знать
• определение полимеров, их классификацию;
• определение полимеризации, механизм радикальной и ионной полимеризации;
• суть процесса поликонденсации;
• различия кристаллических и аморфных полимеров;
• физические и химические свойства синтетических полимеров, их применение;
Уметь
• составлять реакции получения полимеров;
• рассчитать коэффициент полимеризаци;
• решать расчетные задачи по полимерам;
• экспериментально получать некоторые полимеры (плексиглас, новолачную и резольную смолы);
Владеть
• представлениями о строении и способах получения полимеров;
• навыками экспериментального получения некоторых полимеров (плексиглас, новолачная и резольная смолы);
• навыками составления реакций получения полимеров;
• навыками решения расчетные задач по полимерам
Природные полимеры
К природным полимерам, например, относят натуральный каучук, углеводы (крахмал, целлюлозу), белки.
Натуральный каучук
Натуральный каучук получают из млечного сока гевеи, произрастающей в Бразилии. Млечный сок, выделяющийся из надрезов на деревьях, представляет собой коллоидный раствор каучука. Его собирают и подвергают коагуляции действием раствора кислоты или нагреванием. Важнейшими свойствами каучука являются высокая эластичность, газо- и водонепроницаемость.
По химическому составу каучук относится к углеводородам, т.к. в его состав входят только углерод и водород. Термическим разложением каучука установлено, что макромолекулы его состоят из молекул изопрена: СН2=С(СН3)–СН=СН2.
Схематично образование полимера можно представить как последовательное присоединение мономеров:
СН2=С(СН3)–СН=СН2 + СН2=С(СН3)–СН=СН2 →
→ –СН2–С(СН3)=СН–СН2–С(СН3)=СН–СН2–
При этом свободные электроны средних атомов углерода образуют двойные связи в середине звеньев растущей цепи.
Строение макромолекулы каучука выражается формулой:
[–СН2–С(СН3)=СН–СН2–]n.
Макромолекулы имеют линейную структуру, но при этом они свернуты в клубки. При растяжении такие молекулы распрямляются, а образец каучука удлиняется. При снятии нагрузки молекулы возвращаются в прежнее состояние в результате внутреннего теплового движения. Размеры каучука сокращаются.
Натуральный каучук, преимущественно используется в виде резины. Для получения резины каучук подвергают вулканизации с серой и другими добавками. При нагревании атомы серы «сшивают» соседние линейные молекулы каучука по месту некоторых двойных связей. Образуется пространственная структура, обеспечивающая резине более высокую химическую стойкость, стойкость к истиранию, высокие электроизоляционные свойства, более высокую, чем у каучука газо- и водонепроницаемость. Резина не растворяется в бензине как каучук, а только набухает.
При вулканизации каучука с большим количеством серы степень «сшивания» повышается, материал утрачивает эластичность, становится твердым и превращается в эбонит.
Крахмал
Крахмал представляет собой порошок белого цвета, нерастворимый в воде. Он является продуктом фотосинтеза у зеленых растений. Состав крахмала выражается формулой: (С6Н10О5)n, где n может варьироваться от нескольких сотен до нескольких тысяч. Наряду с линейными молекулами имеются молекулы разветвленной структуры.
В кислой среде при нагревании с водой молекулы крахмала подвергаются гидролизу. Сначала при расщеплении молекул крахмала образуются промежуточные продукты – декстрины, затем мальтоза – изомер сахарозы, конечный продукт – глюкоза:
(С6Н10О5)n + nН2О → nС6Н12О6.
Установлено, что макромолекулы крахмала состоят из остатков молекул циклической α-глюкозы.
Крахмал является основным углеводом нашей пищи. В организме он подвергается ферментативному гидролизу. Образующаяся глюкоза поступает в кровь и идет на питание клеток организма. Избыток глюкозы депонируется печенью в виде гликогена, который имеет более разветвленную структуру. Он может превращаться в глюкозу по мере ее расходования.
Промежуточный продукт гидролиза – декстрины образуются в виде корки, при варке и жарке картофеля, выпечке хлеба, при глажении накрахмаленной ткани. Смесь декстринов и глюкозы – патока применяется в кондитерской промышленности для приготовления конфет, мармелада, пряников.
Крахмал злаков и картофеля идет на производство спирта. При этом его сначала подвергают гидролизу под действием фермента, содержащегося в солоде, а затем сбраживают в присутствии дрожжей.
Целлюлоза
Целлюлоза входит в состав растений, образуя оболочки клеток, придавая им прочность и эластичность. Волокна хлопка, льна, конопли представляют собой почти чистую целлюлозу. Из целлюлозы производят хлопчатобумажные ткани, бумагу. В чистом виде целлюлоза – твердое волокнистое вещество, не растворяющееся в воде и других растворителях.
Целлюлоза является природным полимером, молекулы которого состоят из остатков молекул β-глюкозы. Значение n у целлюлозы выше, чем у крахмала. Молекулы целлюлозы имеют только линейную структуру.
При нагревании без доступа воздуха целлюлоза разлагается с образованием воды, древесного угля, метилового спирта, уксусной кислоты, ацетона.
Целлюлоза подвергается гидролизу с образованием глюкозы. Суммарно гидролиз целлюлозы выражается тем же уравнением, что и гидролиз крахмала. Из этой глюкозы получают технический (гидролизный) спирт.
Каждое структурное звено молекулы целлюлозы содержит по три гидроксильных группы [C6H7O2(OH)3]n. За счет этих групп целлюлоза может образовывать простые и сложные эфиры. Так в реакции с азотной кислотой в присутствии серной кислоты образуются нитраты целлюлозы, которые обладают чрезвычайной горючестью.
[C6H7O2(OH)3]n + 3nHNO3 → [C6H7O2(ONO2)3]n + 3nH2O.
Тринитрат целлюлозы – пироксилин – взрывчатое вещество, применяется для производства бездымного пороха.
Уксуснокислые эфиры целлюлозы – диацетат и триацетат используют для приготовления искусственного ацетатного волокна. Для этого целлюлозу, выделенную из древесины или хлопковый пух обрабатывают уксусным ангидридом в присутствии серной кислоты. Продукт этерификации – триацетат целлюлозу растворяют в смеси дихлорметана CH2Cl2 и этилового спирта. Раствор полимера продавливают через фильеры, представляющие собой металлические колпачки с многочисленными отверстиями. Струи раствора опускаются в шахту высотой 3 м, продуваемую нагретым воздухом. Растворитель испаряется, а триацетат целлюлозы образует волокна, которые затем скручивают в нити. При прохождении через отверстия фильеров молекулы ацетата целлюлозы ориентируются вдоль струи раствора, их расположение становится упорядоченным. Это приводит к большой прочности волокон и нитей. Ткани из этого волокна обладают мягкостью, блеском, мало мнутся, хорошо сохраняют тепло, мало садятся при стирке.
Белки
Белки – природные высокомолекулярные азотсодержащие вещества. Молекулярная масса белков выражается десятками и сотнями тысяч, а иногда достигает нескольких миллионов. Они выполняют в организме множество функций. Это пластический материал, из которого построены ткани организма. Белки переносят вещества в организме, например, кислород, углекислый газ. Белки-ферменты катализируют все химические процессы в организме. Белки-антитела защищают организм от инфекций. Образование из белков актина и миозина актомиозина обусловливает сокращение мышечной ткани и т.д.
Гидролизом белков установлено, что они состоят из 20 α-аминокислот. Строение аминокислот, образующих белки, можно представить общей структурной формулой:
R–CH–COOH
│
NH2
В составе радикала могут быть углеводородные цепи, циклы, различные функциональные группы (–SH, –OH, –COOH, –NH2, бензольное кольцо).
Молекулы белка представляют собой длинные цепи остатков аминокислот, соединенных пептидными связями. Группа атомов:
( –С – N – ) – пептидная группа.
║ │
O H
Пептидные связи образуются при взаимодействии карбоксильной группы одной кислоты с аминогруппой другой. Поэтому белки называют еще полипептидами.
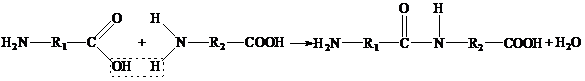
Последовательность чередования различных аминокислотных звеньев в полипептидной цепи называется первичной структурой белковой молекулы.
Полипептидные цепи на значительной своей части свернуты в виде спирали. Эта конфигурация полипептидной цепи называется вторичной структурой белка. Она удерживается за счет многочисленных водородных связей, образованных между группами >С=О и >NH, расположенными на соседних витках спирали.
Третичная структура – это конфигурация, которую принимает в пространстве спираль полипептидной цепи. Ее часто называют глобулой белка. Эта структура поддерживается взаимодействием функциональных групп радикалов аминокислот, составляющих полипептидную цепь. Солевые мостики образуются при сближении карбоксильной и аминогруппы, дисульфидные мостики (–S–S–) образуются между радикалами двух молекул цистеина, сложноэфирные мостики образуются между карбоксильной группой и гидроксилом и т.д. Функциональные группы аминокислот, обращенные наружу глобулы белка, определяют ее специфическую биологическую активность.
Иногда несколько глобул объединяются в более сложную структуру, которую называют четвертичной структурой белка.
Под действием различных факторов, таких как нагревание, действие радиации, сильное встряхивание третичная и вторичная структура белков может разрушаться. Этот процесс называется денатурацией. Денатурированный белок утрачивает биологическую активность.
Существуют белки, молекулы которых не скручиваются в спираль, а имеют вытянутую форму. Такую структуру имеют молекулы белка фибрина, входящего в состав натурального шелка.
Синтетические полимеры
Полимеры – химические соединения, молекулы которых состоят из многократно повторяющихся атомных группировок (элементарных звеньев), соединенных химическими связями в длинные цепи.
Полимеры, синтезированые в лаборатории, имеют молекулярную массу 5 000-200 000 у.е.
Полимеры весьма разнообразны по своему составу, методам получения и свойствам. Это обстоятельство и предопределило быстрое внедрение их в различные области техники, в том числе в автомобилестроение.
Высокая молекулярная масса и гибкость макромолекул определяют специфические физико-химические свойства полимеров, а именно:
· полимеры могут пребывать в характерном только для них высокоэластичном состоянии;
· растворы полимеров имею высокую вязкость, растворению часто
предшествует набухание;
· полимеры нелетучи;
· полимеры могут образовывать волокна, пленки, отличающиеся высокой, анизотропией (не зависимость механических, оптических, электрических и др. свойств веществ от направления).
Полимеры, цепи которых состоят из звеньев различного состава, называются сополимерами. Если в макромолекулах сополимеров чередуются длинные цепочки (блоки) одного химического состава с блоками другого состава, то такие сополимеры называют блоксополимерами.
