Алканы,алкены, алкины и алкадиены
Предельными углеводородами (алканами) называются соединения, состоящие из атомов углерода и водорода, соединенных между собой только σ-связями. В алканах атомы углерода находятся в состоянии sp3-гибридизации.
Алканы: определениек,изомерия и номенклатура
Для предельных углеводородов характерна структурная изомерия. Изомеры этого типа отличаются друг от друга порядком связей между отдельными атомами в молекуле (структурой углеродной цепи).
Как ранее отмечалось, первые четыре члена гомологического ряда предельных углеводородов сохранили тривиальные названия: метан, этан, пропан, бутан. По рациональной номенклатуре алканы называют как производные метана. При выборе основы используют или самый разветвленный атом углерода, или тот, вокруг которого стоят наиболее простые радикалы. По номенклатуре ИЮПАК названия предельных углеводородов характеризуются суффиксом «ан».
 триметилизобутилметан трет-бутилнеопентилметан
триметилизобутилметан трет-бутилнеопентилметан
2,2,4-триметилпентан 2,2,5,5-тетраметилгексан
Способы получения алканов
Главным природным источником предельных углеводородов является нефть, а для первых членов гомологического ряда – природный и попутный газы.
Выделение индивидуальных соединений из нефти или продуктов ее крекинга – задача весьма трудоемкая, поэтому приходится прибегать к синтетическим методам получения.
1. Алканы могут быть получены при восстановлении алкенов или алкинов водородом в присутствии катализаторов. Катализаторами гидрирования и дегидрирования чаще всего используют специальным образом обработанные металлические платину, палладий или никель.
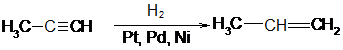
пропин пропен
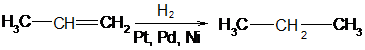
пропен пропан
2. Самые разнообразные производные алканов могут быть восстановлены при высокой температуре восстановителями или водородом на катализаторе. Обычно эта реакция используется для восстановления галогенопроизводных:

иодэтан этан
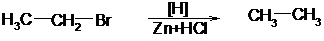
бромистый этил этан
3. Предельные углеводороды образуются при действии воды на металлоорганические соединения:
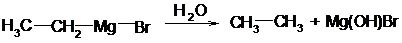
бромистый этилмагний этан
4. В лабораторной практике алканы получают сплавлением солей карбоновых кислот со щелочами:
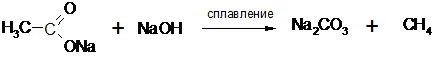
ацетат натрия метан
5. При действии металлического натрия на моногалогенопроизводные (реакция Вюрца):
2 CH3─CH2─J 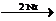 2NaJ + CH3─CH2─CH2─CH3
2NaJ + CH3─CH2─CH2─CH3
иодэтан бутан
Если в реакции Вюрца участвуют два типа галогенопроизводных, то образуется смесь трех различных алканов, так как вероятность встречи в реакционном комплексе молекул одинаковых или разных равна:
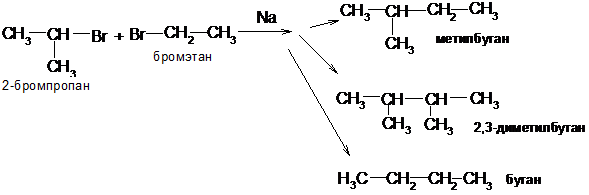
6. Электролиз солей карбоновых кислот (реакция Кольбе):

Анионы кислотного остатка окисляются на аноде с образованием свободных радикалов:
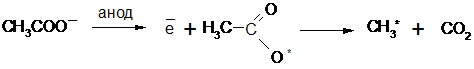
которые объединяются в молекулы предельных углеводородов:
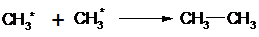
Физические свойства
Согласно теории химического строения А.М.Бутлерова, физические свойства алканов, как и других органических соединений, определяются их составом и строением.
В гомологическом ряду предельных углеводородов четыре первых члена при обычной температуре – газы, далее следуют жидкости и, начиная с С16Н34 – твердые вещества.
Таблица 3.1 - Физические свойства некоторых алканов
| Углеводород | tпл,оС | tкип,оС | Плотность г/см3 | Показатель рефракции |
| Метан СН4 Этан С2Н6 Пропан С3Н8 н-Бутан С4Н10 Изобутан С4Н10 н-Пентан С5Н12 Изопентан С5Н12 Неопентан С5Н12 н-Гексан С6Н14 н-Гептан С7Н16 н-Октан С8Н18 Изооктан (2,2,4-триметилпентан) н-Нонан С9Н20 н-Декан С10Н22 н-Пентадекан С15Н32 н-Эйкозан С20Н42 н-Гектан С100Н202 | -182,5 -182,8 -187,6 -138,3 -159,4 -129,8 -159.9 -16,6 -95,3 -90,6 -56,8 -107,4 -53.6 -29,7 10,0 36,4 115,2 | -161,6 -88,6 -42,1 -0,5 -11,7 36,0 27,9 9,5 68,7 98,5 125,7 99,2 150,8 174,0 270,5 205,0 (2кПа) - | 0,4161 0,5461 0,5082 0,5842 0,5632 0,563 0,626 0,613 0,660 0,684 0,703 0,692 0,718 0,730 0,765 0,777при tпл - | - - 1,33781 1,3326 - 1,3575 1,3537 1,3513 1,3749 1,3838 1,3974 1,3915 1,4056 1,4120 1,4313 - - |
1.При температуре кипения
2. В жидком состоянии под давлением
Алканы – вещества неполярные и труднополяризуемые. Растворимость их в воде ничтожна. Атомы в молекулах предельных углеводородов соединены только σ-связями. Расстояния между соседними углеродными атомами 0,154 нм. В коротких цепях по С-С связям возможно свободное или почти свободное вращение.
Алканы поглощают ультрафиолетовое излучение в области длин волн менее 200 нм (они бесцветны). В ИК спектрах для них характерны полосы в области 2800 – 3000 см–1 (валентные колебания связи С-Н) 1380 -1470 см–1 (деформационные колебания той же связи). Полосы поглощения, отвечающие колебаниям связи С-С, мало интенсивны и трудно идентифицируются.
ЯМР-спектры алканов трудно расшифровываются, так как химические сдвиги различным образом расположенных протонов имеют близкие значения (около 0,5 – 2 м.д.)
Химические свойства
Химические превращения предельных углеводородов могут происходить либо за счет разрыва цепи углеродных атомов, либо за счет отрыва атомов водорода с последующим замещением их другими атомами или группами. Поэтому для предельных углеводородов характерны реакции расщепления и замещения.
Процессы расщепления связей С-С или С-Н с образованием свободных радикалов требуют большой энергии активации и поэтому при обычной температуре идут только в присутствии катализаторов.
Место вступления заместителя в молекулу алкана определяется в первую очередь вероятностью образования того или иного радикала, т.е. прочностью связей водородного атома с углеродом и стабильностью возникающего радикала.
Радикальное галогенирование
Замещение водородных атомов на галоген – одна из наиболее характерных реакций предельных углеводородов. С F2 реакция идет со взрывом, а с J2 – процесс ограничен равновесием, т.к. йодистый водород восстанавливает образующиеся йодистые алкилы. Следовательно, скорость галогенирования с одной стороны зависит от природы галогена (F>>Cl>Br>J), а с другой от строения углеводорода. Общеизвестно, что легче всего галогенирование протекает по третичному углеродному атому, а труднее всего – по первичному.
Галогеном можно заместить как один атом водорода в молекуле, так и все.
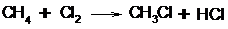
хлористый метил
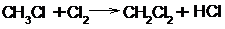
хлористый метилен
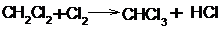
Хлороформ

четыреххлористый углерод
Галогенирование алканов на свету или под действием высоких температур протекает по цепному радикальному механизму и является типичным примером радикального замещения (SR).
СН4 + Br2 → СН3Br + НBr
На первой стадии под влиянием света происходит гомолитический разрыв связи в молекуле брома и она распадается на два радикала:
Br2 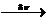 2 Br*
2 Br*
Атом или молекула подобного типа, содержащие неспаренный электрон, называются свободными радикалами и, как правило, существуют лишь доли секунды, так как мгновенно реагируют с присутствующими веществами.
Поэтому на следующей стадии реакции радикал Br• атакует молекулу метана, образуя бромистый водород и углеводородный радикал – метил:
СН4 + Br* → НBr + СН3*
Образовавшийся органический радикал атакует молекулу брома и регенерирует радикал галогена:
СН3* + Br2 → СН3Br + Br*
Этот процесс может продолжаться бесконечно долго, но на практике течение цепных реакций ограничивается так называемыми процессами обрыва цепи, при которых радикалы, реагируя один с другим, выбывают из процесса:
Br• + Br• → Br2
CH3• + Br• → CH3Br
CH3• + CH3• → CH3-CH3
Кроме того, они могут взаимодействовать с примесями или со стенками сосуда.
Нитрование
Концентрированная азотная кислота при обычной температуре почти не действует на предельные углеводороды, а при нагревании действует как окислитель. М. И. Коновалов предложил проводить нитрование предельных углеводородов разбавленной азотной кислотой при нагревании (около 140 оС). По механизму реакция нитрования является свободно радикальным процессом:
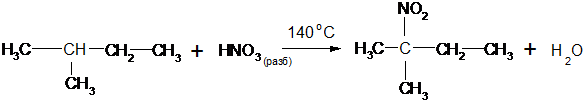
2-метил-2-нитробутан
В случае разветвленной молекулы алкана легче всего замещается водород у третичного углеродного атома. В промышленных условиях нитрование осуществляют оксидами азота.
