Электронные представления в органической химии
Применение электронной теории строения атома и химической связи в органической химии явилось одним из важнейших этапов развития теории строения органических соединений. Понятие о химическом строении как последовательности связей между атомами (А.М. Бутлеров) электронная теория дополнила представлениями об электронном и пространственном строении и их влиянии на свойства органических соединений. Именно эти представления дают возможность понять способы передачи взаимного влияния атомов в молекулах (электронные и пространственные эффекты) и поведение молекул в химических реакциях.
Согласно современным представлениям свойства органических соединений определяются:
· природой и электронным строением атомов;
· типом атомных орбиталей и характером их взаимодействия;
· типом химических связей;
· химическим, электронным и пространственным строением молекул.
Свойства электрона
Электрон имеет двойственную природу. В разных экспериментах он может проявлять свойства как частицы, так и волны. Движение электрона подчиняется законам квантовой механики.
Связь между волновыми и корпускулярными свойствами электрона отражает соотношение де Бройля:
…………………………..
- длина волны электрона; m - его масса; v - скорость;lгде
h = 6.62 • 10-34 Дж • с - постоянная Планка.
Энергию и координаты электрона, как и других элементарных частиц, невозможно одновременно измерить с одинаковой точностью (принцип неопределенностиГейзенберга). Поэтому движение электрона в атоме или в молекуле нельзя описать с помощью траектории. Электрон может находиться в любой точке пространства, но с разной вероятностью.
Часть пространства, в котором велика вероятность нахождения электрона, называют орбиталью или электронным облаком.
Например:
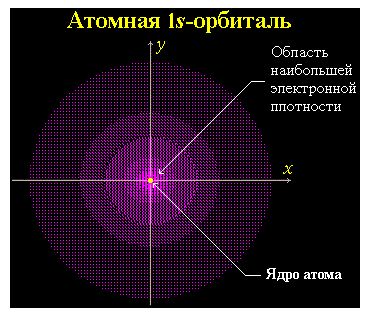
Атомные орбитали
Атомная орбиталь (АО) - область наиболее вероятного пребывания электрона (электронное облако) в электрическом поле ядра атома.
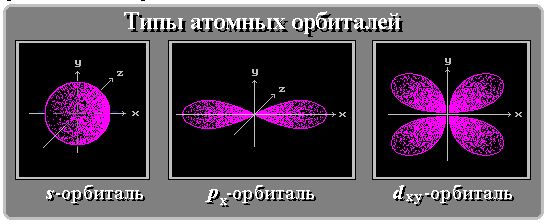
Положение элемента в Периодической системе определяет тип орбиталей его атомов (s-, p-, d-, f-АО и т.д.), различающихся энергией, формой, размерами и пространственной направленностью.
Для элементов 1-го периода (Н, He) характерна одна АО - 1s.
В элементах 2-го периода электроны занимают пять АО на двух энергетических уровнях: первый уровень 1s; второй уровень - 2s, 2px, 2py, 2pz. (цифры обозначают номер энергетического уровня, буквы - форму орбитали).
Состояние электрона в атоме полностью описывают квантовые числа.
Форма и энергия атомных орбиталей
Атомные орбитали (АО) разных типов отличаются друг от друга формой и энергией и обозначаются символами: s, p, d, f и т.д.
Органические вещества состоят в основном из элементов 2-го и 3-го периодов, валентные электроны которых находятся на s- и р-АО.
Атомные орбитали s-типа имеют форму сферы:

Вопрос
Предельные углеводороды - это углеводороды, в молекулах которых имеются только простые (одинарные) связи (  -связи). Предельными углеводородами являются алканы и циклоалканы.
-связи). Предельными углеводородами являются алканы и циклоалканы.
Атомы углерода в предельных углеводородах находятся в состоянии sp3-гибридизации.
Алканы - предельные углеводороды, состав которых выражается общей формулой CnH2n+2. Алканы являются насыщенными углеводородами.
Физические свойства алканов
При комнатной температуре С1-C4 - газы, C5-C15 - жидкости, C16 и следующие - твердые вещества; нерастворимы в воде; плотность меньше 1 г/см3; жидкие - с запахом бензина.
С увеличением числа атомов углерода в молекуле возрастает температура кипения.
Химические свойства алканов
Малоактивны в обычных условиях, не реагируют с растворами кислот и щелочей, не обесцвечивают раствор KMnO4 и бромную воду.
1. Горение (окисление с разрывом связей C—C и C—H): CH4 + 2O2  CO2 + 2H2O + Q
CO2 + 2H2O + Q
2. Замещение (с разрывом связей C—H):
а) галогенирование (только с хлором и с бромом):
1-я стадия: CH4 + Cl2  CH3Cl + HCl (при нагревании или на свету).
CH3Cl + HCl (при нагревании или на свету).
При достаточном количестве галогена происходит дальнейшее замещение атомов водорода:
| CH3Cl хлорметан | + Cl2 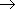 | CH2Cl2 дихлорметан | + HCl, |
CH2Cl2 + Cl2 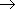 | CHCl3 трихлорметан | + HCl, |
CHCl3 + Cl2 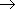 | CCl4 тетрахлорметан | + HCl. |
б) нитрование (реакция Коновалова):
CH4 + HONO2 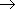 | CH3NO2 нитрометан | + H2O (при нагревании) |
Получение алканов
Лабораторные способы:
1. Гидролиз карбида алюминия (получение метана): Al4C3 + 12H2O 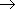 4Al(OH)3 + 3CH4
4Al(OH)3 + 3CH4 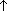
2. Реакция обмена: CH3COONa + NaOH 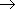 Na2CO3 + CH4
Na2CO3 + CH4 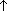 (при нагревании)
(при нагревании)
3. Реакция Вюрца: 2CH3Cl + 2Na 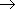 CH3—CH3 + 2NaCl
CH3—CH3 + 2NaCl
Промышленные способы:
1. Выделение из природных источников (природного газа, нефти, каменного угля, горючих сланцев).
2. Газификация твердого топлива: C + 2H2 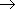 CH4 (при нагревании под давлением в присутствии Ni-катализатора)
CH4 (при нагревании под давлением в присутствии Ni-катализатора)
Циклоалканы - предельные углеводороды, состав которых выражается формулой CnH2n. В состав молекул циклоалканов входят замкнутые углеродные цепи (циклы).
Изомеры и гомологи
Упрощенно углеводородный цикл часто изображают правильным многоугольником с соответствующим числом углов.
Физические свойства мало отличаются от свойств алканов.
Химические свойства
За исключением циклопропана и циклобутана циклоалканы, как и алканы, малоактивны в обычных условиях.
Общие свойства циклоалканов (на примере циклогексана):
1. горение (окисление с разрывом связей C—C и C—H):
C6H12 + 9O2 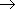 6CO2 + 6H2O + Q
6CO2 + 6H2O + Q
2. замещение (галогенирование, нитрование):
C6H12 + Cl2 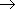 C6H11Cl + HCl (при нагревании или на свету)
C6H11Cl + HCl (при нагревании или на свету)
3. присоединение (гидрирование):
C6H12 + H2 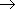 C6H14 (при нагревании под давлением в присутствии Ni-катализатора)
C6H14 (при нагревании под давлением в присутствии Ni-катализатора)
4. разложение (дегидрирование, крекинг, пиролиз):
C6H12 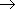 C6H6 + 3H2 (при нагревании с катализатором).
C6H6 + 3H2 (при нагревании с катализатором).
Особые свойства циклопропана и циклобутана (склонность к реакциям присоединения):
1. галогенирование:
 + Br2
+ Br2 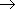 BrCH2—CH2—CH2Br
BrCH2—CH2—CH2Br
2. гидрогалогенирование:
 + HBr
+ HBr 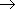 CH3—CH2—CH2Br
CH3—CH2—CH2Br
