Определить, образуется ли осадок хлорида свинца (II), если к 0,05 М раствору нитрата свинца (II) добавить равный объем 0,02 М раствора хлороводородной кислоты.
Дано: с 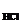 = 0,02 M с = 0,02 M с  = 0,05 M = 0,05 M 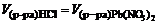 | Решение При сливании растворов протекает следующая реакция: Pb(NO3)2 + 2HCl = PbCl2 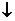 + 2HNO3. Осадок PbCl2 образуется только в случае, если + 2HNO3. Осадок PbCl2 образуется только в случае, если |
| Образуется ли осадок – ? |
с 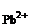 · с
· с 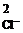 > ПР
> ПР 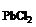 = 2·10
= 2·10 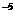 (таблица).
(таблица).
С учетом увеличения объема раствора при сливании в 2 раза:
с 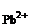 =
= 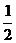 с
с  ·
· 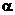 ·n
·n 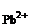 =
= 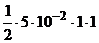 = 2,5·10-2 моль/л;
= 2,5·10-2 моль/л;
с 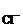 =
= 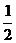 с
с 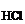 ·
· 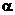 ·n
·n 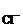 =
= 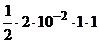 = 1·10-2 моль/л;
= 1·10-2 моль/л;
с 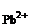 ·с
·с 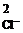 = 2,5·10
= 2,5·10 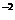 ·(1·10
·(1·10 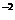 )2 = 2,5·10
)2 = 2,5·10 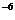 .
.
Так как 2,5·10 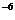 < 2·10-5 (ПР
< 2·10-5 (ПР 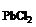 ), то осадок PbCl2 не образуется.
), то осадок PbCl2 не образуется.
Ответ: осадок PbCl2 не образуется .
3. Составить схему коррозионного ГЭ, возникающего при контакте оловянной пластинки площадью 35 см2 с медной в растворе соляной кислоты. Написать уравнения электродных процессов и суммарной реакции процесса коррозии.
а) Вычислить объемный и весовой показатели коррозии, если за 70 мин в процессе коррозии выделилось 1,5 см3 газа (н.у.).
б) Вычислить весовой и глубинный показатели коррозии, если за 80 мин потеря массы корродируемого металла составила 5,6 ∙10-3 г. Плотность металла 7,3 г/см3.
Решение
По таблице находим значения стандартных электродных потенциалов олова (II) и меди (II):
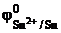 = – 0,14 В,
= – 0,14 В, 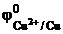 = 0,34 В.
= 0,34 В.
Так как 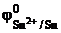 <
< 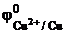 , то анодом в коррозионном ГЭ будет олово, катодом – медь.
, то анодом в коррозионном ГЭ будет олово, катодом – медь.
Составим схему коррозионного ГЭ:
А(-)Sn │ HCl │ Cu(+)K
или
А(-)Sn │ H+ │ Cu(+)K
Cоставляем уравнения электродных процессов и суммарной реакции процесса коррозии:
На A(-)Sn – 2ē = Sn2+
На К(+)2Н+ + 2ē = Н2
 |
Sn + 2H+ = Sn2+ + H2
Sn + 2HCl = SnCl2 + H2 – суммарная реакция процесса коррозии.
а) Рассчитываем объемный показатель коррозии (KV) по формуле
| Дано: τ = 70 мин Vгаза = 1,5см3 S = 35 см 2 | KV =  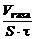 , см3/м2∙час. При расчете KV принимаем: S – площадь поверхности анода, м2; τ – время процесса коррозии, ч; Vгаза – объем выделившегося газа, см3. , см3/м2∙час. При расчете KV принимаем: S – площадь поверхности анода, м2; τ – время процесса коррозии, ч; Vгаза – объем выделившегося газа, см3. |
| KV –? Km – ? |
Из уравнения суммарной реакции процесса коррозии следует, что при коррозии выделяется водород. Следовательно, Vгаза = 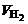 .
.
Тогда
KV = 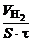 =
= 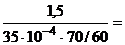 367,3 см3/м2∙ч.
367,3 см3/м2∙ч.
Рассчитываем весовой показатель коррозии Km по формуле
Km = 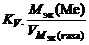 , г/м2∙ч.
, г/м2∙ч.
В процессе коррозии разрушению подвергается олово и выделяется водород.
Следовательно:
Мэк(Ме) = Мэк(Sn) = 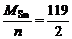 = 59,5 г/моль,
= 59,5 г/моль,
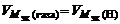 = 11200 см3/моль.
= 11200 см3/моль.
Km = 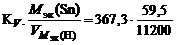 = 1,95 г/м2∙ч.
= 1,95 г/м2∙ч.
Ответ: KV = 367,3 см3/м2∙ч.
Km = 1,95 г/м2∙ч.
б) Рассчитываем весовой показатель коррозии Km по формуле
Дано: τ = 80 мин 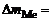 5,6∙10-3 г S = 35 см 2 ρMe = 7,3 г/см3 5,6∙10-3 г S = 35 см 2 ρMe = 7,3 г/см3 | Km =  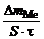 , г/м2∙ч. Коррозии подвергается олово. Тогда потеря массы металла , г/м2∙ч. Коррозии подвергается олово. Тогда потеря массы металла 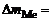 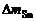 . . |
| Km – ? П – ? |
При расчете Km принимаем
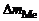 – г; S – м2, τ – ч.
– г; S – м2, τ – ч.
Тогда
Km = 
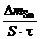 =
= 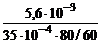 = 1,2 г/м2∙ч.
= 1,2 г/м2∙ч.
Рассчитываем глубинный показатель коррозии по формуле
П = 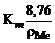 =
= 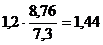 мм/год.
мм/год.
Ответ: Km = 1,2 г/м2∙ч, П = 1,44 мм/год.
МЕТАЛЛЫ V–VI ГРУППЫ
УРОВЕНЬ А
1. Определить степень окисления всех элементов в соединениях WO2, WBr5, (NH4)2WO4.
Ответ:
+4 -2 +5-1 -3+1 +6-2
WO2, WBr5, (NH4)2WO4
Как изменяются кислотно-основные свойства гидроксидов хрома с увеличением его степени окисления в ряду
Сr+2, Сr+3, Сr+6?

 Ответ: В указанном ряду с увеличением степени окисления хрома кислотные свойства гидроксидов усиливаются, а основные свойства ослабевают: (Cr(OH)2 Сr(OH)3 H2CrO4).
Ответ: В указанном ряду с увеличением степени окисления хрома кислотные свойства гидроксидов усиливаются, а основные свойства ослабевают: (Cr(OH)2 Сr(OH)3 H2CrO4).
основание HCrO2 кислота
амфотер. гидроксид
Написать сокращенную электронную формулу атомов вольфрама, ванадия и ниобия и указать расположение валентных электронов по подуровням.
Ответ:
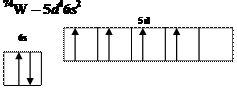
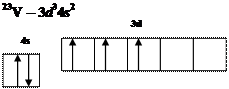
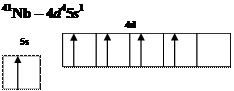
УРОВЕНЬ В
1. Можно ли восстановить оксид хрома (III) до металла при стандартных условиях:
а) цинком;
б) кремнием.
Ответ подтвердить расчетом ΔrGo(298 K) по ΔfGo(298 K, B).
| Дано: Cr2O3(к) Zn(к) Si(к) | Решение а) Составляем уравнение реакции и рассчитываем изменение стандартной энергии Гиббса ΔrGº(298 K) реакции, используя I следствие из закона Гесса. Значения стандартных энергий Гиббса образования веществ ΔfGº (298 K,B) берем из таблицы. |
| Cr – ? |
Cr2O3(к) + 3Zn(к) = 2Сr(к) + 3ZnO(к),
ΔfGº(298 K) – 1058,97 0 0 3(-320,7)
кДж/моль
ΔrGº(298 K) = [3ΔfGº(298 K, ZnO(к)) + 2ΔfGº(298 K, Сr(к))] –
– [ΔfGº(298 K, Cr2O3(к)) + 3ΔfGº(298 K, Zn(к))] =
= 3(–320,7) – (–1058,97) = 96,87 кДж.
Так как ΔrGº(298 K) > 0, то при стандартных условиях реакция невозможна.
б) Аналогично
2Cr2O3(к) + 3Si(к) = 4Сr(к) + 3SiО2(к)
ΔfGº(298K) 2(–1058,97) 0 0 3(-856,7)
кДж/моль
ΔrGº(298 K) = [3ΔfGº(298 K, SiO2(к)) + 4ΔfGº(298 K, Cr(к))] –
– [2ΔfGº(298 K, Cr2O3(к)) + 3ΔfGº(298 K, Si(к))] =
= 3(–856,7) – 2(–1058,97) = –452,16 кДж.
Так как ΔrGº(298 K) < 0, то самопроизвольное протекание реакции при стандартных условиях возможно.
Ответ: при стандартных условиях возможно восстановление хрома из оксида хрома (III) только кремнием.
2. Определить рН раствора, при котором установилось равновесие: 2CrO 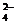 + 2H+ <=> Cr2O
+ 2H+ <=> Cr2O 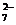 + H2O. Равновесные концентрации ионов Cr2O
+ H2O. Равновесные концентрации ионов Cr2O 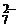 и CrO
и CrO 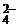 соответственно равны 4,5 и
соответственно равны 4,5 и
0,001 моль/л. Константа равновесия Кс = 1,1·1018.
Дано: [Cr2O 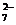 ] = 4,5 моль/л [CrO ] = 4,5 моль/л [CrO 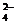 ] = 0,001 моль/л Кс = 1,1·1018 ] = 0,001 моль/л Кс = 1,1·1018 | Решение 2CrO 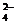 + 2H+ <=> Cr2O + 2H+ <=> Cr2O 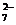 + H2O рН = -lg[H+] Kc = + H2O рН = -lg[H+] Kc = 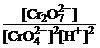 ; ; |
| рН – ? |
[H+] = 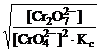 =
= 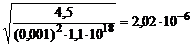 .
.
рН = -lg2,02·10-6 = 5,7.
Ответ: рН = 5,7.
3. Шестивалентный элемент образует оксид, содержащий 20,71 % мас. кислорода. Вычислить молярную массу эквивалента элемента и назвать элемент.
Дано: 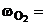 20,71 % мас. В = 6 20,71 % мас. В = 6 | Решение По закону эквивалентов: nэк(О2) = nэк(Э);  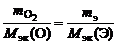 ; ; |
| Мэк(Э) – ? Э – ? |
Мэк(О) = 8 г/моль;
Мэк(Э) = 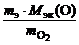 ;
;
mокс = mэ + 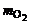 ;
;
mэ = 100 – 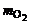 = 100 – 20,71 = 79,29 г.
= 100 – 20,71 = 79,29 г.
Мэк(Э) = 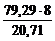 = 30,63 г/моль; Мэк(Э) =
= 30,63 г/моль; Мэк(Э) = 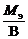 ,
,
где В – валентность элемента.
Мэ = Мэк(Э)∙В = 30,63∙6 = 183,77 г/моль, что соответствует молекулярной массе атома вольфрама .
Ответ: Мэк(Э) = 30,63 г/моль; элемент – W.
УРОВЕНЬ С
Уравнять реакцию
Cr(NO3)3 + Br2 + KOH → K2CrO4 + KBr + KNO3 + H2O ,
