Обратимые реакции. Химическое равновесие
Обратимые и необратимые химические процессы. Химическое и фазовое равновесии. Факторы, воздействующие на химическое равновесие. Методы управления технологическими процессами, основанные на изменении скорости химических реакций и смещении химического равновесия.
Реакция, протекающая до конца, то есть до полного израсходования одного из реагирующих веществ называется необратимой.
Например: взаимодействие алюминия с соляной кислотой идет необратимо. Обратный процесс взаимодействия хлорида алюминия и водорода с получением алюминия и соляной кислоты невозможен.
Однако большинство химических реакций протекает не до конца, когда ни одно из исходных веществ не расходуется полностью. Такие реакции называются обратимыми.
В уравнениях обратимых реакций вместо знака равенства обычно ставят разнонаправленные стрелки, которые характеризуют одновременное протекание процессов в двух взаимно противоположных направлениях:
H2 + I2 ↔ 2 HI
Согласно закону действующих масс скорость прямой реакции выражается уравнением:
v1 = k1 [ H2 ]∙ [I2],
а скорость обратной реакции — уравнением
v2 = k2 [ HI ]2
В начальный момент времени скорость синтеза HI максимальна, поскольку максимальна концентрация H2 и I2), а скорость разложения HI равна нулю, так как в системе отсутствует HI. По мере расходования водорода и иода скорость прямой реакции постепенно уменьшается, а скорость обратной, напротив, возрастает в соответствии с накоплением в реакционном объеме HI. Рано или поздно наступит такой момент, когда эти скорости станут одинаковыми: v1 = v2 и кривые скоростей сольются в горизонтальную прямую (см. рис.5). Подобное состояние системы называется химическим равновесием.
Начиная с этого момента времени, скорости v1 и v2 остаются неизменными, а значит:
k1 [ H2 ] [I2] = k2 [ HI ]2
откуда:
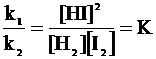
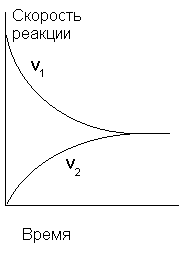 |
Рис.5. Изменение во времени скоростей прямой и обратной реакций
Отношение констант скоростей при данной температуре является также константой, называемой константой равновесия К.
Концентрации веществ, которые устанавливаются при равновесии называют равновесными концентрациями. Пока сохраняется равновесие эти концентрации остаются неизменными.
Но состояние химического равновесия не означает прекращения химических реакций. В состоянии химического равновесия взаимодействие исходных веществ и разложение продуктов реакции продолжаются с одинаковыми скоростями. Поэтому такое равновесие называется динамическим.
Для реакции общего вида:
аА +bB ↔ cC+dD
константа равновесия определяется равенством:
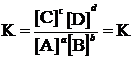
A, B, C, D – формулы веществ, а a, b, c, d – стехиометрические коэффициенты.
Константа равновесия зависит только от природы реакции и от температуры, но не зависит от механизма реакции, поэтому:
1. В уравнении константы равновесия показатели степеней, в которые возводятся концентрации участвующих в реакции веществ, всегда совпадают с коэффициентами в уравнении химической реакции.
2. Введение катализатора не изменяет константы равновесия, а только ускоряет наступление равновесия. Катализатор в одинаковой мере изменяет энергию активации прямой и обратной реакций. Поэтому отношение констант скорости прямой и обратной реакций, т.е. константа равновесия остается неизменным.
Смещение химического равновесия
Состояние химического равновесия в системе поддерживается до тех пор, пока сохраняются постоянными параметры состояния системы: концентрации компонентов, давление, температура. При изменении какого-либо из параметров состояния вследствие взаимодействия системы с внешней средой равновесие нарушится, а затем в ней установится другое равновесие с новыми значениями равновесных концентраций веществ.
Процесс изменения концентраций, обусловленный нарушением равновесия, называется смещением или сдвигом равновесия.
Направление сдвига равновесия в общем виде определяется принципом Ле Шателье (1884):
если находящаяся в равновесии система подвергается внешнему воздействию, то равновесие смещается в сторону ослабления этого воздействия или противодействия ему.
Так, понижение температуры смещает равновесие в направлении процессов, сопровождающихся выделением теплоты, а повышение температуры действует в противоположном направлении. Если в равновесную систему ввести дополнительное количество какого-либо вещества, то равновесие сместится в направлении соответствующем уменьшению концентрации введенного вещества.
Например, добавление хлорида железа (III) в раствор, где установилось химическое равновесие:
FeCl3 + 3 KCNS ↔ Fe(CNS)3 + 3KC1
сдвинет равновесие вправо, что заметно по усилению интенсивности окраски раствора (роданид железа (III) имеет кроваво-красную окраску).
Обратимая реакция: 2NO + O2↔2NO2 при протекании в смеси газов в прямом направлении сопровождается уменьшением числа молекул и, следовательно, уменьшением давления при постоянном объеме реактора (реакционного сосуда) и постоянной температуре. Протекание реакции в обратном направлении сопровождается, напротив, увеличением и числа молекул, и давления внутри реактора.
Поэтому в соответствии с принципом Ле Шателье уменьшение давления вызовет смещение равновесия в сторону исходных веществ (NO и О2). И наоборот, повышение давления сместит равновесие в сторону продукта реакции (NO2).
Приведенные рассуждения применимы лишь к реакциям с участием газообразных компонентов. Если же ни один из компонентов не является газообразным, то положение равновесия при изменении давления не изменяется.
Движущая сила химических процессов
Многие химические реакции при заданных условиях самопроизвольно протекают только в определенных направлениях. Например, реакция взаимодействия оксида кальция и воды
СаО + H2O = Са(ОН)2 - 66,7 кДж
при комнатной температуре происходит лишь в прямом направлении, однако при более высоких температурах она может протекать и в обратном.
Что же является причиной или, как принято говорить, движущей силой химических процессов?
В серединеXIX в. французский химик Марселен Бертло и датский химик Юлиус Томсен сформулировали правило:
химические процессы могут протекать самопроизвольно только в том случае, если они сопровождаются выделением теплоты, т.е. уменьшением внутренней энергии системы.
Бертло и Томсен исходили из аналогии в поведении механических и химических систем. Так, в механической системе шарик, помещенный на наклонную плоскость, склонен к самопроизвольному скатыванию вниз, переходяизположения с большим в положение с меньшим уровнем потенциальной энергии. Обратное перемещение шарика возможно только при затрате энергии извне. Подобно этому и химические процессы, по мнению Бертло и Томсена, должны самопроизвольно протекать в направлении уменьшения внутренней энергии системы, т.е. с выделением теплоты.
Но оказалось, что существует немало процессов, в которых теплота поглощается. Например, при растворении нитратов натрия и аммония наблюдается сильное охлаждение раствора.
Смешение газов происходит самопроизвольно, но без изменения энергетического состояния системы. Обратный ему процесс самопроизвольно не идет.
Причину прохождения такого рода процессов удалось объяснить с позиций понятия порядка и беспорядка системы. Распределение молекул газов в состоянии, когда они разделены перегородкой, отличается большим порядком. Степень порядка распределения молекул газов в состоянии, когда они смешаны меньше. Следовательно, движущей силой смешения газов является стремление их перейти в состояние с меньшим порядком.
Таким образом, существует еще один критерий самопроизвольности процессов - уменьшение степени упорядоченности системы. С точки зрения теории вероятности этот критерий выражается так: все процессы направлены к наиболее вероятному состоянию системы.
Энтропия
За меру вероятности (беспорядка) состояния системы принята логарифмическая функция которую называют энтропия:
S == k In W, в данном соотношении k=R/NA, где: R —универсальная газовая постоянная, 8,31 Дж/моль∙К; NА — постоянная Авогадро, 6,02∙1023 1/моль; W — вероятность состояния системы (безразмерная величина), т.е. число микросостояний, посредством которых осуществляется данное макросостояние .
Все то, что увеличивает беспорядок в расположении частиц способствует возрастанию энтропии. Свобода движения молекул в газообразном состоянии больше и, следовательно, движение более беспорядочное, чем в жидком или твердом состояниях. Поэтому энтропия возрастает при плавлении кристаллов или их растворении и особенно резко — при переходе вещества в газообразное состояние.
Если одно и то же вещество образует несколько разновидностей, то энтропия его тем меньше, чем тверже вещество. Более прочная решетка алмаза ограничивает беспорядок в расположении атомов углерода в отличие от слоистой решетки графита. Поэтому энтропия алмаза мала (2,4 Дж/(мольК), а графита вдвое выше (5,7 Дж(мольК)).
Энтропия меняется и при протекании химических процессов. В случае газовых реакций: при увеличении числа молекул газов энтропия возрастает, а при уменьшенииихчисла — падает.
Суммируя все сказанное, можно прийти к выводу, что:
направленность процессов обусловлена одновременным взаимодействием двух факторов: стремлением системы перейти в состояние с наименьшей внутренней энергией (энтальпией) и стремлением ее достичь наиболее вероятного состояния.
Равнодействующую этих факторов можно выразить количественно — с помощью термодинамической функции, называемой энергией Гиббса.
Энергия Гиббса и ее изменение при химических процессах
Рассмотрим экзотермическую реакцию:
СО + 2Н2=> СН3ОН - 93,5 кДж
Действие энтальпийного фактора обусловливает ее протекание в прямом направлении.
∆H <0 (процесс экзотермический)
Однако наибольшее значение энтропии достигается при полном разложении метанола на водород и оксид углерода, так как при этом число молекул газов возрастает втрое.
Вычислим изменение энтропии системы при прямой реакции.
Изменение энтропии в ходе химической реакции ( ΔS) равно сумме энтропий продуктов за вычетом суммы энтропии исходных веществ.
Таблица 3. Стандартные энтропии веществ-участников реакции
| Вещество | Стандартная энтропия, S0 Дж/моль·K |
| CO (газ) | 197,5 |
| H2(газ) | 130,5 |
| CH3OH (газ) | 240,1 |
ΔS° = 240,1 Дж/моль·K· 1 моль —(197,5 Дж/моль·K· 1 моль + 130,5 Дж/моль·K· 2 моль) = -218,4 Дж/К.
Отсюда, при синтезе метанола энтропия уменьшается.
Таким образом энтальпийный и энропийный факторы действуют в противоположных направлениях.
Для того чтобы учесть действие обоих факторов в термодинамике используется функция состояния системы - энергия Гиббса (G). Она применяется для изобарно-изотермических условий и связана с энтальпией и энтропией простым соотношением:
G = H - TS.
Изменение энергии Гиббса в ходе химической реакции:
∆G = ∆H - T∆S
Характер этого изменения позволяет судить о принципиальной возможности или невозможности осуществления процесса.
При постоянных давлении и температуре самопроизвольно протекают только такие химические реакции, которые сопровождаются уменьшением энергии Гиббса.
Иными словами, ∆G < 0 (т.е. энергия Гиббса системы в исходном состоянии больше, чем в конечном) свидетельствует о возможности самопроизвольного осуществления реакции. Если же ∆G > 0, то процесс не может идти в данных условиях.
Используя известные значения стандартных энтальпий образования и стандартных энтропии веществ, можно прогнозировать возможность протекания химической реакции при той или иной температуре.
Под стандартной энергией Гиббса образования понимают изменение энергии Гиббса при реакции образования 1 моль данного соединения из простых веществ. Подобно энтальпии и энтропии:
стандартное изменение энергии Гиббса в ходе химической реакции равно сумме стандартных энергий Гиббса образования продуктов реакции за вычетом суммы стандартных энергий Гиббса образования исходных веществ.
Пользуясь табличными данными можно рассчитать изменение энергии Гиббсав стандартных условиях.
Рассмотрим обратимую реакцию:
N2 (г) +ЗН2 (г) ↔ 2NH3(г) .
Для стандартных условий ∆H° = - 92,4кДж ∆S°= -0,1978 кДж/К
Изменение энергии Гиббса:
∆G0 = ∆H0 - T∆S0 = -92,4 - (0,198 ∙ 298) = 92,4 + 59,0 = -33,4 кДж.
Итак, при стандартных условиях реакция протекает в прямом направлении, хотя она сопровождается уменьшением энтропии (превалирует энтальпийный фактор). Обратная реакция — разложение аммиака на водород и азот — в этих условиях термодинамически (принципиально) невозможна.
Однако по мере повышения температуры все более существенным становится влияние энтропийного фактора.
∆G500 = 6,6 кДж,
∆G800 = 66,0 кДж.
В случае обратной реакции ∆G имеют, естественно, противоположные знаки. Уже при 500К становится принципиально возможным разложение аммиака. При 800К эта возможность возрастает.
Когда действия энтальпийного и энтропийного факторов уравновешивают друг друга, т.е. ∆G=0, наступает состояние химического равновесия. В этом случае скорость прямой реакции равна скорости обратной.
Константа химического равновесия связана с изменением энергии Гиббса уравнением: ΔGреак. = -RT In К
Изменение энергии Гиббса определяет лишь возможность протекания химических реакций. В конкретных условиях скорость протекания реакции может быть бесконечно мала. Это обусловлено барьером энергии активации, при нагревании или освещении солнечным светом реакция немедленно произойдет.
Тема 1.2. Реакционная способность веществ
Основные законы химии
Основные стехиометрические законы. Методы расчета материального баланса химических процессов и технологии.
1. Закон сохранения массы веществ:
Масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции. (М. В. Ломоносов, А.Л. Лавуазье, 1748—1756 гг.).
В производстве на его основе ведутся расчеты материальных балансов.
Материальный балансотражает количественные изменения,происходящие в ходе химико-технологического процесса.
Материальный баланс содержит приходную и расходную части. Приходная часть баланса: массы всех веществ, поступивших на переработку. Расходная часть баланса: массы всех веществ, получившихся в результате проведения технологического процесса. В таблице 4 приведен пример материального баланса обжига колчедана. Целью данного технологического процесса является получение оксида серы (IV), необходимого для производства серной кислоты.
Таблица 4. Материальный баланс обжига колчедана
| Вещество | Приход | Вещество | Расход |
| Колчедан | Оксид серы (IV) | ||
| Вода в колчедане | Оксид серы (VI) | ||
| Сухой воздух | Кислород | ||
| Вода в воздухе | Азот | ||
| Водяной пар | |||
| Огарок | |||
| Всего | Всего |
2. Закон сохранения энергии:При любых взаимодействиях, имеющихместо в изолированной системе, энергия этой системы остается постоянной и возможны лишь переходы одного вида энергии в другой.
В производстве на основе данного закона рассчитываются энергетические балансы. Энергетический баланс отражает расход различных видов энергии в ходе химико-технологического процесса. Приходная часть энергетического баланса: количество энергии, которое было затрачено для проведения и выделилось в ходе химико-технологического процесса. Расходная часть баланса: количество энергии, которое выделяется в окружающую среду продуктами химико-технологического процесса.
В таблице 5 приведен пример энергетического баланса обжига колчедана.
Таблица 5. Энергетический баланс обжига колчедана
| Приход | Энергия, МДж | Расход | Энергия, МДж |
| Тепло, выделяющееся при обжиге колчедана | Теплота, унесенная газами | ||
| Тепло, которое израсходовано на нагревание | Теплота огарка | ||
| Потери в окружаю- Щую среду | |||
| Получение водяного пара | |||
| Всего | Всего |
4. Закон постоянства состава:Любое химическое соединение имеет один и тот же количественный состав независимо от способа его получения (Ж. Пруст, 1801—1808 гг.).
Это значит, что соотношения между массами, элементов, входящих в состав соединения, постоянны.
Закон всегда выполняется для веществ молекулярного строения, но не всегда для веществ кристаллического строения.
Причина: наличие в кристаллической структуре пустот, не заполненных атомами, примесных атомов других элементов и других отклонений от идеальной структуры.
Пример: В диоксиде титана ТiO2 на единицу массы титана может приходиться от 0,65 до 0,67 единиц массы кислорода, что соответствует формуле ТiO1,9-2,0 .
Основные законы химии лежат в основе количественных расчетов, выполняемых в рамках стехиометрии.
Стехиометрия- раздел химии, посвященный изучению количественного состава веществ иотношений междуреагирующими веществами.
Без стехиометрии невозможно планирование процессов промышленного производства необходимых веществ, осуществляемого в рамках химической технологии.
Химическая технология - наука об оптимальных способах производства промышленных продуктов посредством химических реакций.
