Определение гидрокарбонатной жесткости воды
Теоретические основы. За счет вымывания осадочных горных пород природные воды содержат растворенные соли кальция и магния, которые придают воде жесткость. Гидрокарбонаты кальция и магния Са(НСО3)2 и Mg(НСО3)2 обусловливают гидрокарбонатную (временную) жесткость воды (Жврем). Она легко удаляется за счет разложения гидрокарбонатов при кипячении воды:
Са(НСО3)2 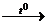 СаСО3
СаСО3 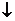 + СО2
+ СО2 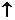 + Н2О
+ Н2О
Mg(НСО3)2 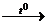 MgСО3
MgСО3 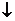 + СО2
+ СО2 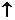 + Н2О
+ Н2О
Постоянная жесткость воды (Жпост) связана с присутствием в воде сульфатов и хлоридов кальция и магния: MgSO4, MgCl2, CaCl2. Эта жесткость воды удаляется только за счет обменных реакций, приводящих к образованию осадков (карбонатов кальция и магния) или с помощью ионообменных смол, обменивающих ионы водорода или натрия на ионы магния и кальция:
Са(НСО3)2 + Na2CO3  CaCO3
CaCO3 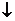 + 2 NaHCO3
+ 2 NaHCO3
Mg(НСО3)2 + Na2CO3  MgCO3
MgCO3 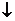 + 2 NaHCO3
+ 2 NaHCO3
Общее содержание солей кальция и магния в воде носит название общей жесткости воды (Жобщ). Общая жесткость слагается из постоянной и временной жесткости:
Жобщ=Жпост+ Жврем
Количественно жесткость выражается суммарным числом моль эквивалентов ионов магния и кальция в 1 м3 воды и может быть рассчитана по формуле:
Ж = СN 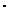 1000 = CN (Ca2+)
1000 = CN (Ca2+) 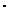 1000 + CN (Mg2+)
1000 + CN (Mg2+) 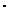 1000
1000
Гидрокарбонатная жесткость воды определяется титрованием соляной кислотой:
Са(НСО3)2 + 2 НСl  СаCl2 + 2 CO2
СаCl2 + 2 CO2 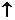 + 2 H2O
+ 2 H2O
Mg(НСО3)2 + 2 НСl  MgCl2 + 2 CO2
MgCl2 + 2 CO2 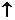 + 2 H2O
+ 2 H2O
Цель работы. Экспериментально определить гидрокарбо-натную жесткость предложенного образца жесткой воды титрованием соляной кислотой.
Порядок работы.
В коническую колбу отмерьте пипеткой точный объем жесткой воды (по указанию преподавателя), добавьте при необходимости дистиллированной воды. Титруйте раствором соляной кислоты в присутствии индикатора - метилоранжа как указано в работе 5.
Форма лабораторного отчета.
1. Название лабораторной работы.
2. Краткое описание, цель работы.
3. Номер варианта жесткой воды ...... .
4. Экспериментальные данные:
| № опыта | |||
| Объем кислоты V, мл |
Объем жесткой воды V 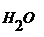 = .......
= .......
Концентрация раствора кислоты СN (HCl) = ......
5. Расчеты:
а) средний объем раствора кислоты:
V = 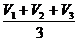 = ......
= ......
б) концентрация гидрокарбонатов кальция и магния в жесткой воде:
СN (солей) = 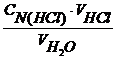 = .......
= .......
в) гидрокарбонатная жесткость воды:
Жврем = СN (солей) 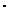 1000 = ........
1000 = ........
Типовые задачи
1. Жесткость воды, содержащей только гидрокарбонат кальция, равна 1,785 мэкв/л. Определить массу гидрокарбоната кальция в 3 л воды.
2. Чему равна временная жесткость воды, в 2 л которой содержится 0,292 г гидрокарбоната кальция?
3. В 2 л воды содержится 76 мг ионов магния и 216 мг ионов кальция. Вычислить общую жесткость воды.
4. Какую массу карбоната натрия надо добавить к 20 л воды, чтобы устранить общую жесткость, равную 4,60 мэкв/л?
5. При определении гидрокарбонатной жесткости воды на титрование 100 мл воды пошло 4,0 мл 0,1500 Н раствора соляной кислоты. Найти постоянную жесткость, если общая жесткость равна 7,1 мэкв/л.
6. При определении гидрокарбонатной жесткости воды на титрование 100 мл воды пошло 8,0 мл 0,0900 Н раствора соляной кислоты. Найти постоянную жесткость, если общая жесткость равна 8,3 мэкв/л.
Лабораторная работа 9
