Кафедра неорганической химии
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РФ
Кафедра неорганической химии
Х И М И Я
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по изучению дисциплины и задания
для контрольных работ
студентам заочного отделения
по инженерным специальностям
САНКТ-ПЕТЕРБУРГ
2 0 1 0
Методические рекомендации рассмотрены и одобрены учебно-методической комиссией факультета почвоведения и агроэкологии СПбГАУ. Протокол № 6 от 15 июня 2010 г.
С о с т а в и т е л и: доцент Б.П. Титов
доцент В.В. Порсев
доцент А.П. Агапова
ВВЕДЕНИЕ
В настоящее время в России одним из приоритетных национальных проектов по модернизации страны признана коренная перестройка сельскохозяйственного производства. Одним из важнейших этапов решения данной задачи является создание прочной материальной базы АПК.
И руководство страны, и руководство АПК стремятся модернизировать и развивать продовольственную отрасль экономики. Это предполагает: увеличение объемов производимой сельхозпродукции (при обеспечении ее необходимого качества), технологическое перевооружение перерабатывающих комплексов, ориентация производств АПК на научно обоснованные нормы потребления, а также внедрение новейших индустриальных технологий на всех участках функционирования АПК.
Усваивая общетеоретический материал, студент приобретает тот минимальный запас знаний, который понадобится ему и в будущей профессии, и при изучении специальных дисциплин на последующих курсах обучения по избранной специальности.
ОБЩИЕ МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ИЗУЧЕНИЮ ДИСЦИПЛИНЫ
Самостоятельное изучение курса предполагает ознакомление с программой курса химии.
Каждый студент выполняет одну контрольную работу и доставляет (или высылает по почте) в деканат заочного отделения, что является основанием для вызова студента на экзаменационную сессию. Во время сессии после прослушивания лекций и выполнения лабораторных работ студент сдает экзамен по всему курсу.
Оформление контрольной работы должно быть выполнено аккуратно и разборчиво. Для замечаний рецензента должны быть оставлены поля.
Условия заданий переписываются полностью с указанием номера задачи в соответствии с методическими рекомендациями.
Неряшливо оформленная или не полностью выполненная контрольная работа возвращается студенту.
После проверки контрольной работы студент внимательно рассматривает все замечания и указания преподавателя и вносит все необходимые коррективы и дополнения. Доработку неправильно выполненных заданий необходимо проводить в конце тетради.
ВНИМАНИЕ!На экзамене по химии будет проводиться собеседование по материалу контрольной работы. Данные методические рекомендации преследуют цель восстановить и закрепить основы, необходимые для усвоения курса химии в целом. Этими рекомендациями необходимо пользоваться параллельно с рекомендованным учебником.
Если задача не получается, рекомендуется еще раз обратиться к учебнику.
По непонятным вопросам рекомендуется обратиться на кафедру неорганической химии и получить там необходимую консультацию. При этом надо четко сформулировать свою проблему и указать, какой учебник был использован при выполнении контрольной работы.
ВОССТАНОВИТЕЛЬНАЯ ЧАСТЬ
Основные понятия химии
Атом – частица вещества, состоящая из положительного заряженного ядра и отрицательно заряженных электронов.
Молекула – наименьшая частица вещества, обладающая его химическими свойствами. Химические свойства молекул определяются их составом и химическим строением.
Химический элемент – определенный вид атомов с одинаковым зарядом ядра.
Простые вещества – вещества, образованные из атомов одного элемента. Например: N2, O2, Cl2, P4, S8 и т.п.
Сложные вещества, или химические соединения – вещества, образованные атомами разных элементов. Например: NH3; Ca(H2PO4)2; MgCl2; KNO3 и т.п.
Относительная атомная масса химического элемента – отношение средней массы атома естественного изотопического состава элемента к 1/12 массы атома изотопа углерода 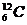 . Относительные атомные массы элементов обозначают Ar, где индекс«r» – начальная буква английского слова relative (относительный).
. Относительные атомные массы элементов обозначают Ar, где индекс«r» – начальная буква английского слова relative (относительный).
Записи Ar(H), Ar(O), Ar(C) означают относительные массы водорода, кислорода и углерода соответственно.
Вместо термина «относительная атомная масса» можно использовать исторически сложившийся термин «атомная масса».
Относительная молекулярная масса (Мr) равна отношению средней массы молекулы естественного изотопического состава к 1/12 массы изотопа углерода 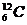 .
.
Относительная молекулярная масса равна сумме относительных атомных масс всех атомов, входящих в состав молекулы вещества. Она легко высчитывается по формуле вещества.
Относительная молекулярная масса вещества показывает, во сколько раз масса молекулы данного вещества больше 1/12 массы атома 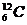 (т.е. атомной единицы массы, которая численно равна 1,66∙10-24 г).
(т.е. атомной единицы массы, которая численно равна 1,66∙10-24 г).
Моль – это единица количества вещества, принятая в международной системе единиц (СИ).
Один моль содержит, столько структурных единиц (молекул, атомов, ионов или других частиц), сколько атомов содержит 12 гизотопа углерода 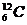 .
.
Зная массу одного атома углерода (1,999∙10-23 г), можно легко вычислить число атомов (NA)в 12 г углерода.
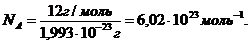
Это число называется постоянной Авогадро.
Единица количества (моль) обозначается «n».
Молярная масса вещества – это величина, равная отношению массы вещества (m) к количеству вещества:
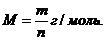
Основные законы химии
1. Закон сохранения массы вещества Масса веществ, вступающих в химическую реакцию равна массе веществ, образующихся в результате реакции.
2. Закон постоянства состава вещества Всякое химически чистое вещество молекулярной структуры всегда имеет постоянный качественный и количественный состав независимо от условий и способа получения этого вещества. Состав же соединений немолекулярной структуры (с атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения.
3. Закон Авогадро В равных объемах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул. Из закона Авогадро вытекает важное следствие: при одинаковых условиях 1 моль любого газа занимает одинаковый объем. При нормальных условиях (0ºС и р=101,3 кПа) 1 моль различных газов занимает объем, равный 22,4 л. Этот объем называется молярным объемом газа.
4. Закон эквивалентов Вещества, вступающие в химические реакции, реагируют между собой в количествах, прямо пропорциональных массам их эквивалентов.
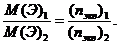
М(Э)1 и М(Э)2 – молярные массы эквивалентов веществ (1) и (2) соответственно.
n(экв)1 и n(экв)2 – числа моль эквивалентов веществ (1) и (2) соответственно. Как вычисляют М(Э)1 и М(Э)2, следует смотреть в учебнике.
ЗАДАНИЯ И МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ВЫПОЛНЕНИЮ КОНТРОЛЬНОЙ РАБОТЫ
Гидролиз солей
Гидролизом солей называют реакции ионного обмена между молекулами растворенной соли и молекулами воды с образованием слабого электролита (т.е. молекул или ионов слабого электролита).
Студентам рекомендуется основательно проработать по учебным пособиям соответствующие параграфы и приобрести навыки для записи процессов гидролиза солей по шагам:
1. Составить уравнение электролитической диссоциации соли.
2. Определить, по какому из ионов идет гидролиз соли. Гидролиз идет по иону, образованному из слабого электролита. Список сильных кислот и оснований приведен выше (см. раздел «Кислоты и основания.
3. Написать для выбранного иона уравнение взаимодействия с одной молекулой воды. Данное уравнение и будет главной записью гидролиза соли – сокращенным ионным уравнением гидролиза. Уравнение демонстрирует наступившее в растворе равновесие и характеризуется собственной константой равновесия – константой гидролиза (КГ.). На этом этапе возможно определить характер среды, возникающей в растворе – создается: либо кислая, либо щелочная реакция среды. В случае, когда соль образована слабой кислотой и слабым основанием, реакция среды будет близкой к нейтральной (т.е. pН ≈ 7).
4. Написать уравнение гидролиза в молекулярном виде. При этом за основу берется ионное уравнение, а для составления молекул используются ионы противоположного знака (противоионы) из уравнения диссоциации соли (см. шаг 1).
Пример.Составить уравнение гидролиза хлорида меди (II).
1. Диссоциация соли: CuCl2 = Cu2+ + 2Cl–.
2. Известно, что катиону Cu2+ соответствует слабое основание, а иону Cl– – сильная кислота. Таким образом, гидролиз идет по катиону.
3. Уравнение гидролиза: Cu2+ + HOH ↔ (CuOH)+ + H+. Закономерно, что положительный катион Cu2+ притягивает к себе из молекулы воды отрицательную частицу OH– и образуется составной катион с зарядом +1. Связывание катионом Cu2+ частиц OH– приводит к накоплению в растворе избытка ионов H+ и, следовательно, в результате гидролиза в растворе создается кислая среда.
Осталось записать выражение для константы гидролиза:
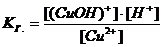 .
.
4. При составлении уравнения в молекулярной форме, надо увидеть, что всем положительным ионам соответствуют имеющиеся в растворе в свободном виде отрицательные ионы Cl–. С учетом зарядов ионов составляем электронейтральные молекулы и подбираем коэффициенты:
CuCl2 + HOH ↔ Cu(OH)Cl + HCl.
Контрольные задания.
Составьте ионные и молекулярные уравнения гидролиза солей, приведенных в вашем задании, а также напишите выражения для констант гидролиза.
101. Хлорид алюминия, сульфид калия.
102. Нитрат меди (II), карбонат натрия.
103. Сульфат железа (II), силикат натрия.
104. Хлорид никеля (II), сульфит калия.
105. Сульфат аммония, ортоборат натрия.
106. Хлорид цинка, сульфид бария.
107. Нитрат свинца (II), цианид калия.
108. Нитрат алюминия, ацетат калия.
109. Хлорид марганца (II), ортофосфат калия.
110. Бромид железа (III), гипохлорит натрия.
111. Хлорид хрома (III), сульфид кальция.
112. Нитрат свинца (II), карбонат калия.
113. Сульфат алюминия, ортоборат натрия.
114. Нитрат никеля (II), силикат натрия.
115. Иодид железа (II), ацетат кальция.
116. Сульфат цинка, сульфид натрия.
117. Хлорид цинка, ортофосфат калия.
118. Бромид свинца (II), карбонат натрия.
119. Сульфат олова (II), силикат калия.
120. Йодид марганца (II), гипохлорит кальция.
Коррозия металлов
Коррозией металлов называется самопроизвольно протекающий процесс разрушения металлов и сплавов в результате воздействия на них окружающей среды. Характер этого воздействия может иметь либо химический, либо электрохимический характер.
Чаще всего, используя на практике металлы и сплавы, а также при эксплуатации различного оборудования, приходится сталкиваться с электрохимической коррозией. В этом случае на поверхности образуются так называемые микрогальванические элементы. Анодом в этом случае будет более активный металл, катодом – менее активный.
На аноде всегда будет проходить процесс окисления металла:
Ме – nē → Men+ (анодный процесс).
Катодный процесс зависит от pH среды:
· Если среда кислая, то на катоде происходит восстановление катионов водорода:
2Н+ + 2ē → Н2 (катодный процесс, pH < 7).
· В нейтральной и щелочной среде на катоде протекает реакция восстановления молекул кислорода:
О2 +2Н2О + 4ē → 4ОН– (катодный процесс, pH ≥ 7).
Пример.Составить схему микрогальванического элемента, образующегося на поверхности стального изделия, находящегося в контакте со свинцом. Отметить какой металл является катодом, а какой анодом. Разобрать случаи нейтральной и кислой коррозионных сред. Составить электронные уравнения катодного и анодного процессов и определить состав продуктов коррозии.
Так как железо имеет меньшее значение стандартного электродного потенциала (–0,440 В) по сравнению со свинцом (–0,127 В), то железо является анодом, а свинец – катодом.
На аноде проходит следующий процесс:
Fе – 2ē → Fe2+ (анод – окисление железа).
На катоде, при pH < 7:
2Н+ + 2ē → Н2 (катод – восстановление Н+).
На катоде, при pH ≈ 7:
О2 +2Н2О + 4ē → 4ОН– (катод – восстановление O2)
Продукты коррозии формируются из соединений, образующихся на катоде и аноде. В случае кислой среды, продуктом будет соль иона Fe2+ и кислотного остатка кислоты, которая определяет pH среды. Например, если кислая среда создается растворенным углекислым газом, то в качестве продуктов коррозии будет образовываться соль FeCO3:
Fe2+ + CO32– → FeCO3.
В случае щелочной или нейтральной среды, продуктом будет гидроксид металла:
Fe2+ + 2OH– → Fe(OH)2.
В свою очередь, Fe(OH)2 окисляется на воздухе до Fe(OH)3, переходящего в бурую ржавчину – FeO(OH):
4Fe(OH)2 + O2 + 2Н2О → 4Fe(OH)3,
Fe(OH)3 → FeO(OH) + Н2О.
Схемы микрогальванического элемента выглядят следующим образом:
(анод) Fe| H+ |Pb (катод) (при pH < 7),
(анод) Fe| Н2О, O2 |Pb (катод) (при pH ≈ 7).
Нужно обратить внимание, что в данных Г.Э. нет двойной черты, так как оба «электрода» находятся в одном и том же растворе.
Контрольные задания
1. Составить схему микрогальванического элемента, пометив какой металл является катодом, а какой анодом.
2. В соответствии со средой, указанной в таблице 11, составить электронные уравнения катодного и анодного процессов.
3. Составить уравнения образования конечных продуктов коррозии.
Т а б л и ц а 11
| номер задания | контактирующие металлы | коррозионная среда |
| Al и Cd | HCl | |
| Cu и Zn | Ca(OH)2 | |
| Cu и Mg | влажный воздух | |
| Zn и Pb | вода, насыщенная кислородом | |
| Ni и Cu | Н2SO4 | |
| Cr и Cu | CH3COOH | |
| Pb и Zn | влажный воздух | |
| Fe и Sn | HCl | |
| Ni и Ag | Na2CO3 (раствор) | |
| Cu и Cr | Ca(OH)2 | |
| Cd и Fe | влажный воздух | |
| Fe и Sn | HF | |
| Mg и Cu | HCl | |
| Al и Cu | вода, насыщенная кислородом | |
| Cr и Mg | Н2SO4 | |
| Ag и Cd | HСl | |
| Fe и Zn | влажный воздух | |
| Cd и Al | К2CO3 | |
| Cu и Co | HF | |
| Fe и Mg | вода, насыщенная кислородом |
Электролиз
Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического токачерез систему, состоящую из раствора или расплава электролита и из двух электродов, помещенных в раствор или расплав.
Как и при работе гальванических элементов, электрод, на котором происходит восстановление,называется катодом, а электрод, на котором происходит окисление – анодом.
При электролизе расплавов (вода в системе отсутствует) процесс электролиза протекает по относительно простому механизму. На катоде идет процесс восстановления катиона электролита, а на аноде – процесс окисления аниона электролита, например, электролиз расплава ScCl3:
2Сl– – 2ē → Cl2 (анод),
Sc3+ + 3ē → Sc (катод).
В случае электролиза водных растворов электролитов на механизм химических превращений при электролизе накладывается возможное превращение воды под воздействием постоянного электрического тока.
Принято отдельно рассматривать процессы, протекающие на катоде (т.е. процессы восстановления). Эти процессы не зависят от материала катода, а определяются преимущественно положением металла электролита в ряду стандартных электродных потенциалов. Богатейший индустриальный и научный опыт показывает, что, если металл, образующий данный электролит, находится в ряду стандартных электродных потенциалов после водорода (т.е. Eº > 0), то из двух конкурирующих процессов (восстановление молекул Н2О или восстановление катионов Меn+) предпочтение получают катионы Меn+, т.к. потенциал у этих катионов значительно больше, чем потенциал восстановления воды. Такие металлы называются малоактивными. В этом случае полуреакции восстановления выглядят так:
(катод) Меn+ + nē → Me.
При движении по ряду напряжений справа налево, наблюдаем уже сопоставимые величины стандартных электродных потенциалов. Поэтому, на катоде одновременно идут два процесса – восстановление H2O и восстановление Меn+. Такие металлы образуют группу металлов средней активности. Условно считается, что в эту группу входят металлы от алюминия до водорода в ряду напряжений металлов. Катодный процесс записывают двумя электронными уравнениями:
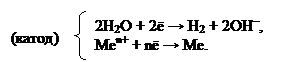
Для катионов металлов, находящихся левее алюминия (а также сам алюминий), величины стандартных электродных потенциалов уже значительно ниже, чем потенциал восстановления воды. Поэтому на катоде будет проходить единственный процесс – восстановление воды. Такие металлы называются активными. На катоде происходит следующий процесс:
(катод) 2Н2О +2ē → Н2 + 2ОН–.
Процессы, проходящие на аноде, зависят от материала, из которого изготовлен анод. Инертным (нерастворимым) называется анод, изготовленный из графита, золота, рутения, родия, палладия, осмия, иридия или платины. Аноды, изготовленные из других металлов, называются растворимыми.
Если анод нерастворимый и анион в составе соли не содержит кислород (например S2–, Cl–, Se2–, Br–, и т.п.), то при достаточно больших концентрациях этих анионов они легко окисляются (исключением из этого правила является анион F–). В этом случае анодный процесс записывается следующим образом:
(анод) S2– – 2ē → S (пример для сульфидного аниона),
(анод) 2Br– – 2ē → Br2 (пример для бромидного аниона).
Если же анод нерастворимый, а в составе аниона соли содержится кислород(например, NO3–, SO42–, и т.п.), то окисляется вода. Такое же правило действует для фторидных анионов F–. На аноде проходит следующий процесс:
(анод) 2Н2О – 4ē → О2 + 4Н+.
Если анод растворимый, то происходит растворение металла, из которого изготовлен анод:
(анод) Me – nē → Меn+.
Для того чтобы рассчитать количественные характеристики процесса электролиза, можно воспользоваться законами Фарадея.
Согласно II закону Фарадея, масса электролита, подвергшаяся разложению при электролизе, а также массы, образующихся на электродах веществ прямо пропорциональны количеству электричества(в кулонах), прошедшего через раствор (или расплав) электролита, и эквивалентным массам соответствующих веществ:
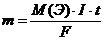 ,
,
где m – масса электролита, окисленного или восстановленного на электроде;
М(Э) – молярная масса эквивалента электролита, измеряется в г/моль-экв.;
I – сила тока, А;
t – продолжительность электролиза, с;
F – число Фарадея. F ≈ 96500 Кл/моль.
Для нахождения молярной массы эквивалента электролита, следует разделить молярную массу электролита на число электронов, участвующих в реакции.
Контрольные задания
1. Составить электронные уравнения катодного и анодного процессов электролиза для заданного в табл. 12 раствора (или расплава) электролита:
· с нерастворимым анодом;
· с растворимым анодом (если анод указан в задании).
2. Рассчитать по закону Фарадея массу металла, выделившегося на катоде, или объем газа (при н.у.), выделившегося на аноде.
3. Составить молекулярное уравнение процесса электролиза.
Т а б л и ц а 12
| номер задания | соль | раств. анод | I, А | t, час | рассчитать: |
| CuSO4 (раствор) | Cu | m(Cu) | |||
| ScCl3 (раствор) | Sc | 1,5 | V(Cl2) | ||
| Pb(NO3)2 (раствор) | Pb | m(Pb) | |||
| TiCl4 (расплав) | Ti | V(Cl2) | |||
| SnCl2 (расплав) | Sn | 0,5 | m(Sn) | ||
| Ni2(SO4)3 (раствор) | Ni | 0,8 | V(O2) | ||
| AgNO3 (раствор) | Ag | m(Ag) | |||
| Cr(NO3)3 (раствор) | Cr | 1,5 | V(O2) | ||
| AlF3 (расплав) | – | m(Al) | |||
| CoSO4 (раствор) | Co | V(O2) |
Задания по органической химии. Полимеры
191. Какие соединения называются диеновыми? Привести пример. Написать схему полимеризации при производстве синтетического каучука.
192. Предельные и непредельные углеводороды. Написать общие формулы алканов и алкенов. Примеры. Что такое полимеризация и поликонденсация? В чем отличие способов получения этих высокомолекулярных соединений?
193. Записать структурную формулу акриловой кислоты. Составить уравнение этерификации акриловой кислоты с этиловым спиртом. Напишите схему полимеризации полученного продукта этерификации.
194. Составить уравнения реакций в соответствии с цепочкой превращений:
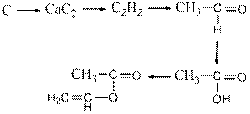
195. Напишите структурную формулу метакриловой кислоты. Составьте уравнения реакции взаимодействия этой кислоты с метанолом, а затем приведите схему полимеризации полученного продукта этерификации.
196. Приведите примеры двух простейших аминокислот. Составьте формулы двух тетрапептидов из этих аминокислот (один – из однородных мономеров; второй – из различных). Назовите полимер из однородных мономеров.
197. Что такое альдегиды? Какова общая формула этих соединений? Написать реакцию серебряного зеркала для ацетальдегида.
198. Написать формулы фенола и муравьиного альдегида. Составить схему получения фенолформальдегидной смолы.
199. Написать формулу изопрена. Составить схему получения натурального каучука.
200. Написать структурную формулу стирола. Составить схему получения полистирола.
ПРИЛОЖЕНИЯ
Т а б л и ц а 13. Номера вопросов для контрольной работы
| Предпоследняя цифра шифра | Последняя цифра шифра | |||||||||
| 10, 30, 50, 70, 90, 110, 130 ,150, 170, 190 | 1, 21, 41, 61, 81, 101, 121, 141, 161, 181 | 2, 22, 42, 62, 82, 102, 122, 142, 162, 182, | 3, 23, 43, 63, 83, 103, 123, 143, 163, 183 | 4, 24, 44, 64, 84, 104, 124, 144, 164, 184 | 5, 25, 45, 65, 85, 105, 125, 145, 165, 185 | 6, 26, 46, 66, 86, 106, 126, 146, 166, 186 | 7, 27, 47, 67, 87, 107, 127, 147, 167, 187 | 8, 28, 48, 68, 88, 108, 128, 148, 168, 188 | 9, 29, 49, 69, 89, 109, 129, 149, 169, 189 | |
| 20, 40, 60, 80, 100, 120, 140, 160, 180, 200 | 11, 31, 51, 71, 91, 111, 131, 151, 171, 191 | 12, 32, 52, 72, 92, 112, 132, 152, 172, 192 | 13, 33, 53, 73, 93, 113, 133, 153, 173, 193 | 14, 34, 54, 74, 94, 114, 134, 154, 174, 194 | 15, 35, 55, 75, 95, 115, 135, 155, 175, 195 | 16, 36, 56, 76, 96, 116, 136, 156, 176, 196 | 17, 37, 57, 77, 97, 117, 137, 157, 177, 197 | 18, 38, 58, 78, 98, 118, 138, 158, 178, 198 | 19, 39, 59, 79, 99, 119, 139, 159, 179, 199 | |
| 19, 32, 57, 76, 93, 114, 137, 151, 73, 198 | 1, 22, 43, 64, 85, 106, 127, 148, 171, 192 | 2, 23, 44, 65, 86, 107, 128, 149, 172, 193 | 3, 21, 46, 67, 88, 109, 131, 152, 174, 195 | 4, 25, 45, 66, 87, 110, 129, 147, 173, 196 | 5, 26, 47, 68, 89, 111, 130, 150, 175, 194 | 6, 27, 41, 61, 82, 101, 132, 151, 176, 191 | 7, 24, 42, 62, 81, 102, 133, 152, 177, 197 | 8, 29, 49, 63, 83, 103, 121, 142, 163, 184 | 9, 28, 50, 71, 92, 104, 122, 141, 178, 198 | |
| 18, 33, 54, 78, 97, 118, 136, 157, 74, 193 | 10, 21, 42, 63, 84, 105, 126, 147, 168, 189 | 11, 22, 43, 64, 85, 106, 127, 148, 169, 190 | 12, 23, 44, 65, 86, 107, 128, 149, 170, 191 | 13, 24, 45, 66, 87, 108, 129, 150, 171, 192 | 12, 25, 46, 67, 88, 109, 130, 151, 172, 193 | 13, 26, 47, 68, 89, 110, 131, 152, 173, 194 | 14, 27, 48, 69, 90, 111, 132, 153, 174, 195 | 15, 28, 49, 70, 91, 112, 133, 154, 175, 196 | 16, 29, 50, 71, 92, 113, 134, 155, 176, 197 |
Т а б л и ц а 13. Номера вопросов для контрольной работы (окончание)
| Предпоследняя цифра шифра | Последняя цифра шифра | |||||||||
| 17, 37, 54, 76, 92, 113, 134, 159, 178, 192 | 17, 30, 51, 72, 93, 114, 135, 156, 77, 198 | 18, 31, 52, 73, 94, 115, 136, 157, 178, 199 | 19, 32, 53, 74, 95, 116, 137, 158, 179, 200 | 20, 33, 54, 75, 96, 117, 138, 158, 180, 190 | 1, 34, 55, 76, 97, 118, 139, 159, 179, 191 | 2, 35, 56, 77, 98, 119, 140, 160, 178, 192 | 3, 36, 57, 78, 99, 118, 138, 159, 180, 193 | 4, 37, 58, 79, 100, 117, 139, 160, 179, 194 | 5, 38, 58, 79, 99, 116, 140, 159, 180, 195 | |
| 16, 34, 55, 74, 94, 115, 138, 152, 172, 191 | 6, 39, 59, 80, 100, 120, 121, 141, 161, 181 | 7, 40, 60, 79, 81, 101, 122, 143, 164, 185 | 8, 21, 41, 61, 82, 103, 123, 142, 162, 182 | 9, 22, 42, 62, 83, 104, 124, 144, 163, 183 | 10, 23, 43, 63, 84, 105, 125, 145, 165, 184 | 11, 24, 44, 64, 85, 106, 125, 145, 164, 184 | 12, 25, 45, 65, 86, 107, 126, 146, 165, 185 | 13, 26, 46, 66, 87, 108, 127, 147, 166, 186 | 14, 27, 47, 67, 88, 109, 128, 148, 167, 187 | |
| 15, 36, 56, 77, 95, 112, 133, 158, 176, 194 | 15, 28, 48, 68, 89, 110, 129, 149, 168, 188 | 16, 29, 49, 69, 90, 111, 130, 150, 169, 189 | 17, 30, 50, 70, 91, 112, 131, 151, 170, 190 | 18, 31, 51, 71, 92, 113, 132, 152, 171, 191 | 19, 32, 52, 72, 93, 114, 133, 153, 172, 192 | 20, 33, 53, 73, 94, 115, 134, 154, 173, 193 | 1, 39, 54, 74, 95, 116, 135, 155, 74, 194 | 2, 38, 55, 75, 96, 117, 136, 156, 175, 195 | 3, 37, 56, 76, 97, 118, 137, 157, 176, 196 | |
| 14, 35, 51, 72, 93, 114, 135, 156, 175, 191 | 4, 36, 57, 77, 98, 119, 138, 158, 177, 197 | 5, 35, 58, 78, 99, 120, 139, 159, 178, 198 | 6, 34, 59, 79, 100, 121, 140, 160, 179, 199 | 7, 33, 60, 80, 99, 120, 139, 151, 180, 200 | 8, 32, 59, 79, 98, 119, 138, 152, 171, 192 | 9, 31, 58, 78, 97, 118, 137, 153, 172, 191 | 10, 30, 57, 77, 96, 117, 136, 154, 173, 192 | 11, 29, 56, 76, 95, 116, 135, 155, 174, 193 | 12, 28, 55, 75, 94, 115, 134, 156, 175, 194 | |
| 13, 39, 58, 79, 91, 111, 131, 154, 171, 197 | 13, 27, 54, 74, 93, 114, 133, 157, 176, 195 | 14, 26, 53, 79, 93, 113, 132, 158, 177, 196 | 15, 25, 52, 72, 92, 112, 131, 159, 178, 197 | 16, 24, 51, 71, 91, 111, 130, 160, 179, 198 | 17, 23, 50, 70, 90, 110, 129, 151, 180, 199 | 18, 22, 49, 69, 89, 109, 128, 152, 171, 200 | 19, 21, 48, 68, 87, 108, 127, 153, 172, 191 | 20, 22, 47, 67, 87, 107, 126, 154, 173, 192 | 1, 23, 46, 66, 86, 106, 125, 155, 174, 193 | |
| 12, 30, 51, 72, 93, 114, 135, 156, 177, 198 | 2, 24, 45, 65, 85, 105, 124, 156, 175, 194 | 3, 25, 44, 64, 84, 104, 123, 157, 176, 195 | 4, 26, 43, 63, 83, 103, 122, 158, 177, 196 | 5, 27, 42, 62, 82, 102, 121, 159, 179, 197 | 6, 28, 41, 61, 81, 101, 130, 160, 180, 198 | 7, 29, 59, 70, 100, 119, 131, 150, 170, 199 | 8, 30, 58, 79, 99, 118, 138, 158, 178, 191 | 9, 31, 57, 78, 98, 117, 132, 159, 179, 192 | 10, 32, 56, 77, 97, 116, 133, 152, 180, 193 |
Т а б л и ц а 14. Номенклатура некоторых кислот и солей
| формула кислоты | название кислоты | название соли |
| Н3ВО3 | ортоборная | ортоборат |
| Н2СО3 | угольная | карбонат |
| Н2С2О4 | щавелевая | оксалат |
| СНзСООН | уксусная | ацетат |
| HCN | циановодородная | цианид |
| H2SiO3 | метакремниевая | метасиликат |
| HNO3 | азотная | нитрат |
| HNO2 | азотистая | нитрит |
| НРО3 | метафосфорная | метафосфат |
| Н3РО4 | ортофосфорная | ортофосфат |
| H3AsO4 | ортомышьяковая | ортоарсенат |
| H2SO4 | серная | сульфат |
| H2SO3 | сернистая | сульфит |
| H2S | сероводородная | сульфид |
| H2SeO4 | селеновая | селенат |
| H2TeO4 | теллуровая | теллурат |
| HF | фтороводородная | фторид |
| HClO4 | хлорная | перхлорат |
| НСlO3 | хлорноватая | хлорат |
| HClO2 | хлористая | хлорит |
| HClO | хлорноватистая | гипохлорит |
| HC1 | хлороводородная | хлорид |
| HBrO4 | бромная | пербромат |
| HBrO3 | бромноватая | бромат |
| HBrO2 | бромистая | бромит |
| HBrO | бромноватистая | гипобромит |
| HBr | бромоводородная | бромид |
| HI | иодоводородная | иодид |
Т а б л и ц а 15. Стандартные электродные потенциалы (ряд напряжений) некоторых металлов
| электрод | Еº(Меn+|Me), В | электрод | Еº(Меn+|Me), В |
| Li+| Li | –3,045 | Fe2+| Fe | –0,440 |
| Rb+| Rb | –2,925 | Cd2+| Cd | –0,403 |
| K+| K | –2,924 | Co2+| Co | –0,227 |
| Cs+| Cs | –2,323 | Ni2+| Ni | –0,250 |
| Ba2+|Ba | –2,900 | Sn2+| Sn | –0,136 |
| Ca2+|Ca | –2,870 | Pb2+| Pb | –0,127 |
| Na+| Na | –2,714 | 2H+|H2 | 0,000 |
| Mg2+| Mg | –2,370 | Sb3+| Sb | +0,200 |
| Al3+| Al | –1,670 | Bi3+| Bi | +0,215 |
| Ti2+| Ti | –1,603 | Cu2+| Cu | +0,340 |
| Zr4+| Zr | –1,580 | Cu+| Cu | +0,520 |
| Mn2+| Mn | –1,180 | Hg22+|2Hg | +0,790 |
| V2+| V | –1,21 | Ag+| Ag | +0,800 |
| Cr2+|Cr | –0,913 | Hg2+| Hg | +0,850 |
| Zn2+| Zn | –0,763 | Pt2+| Pt | +1,190 |
| Cr3+| Cr | –0,740 | Au3+| Au | +1,500 |
Т а б л и ц а 16. Константы диссоциации некоторых слабых кислот и оснований в водных растворах при 250С
| электролит | формула | константа диссоциации |
| кислоты, Ка | ||
| сероводородная | H2S | Ka(I) 9,56·10–8 |
| Ka(II) 1,26·10–14 | ||
| угольная | Н2СО3 | Ka(I) 4,45·10–7 |
| Ka(II) 4,69·10–11 | ||
| кремниевая | H2SiO3 | Ka(I) 2,2·10–10 |
| Ka(II) 1,6·10–12 | ||
| сернистая | H2SO3 | Ka(I) 1,23·10–2 |
| Ka(II) 6,6·10–8 | ||
| ортоборная | Н3ВО3 | Ka(I) 7,1·10–10 |
| Ka(II) 1,8·10–13 | ||
| Ka(III) 1,6·10–14 | ||
| уксусная | СН3СООН | Ka(I) 1,74·10–5 |
| ортофосфорная | Н3РО4 | Ka(I) 7,11·10–3 |
| Ka(II) 6,32·10–8 | ||
| Ka(III) 4,46·10–13 | ||
| циановодородная | HCN | Ka(I) 6,16·10–10 |
| хлорноватистая | HClO | Ka(I) 2,95·10–8 |
| основания, Кb | ||
| гидроксид аммония | NH4OH | Kb(I) 1,76·10–5 |
| гидроксид алюминия | Аl(ОН)3 | Kb(III) 1,38·10–9 |
| гидроксид меди (II) | Сu(ОН)2 | Kb(II) 3,4·10–7 |
| гидроксид железа (II) | Fe(OH)2 | Kb(II) 1,3·10–4 |
| гидроксид железа (III) | Fe(OH)3 | Kb(III) l,35·10–12 |
| гидроксид никеля (II) | Ni(OH)2 | Kb(II) 2,5·10–5 |
| гидроксид цинка | Zn(OH)2 | Kb(II) 4,0·10–5 |
| гидроксид свинца (II) | Pb(OH)2 | Kb(II) 3,0·10–8 |
| гидроксид марганца (II) | Mn(OH)2 | Kb (II) 5,0·10–4 |
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РФ
Кафедра неорганической химии
Х И М И Я
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
по изучению дисциплины и задания
для контрольных работ
студентам заочного отделения
по инженерным специальностям
САНКТ-ПЕТЕРБУРГ
2 0 1 0
Методические рекомендации рассмотрены и одобрены учебно-методической комиссией факультета почвоведения и агроэкологии СПбГАУ. Протокол № 6 от 15 июня 2010 г.
С о с т а в и т е л и: доцент Б.П. Титов
доцент В.В. Порсев
доцент А.П. Агапова
ВВЕДЕНИЕ
В настоящее время в России одним из приоритетных национальных проектов по модернизации страны признана коренная перестройка сельскохозяйственного производства. Одним из важнейших этапов решения данной задачи является создание прочной материальной базы АПК.
И руководство страны, и руководство АПК стремятся модернизировать и развивать продовольственную отрасль экономики. Это предполагает: увеличение объемов производимой сельхозпродукции (при обеспечении ее необходимого качества), технологическое перевооружение перерабатывающих комплексов, ориентация производств АПК на научно обоснованные нормы потребления, а также внедрение новейших индустриальных технологий на всех участках функционирования АПК.
Усваивая общетеоретический материал, студент приобретает тот минимальный запас знаний, который понадобится ему и в будущей профессии, и при изучении специальных дисциплин на последующих курсах обучения по избранной специальности.
ОБЩИЕ МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ИЗУЧЕНИЮ ДИСЦИПЛИНЫ
Самостоятельное изучение курса предполагает ознакомление с программой курса химии.
Каждый студент выполняет одну контрольную работу и доставляет (или высылает по почте) в деканат заочного отделения, что является основанием для вызова студента на экзаменационную сессию. Во время сессии после прослушивания лекций и выполнения лабораторных работ студент сдает экзамен по всему курсу.
Оформление контрольной работы должно быть выполнено аккуратно и разборчиво. Для замечаний рецензента должны быть оставлены поля.
Условия заданий переписываются полностью с указанием номера задачи в соответствии с методическими рекомендациями.
Неряшливо оформленная или не полностью выполненная контрольная работа возвращается студенту.
После проверки контрольной работы студент внимательно рассматривает все замечания и указания преподавателя и вносит все необходимые коррективы и дополнения. Доработку неправильно выполненных заданий необходимо проводить в конце тетради.
ВНИМАНИЕ!На экзамене по химии будет проводиться собеседование по материалу контрольной работы. Данные методические рекомендации преследуют цель восстановить и закрепить основы, необходимые для усвоения курса химии в целом. Этими рекомендациями необходимо пользоваться параллельно с рекомендованным учебником.
Если задача не получается, рекомендуется еще раз обратиться к учебнику.
По непонятным вопросам рекомендуется обратиться на кафедру неорганической химии и получить там необходимую консультацию. При этом надо четко сформулировать свою проблему и указать, какой учебник был использ<
