Ацетиленовые углеводороды (Алкины)
|
Алкины – это УВ, в молекулах которых два атома углерода находятся в состоянии sp-гибридизации и связаны друг с другом тройной связью: 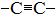
Длина связи 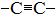 в алкинах равна 0,120 нм. Валентный угол = 180.
в алкинах равна 0,120 нм. Валентный угол = 180.
Каждый атом углерода в состоянии sp-гибридизации связан с двумя другими атомами и может присоединять ещё два атома.
В молекуле одна σ-связь и две π-связи.
Химические свойства
I. Реакции присоединения
1. Гидрирование
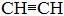 + H2 à CH2 = CH2
+ H2 à CH2 = CH2
этин этен
CH2 = CH2 +H2 à CH3 – CH3
этен этан
2. Присоединение галогенов
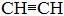 + Cl2 à CHCl = CHCl
+ Cl2 à CHCl = CHCl
этин 1,2 дихлорэтан
CHCl = CHCl + Cl2 à CHCl2 – CHCl2
1,1,2,2 тетрахлорэтан
3. Присоединение галогенно-водородных
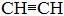 + HCl à CH2 – CHCl
+ HCl à CH2 – CHCl
4. Гидратация (реакция Кучерова)
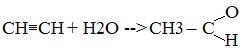 уксусный альдегид
уксусный альдегид
II. Реакции окисления
1. Горение
2C2H2 + 5O2 à 4CO2 + 2H2O
2. Обесцвечивание KMnO4
III. Полимеризация
3C2H2 à C6H6 (t, активированный уголь)
бензол
Получение
1) Из метана
2CH4 à C2H2  + 3H2
+ 3H2 
2) Из карбида кальция
CaC2 + 2HOH à C2H2 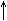 + Ca(OH)2
+ Ca(OH)2
Применение
Винилацетилен, щавельная кислота, винилхлорид, ацельдегид, сварка и резка металлов.
Вопрос №27
Ароматические углеводороды (Арены)
|
Ароматические УВ (арены) – это УВ, молекулы которых содержат одно или несколько бензольных колец или ядер.
Строение молекул бензола
C6H6
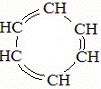
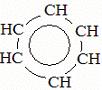
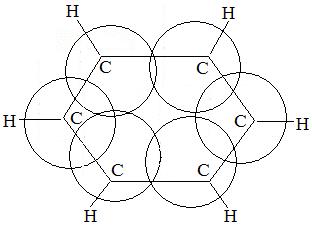
SP2 – гибридизация
1200 – валентный угол
l = 0,140 нм (длина связи)
π-электронное облако состоит из 6 Pe (электронов).
Гомологический ряд
С6H6 – бензол
С6H5 – CH3 – метилбензол
С6H5 – C3H5 – этилбензол
С6H5 – C3H7 – пропилбензол
С6H5 – C4H9 – бутилбензол
Физические свойства
Бензол – бесцветная, нерастворимая в воде жидкость со своеобразным запахом. Его t кипения = 80,10 С. При охлаждении он легко застывает в белую кристаллическую массу с t плавления = 5,50 С.
Химические свойства
I. Реакции замещения
1. Взаимодействие с галогенами
C6H6 + Br2 à C6H5Br + HBr (в присутствии FeCl3)
2. Взаимодействие с HNO3
C6H6 + HONO2 à C6H5NO2 + H2O (в присутствии H2SO4)
нитробензол
II. Реакции присоединения
1. Гидрирование (присоединение Н2)
 + 3H2 à
+ 3H2 à 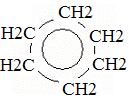
бензол циклогексан
2. Присоединение галогенов
 + 3Cl2 à
+ 3Cl2 à 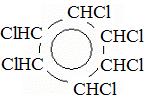 (при температуре)
(при температуре)
бензол гексохлорциклогексан
III. Реакции окисления
1. Горение
2C6H6 + 15O2 à 12CO2 + 6H2O
2. Бензол стоек к действию окислителей. Окисляются только гомологи по боковой цепи.
C6H5 – CH3 + 3O à C6H5 – COOH + H2O (в присутствии KMnO4)
бензойная кислота
Получение
1) Из циклогексана
C6H12 à 3H2 + C6H6 (при t и катализаторе)
циклогексан бензол
2) Из гексана
C6H14 à C6H6 + 4H2 (при t и катализаторе)
3) Из ацетилена
3C2H2 à C6H6 (при t и катализаторе)
Применение бензола: получение пластмасс, красителей, растворителей, бутадиенового каучука, волокна лавсана, сахарина, анилина, лекарств, средств для борьбы с вредными насекомыми и болезнями.
Вопрос №28
Газ, нефть, кокс.
Природный газ
Месторождения: Уренгойское, Заполярное, Вуктыльское, Оренбургское, Газли, Ставропольское.
Основным компонентом природного газа является метан. В нём содержаться также этан, пропан, бутан. Существует следующая закономерность: чем выше относительная молекулярная масса углеводорода, тем меньше его содержится в природном газе.
Применение
При сгорании природного газа выделяется много теплоты, поэтому он служит энергетически эффективным и дешёвым топливом в котельных установках, доменных, мартеновских и стекловаренных печах и так далее.
Природный газ – источник сырья для химической промышленности: получение ацетилена, этилена, водорода, сажи, различных пластмасс, уксусной кислоты, красителей, медикаментов и других продуктов.
Нефть
Нахождение: в недрах Земли на различной глубине. Если она под давлением газов, то поднимается по скважине на поверхность Земли.
Физические свойства:
Масляная жидкость от светло-бурого до чёрного цвета, легче воды, не растворима в ней, нет определённой температуры кипения.
Состав зависит от месторождения.
Фракции нефти:
1. Собираемая от 40 до 200 С – газолиновая фракция бензинов (от C5H12 ДО C11H24). При дальнейшей перегонке получают: газолин (от 40 до 70 С), бензин (от 70 до 120 С) – авиационный, автомобильный и так далее.
2. Лигроиновая фракция, собираемая от 150 до 250 С, (от С8Н18 до С14Н30). Применение: как горячее для тракторов.
3. Керосиновая фракция (от С23Н26 до С18Н38) с температурой кипения = 180 – 300 С. После очистки – горючее для тракторов, реактивных самолётов и ракет.
4. В следующей фракции получают газойль (выше 275 С) – дизельное топливо.
5. Остаток после перегонки – мазут разделяют на фракции: соляровые масла – дизельное топливо, смазочные масла (автотракторные, авиационные, индустриальные и другие), вазелин (основа для косметических средств и лекарств). Из некоторых сортов нефти получают парафин (для производства спичек, свечей и др.). После отгонки остаётся гудрон. Его широко применяют в дорожном строительстве.
Установка для перегонки нефти состоит из:
1. трубчатой печи;
2. ректификационной колонны;
3. холодильника.
Главный недостаток перегонки – малый выход бензина (не более 20%).
Крекингом называется процесс расщепления углеводородов, содержащихся в нефти, в результате которого образуются углеводороды с меньшим числом атомов углерода в молекуле.
C6H14 à C8H18 + C8H16
гексадекан октан октен
Пиролизом называется разложение органического вещества без доступа воздуха при высокой температуре.
| Термический крекинг | Каталитический крекинг |
| Расщепление углеводородов происходит при сравнительно высокой температуре (470 – 550 С). Процесс протекает медленно, образуются углеводороды с неразветвлённой цепью атомов углерода. | Расщепление молекул углеводородов протекает в присутствии катализаторов и при более низкой температуре (450 – 500 С). По сравнению с термическим крекингом процесс протекает значительно быстрее, при этом происходит не только расщепление молекул углеводородов, но и их изомеризация, то есть образуются углеводороды с разветвлённой цепью атомов. |
| БЕНЗИН | |
| Много непредельных углеводородов (обладает больше детонационной стойкостью, чем бензин прямой перегонки). В бензине термического крекинга содержится много непредельных УВ, которые легко окисляются и полимеризуются. Поэтому этот бензин менее устойчив при хранении. При его сгорании могут засориться различные части двигателя. Для устранения этого вредного воздействия к такому бензину добавляют антиокислители. | Бензин каталитического крекинга по сравнению с бензином термического крекинга обладает ещё большей детонационной стойкостью, ибо в нём содержаться УВ с разветвлённой цепью углеродных атомов. В бензине каталитического крекинга непредельных УВ содержится меньше, и поэтому процессы окисления и полимеризации в нём не протекают. Такой бензин более устойчив при хранении. |
Кокс
Одним из основных способов получения углеводородов (в том числе и ароматических) является коксование (пиролиз) каменного угля.
При нагревании каменного угля сложные органические вещества, входящие в его состав, постепенно разлагаются с образованием летучих продуктов. Последние поступают в общий газосборник, где из них конденсируется каменная смола. Из неё путём фракционной дистилляции получают гомологи бензола, фенол и другие вещества.
В газосборнике одновременно со смолой конденсируется и вода, в которой растворяются аммиак, сероводород, фенол и другие вещества. Из надсмольной воды в специальной колонне отгоняется аммиак, а затем и другие продукты.
Коксовый газ охлаждают и пропускают через электрофильтры для отделения смолы. Затем из несконденсировавшегося газа извлекают аммиак и ароматические углеводороды (бензол). С целью извлечения аммиака газ пропускают через раствор серной кислоты и получают сульфат аммония – азотное удобрение. Из коксового газа выделяются водород и этилен для различных синтезов. Газ после очистки используется в качестве топлива в промышленности и быту.
Вопрос №29
