Принципы протекания ионообменных реакций
Реакции в растворах электролитов, при которых составные части (ионы) одного вещества обмениваются с составными частями другого и при которых не происходит изменения зарядов ионов, входящих в соединения, называют ионообменными реакциями.
С точки зрения теории электролитической диссоциации, в водных растворах протекают реакции не между самими электролитами, а между образованными ими ионами. При взаимодействии между ионами в растворах электролитов возможны следующие случаи:
1) образующиеся вещества — сильные электролиты, хорошо растворимые в воде и полностью диссоциирующие на ионы; в таком случае реакция не протекает;
2) одно из образующихся веществ – осадок, газ, слабый электролит (растворимый в воде) или комплексный ион, в таком случае реакция происходит.
При протекании реакции в растворе будет уменьшаться концентрация тех ионов, которые связываются между собой в малорастворимые или слабодиссоциирующие соединения.
Возможность протекания ионообменных реакций определяется правилом:
Реакции обмена в растворах электролитов протекают практически необратимо и до конца в тех случаях, когда в качестве продукта получаются осадки (малорастворимые вещества), газы (или легколетучие вещества), слабые электролиты (малодиссоциирующие соединения) и комплексные ионы (также малодиссоциирующие).
Соответственно, ионообменные реакции можно свести к четырём типам: реакции, идущие с образованием:
– осадков,
– газов,
– слабых электролитов;
– комплексных ионов (комплексных соединений).
Для каждого из случаев приведем примеры:
1. Образование осадков
AgNO3 + NaCl = AgCl↓ + NaNO3;
Ag+ + NO3– + Na+ + Cl– = AgCl↓ + Na+ + NO3–;
Ag+ + Cl– = AgCl↓.
2. Образование газов
Na2S + H2SO4 = Na2SO4 + H2S;
2Na+ + S2– + 2H+ + SO42– = 2Na+ + SO42– + H2S↑;
2H+ + S2– = H2S↑.
3. Образование слабых электролитов:
а) воды
NaOH + HCl = NaCl + H2O
Na+ + OH– + H+ + Cl– = Na+ + Cl– + H2O;
H+ + OH– = H2O
б) слабого основания
NH4Cl + KOH = NH4OH + KCl;
NH4+ + Cl– + K+ + OH– = NH4OH + K+ + Cl–-;
NH4+ + OH– = NH4OH
в) слабой кислоты
2СH3COONa + H2SO4 = 2CH3COOH + 2Na2SO4
2CH3COO– + 2Na+ +2H+ + SO42– = 2CH3COOH + 2Na+ + SO42–
2CH3COO– + H+ = CH3COOH
г) комплексного иона
HgI2 + 2KI = K2[HgI4]
HgI2 + 2K+ + I– = 2K+ = [HgI4]2–
HgI2 + I– = [HgI4]2–
Если при взаимодействии растворов электролитов не образуется ни одного из указанных видов соединений, то это означает, что химического взаимодействия не происходит. Тогда имеют место реакции, которые протекают одновременно в противоположных направлениях, т.е. обратимые, а система находится в состоянии химического равновесия.
При составлении ионообменных реакций, следует пользоваться Таблицей растворимости (см. табл. 4) оснований и солей в воде. При написании ионных и ионно-молекулярных уравнений малорастворимые (осадки, газы) и малодиссоциирующие соединения (слабые электролиты) записывают в виде молекул или комплексных ионов. Сильные электролиты, как полностью диссоциированные, записывают в диссоциированном виде.
Примеры решения задач
Задание: написать молекулярное, ионно-молекулярное и краткое ионное уравнения реакции взаимодействия растворов хлористого бария и сернокислого натрия.
Разобьём решение задачи на этапы:
1. Запишем молекулярное уравнение реакции:
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl.
4 Таблица
Растворимость оснований и солей в воде
| H+ | Li+ | K+ | Na+ | NH4+ | Ba2+ | Ca2+ | Mg2+ | Sr2+ | Al3+ | Cr3+ | Fe2+ | Fe3+ | Ni2+ | Co2+ | Mn2+ | Zn2+ | Ag+ | Hg2+ | Pb2+ | Sn2+ | Cu2+ | ||
| ОН– | P | P | P | P | P | M | H | M | H | H | H | H | H | H | H | H | — | — | H | H | H | ||
| F– | Р | М | P | P | P | M | H | H | H | M | H | H | H | P | P | P | P | P | — | H | P | P | |
| Сl– | Р | Р | P | P | P | P | P | Р | P | P | P | P | P | P | P | P | P | H | P | M | P | P | |
| Вr– | Р | Р | P | P | P | P | P | P | P | P | P | P | P | P | P | P | P | H | M | M | P | P | |
| I– | Р | Р | P | P | P | P | P | P | P | P | ? | P | ? | P | P | P | P | H | H | H | M | P | |
| S2– | Р | Р | P | P | P | — | — | — | H | — | — | H | — | H | H | H | H | H | H | H | H | H | |
| HS– | Р | Р | P | P | P | P | P | P | P | ? | ? | ? | ? | ? | H | ? | ? | ? | ? | ? | ? | ? | |
| SO32– | Р↑ | Р | P | P | P | H | H | M | H | ? | — | H | ? | H | H | ? | M | H | H | H | ? | ? | |
| HSO32– | Р | ? | P | P | P | P | P | P | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | |
| SO42– | Р | Р | P | P | P | H | M | P | H | P | P | P | P | P | P | P | Р | M | — | H | P | P | |
| HSO42– | Р | Р | P | P | P | ? | ? | ? | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | H | ? | ? | |
| NO3– | Р | Р | P | P | P | P | Р | P | P | P | P | P | P | P | P | P | P | P | P | P | — | P | |
| NO2– | Р | Р | P | P | P | P | Р | P | P | ? | ? | ? | ? | P | M | ? | ? | M | ? | ? | ? | ? | |
| PO43– | Р | Н | P | P | — | H | H | H | H | H | H | H | H | H | H | H | H | H | H | H | H | H | |
| HPO42– | Р | ? | P | P | P | H | H | M | H | ? | ? | H | ? | ? | ? | H | ? | ? | ? | M | H | ? | |
| H2PO4– | Р | Р | P | P | P | P | P | P | P | ? | ? | P | ? | ? | ? | P | P | P | ? | — | ? | ? | |
| CO32– | Р↑ | Р | P | P | P | H | H | H | H | ? | ? | H | ? | H | H | H | H | H | ? | H | ? | H | |
| HCO3– | Р | Р | P | P | P | P | P | P | P | ? | ? | P | ? | ? | ? | ? | ? | ? | ? | P | ? | ? | |
| CH3COO– | Р | Р | P | P | P | P | P | P | P | — | P | P | — | P | P | P | P | P | P | P | — | P | |
| SiO32– | Н | Н | P | P | ? | H | H | H | H | ? | ? | H | ? | ? | ? | H | H | ? | ? | H | ? | ? | |
| Р –растворяется (> 1 г в 100 г H2O) | М — мало растворяется (от 0,1 г до 1 г в 100 г H2O) | ||||||||||||||||||||||
| “— “ — разлагается водой или не существует | Н — не растворяется (< 0,1 г в 100 г H2O) | ||||||||||||||||||||||
| “↑ “ — разлагается с выделением газа | “?“ — нет достоверных сведений о существовании соединения | ||||||||||||||||||||||
2. Переписываем это уравнение, изобразив хорошо диссоциирующие вещества в виде ионов, а вещества, уходящие из сферы реакции — в виде молекул:
Ba2+ + 2Cl– + 2Na+ + SO42– = BaSO4↓ + 2Na+ + 2Cl–
Это ионно-молекулярное уравнение реакции (также его называют ионным уравнением).
3. Исключаем из обеих частей равенства одинаковые ионы, т.е. не участвующие в реакции:
Ba2+ + 2Cl– + 2Na+ + SO42–= BaSO4↓ + 2Na+ + 2Cl–
4. Записываем краткое ионное уравнение реакции (также его называют сокращенным ионно-молекулярным уравнением) в окончательном виде:
Ba2+ + SO42– = BaSO4↓
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Содержание работы:
1. После ознакомления с теоретическим материалом выполнить опыты 1 и 2 и записать наблюдения.
2. Сделать общий вывод о том, в каких случаях протекают ионообменные реакции, на основании экспериментальных данных.
Опыт 1. Реакции, протекающие с образованием
малорастворимых веществ
В две пробирки налить по 2-3 мл. растворов: в одну — сульфат натрия Na2SO4, в другую сульфат цинка ZnSO4. В каждую из пробирок прибавить по такому же объёму раствора хлорида бария BaCl2. В обеих пробирках образуется осадок — сульфат бария BaSO4. Написать молекулярные, ионно-молекулярные уравнения реакций и одно общее краткое ионное уравнение. Под формулой BaSO4 указать цвет осадка.
Опыт 2. Реакции, протекающие с образованием
малодиссоциирующих веществ
а) Налить в пробирку 2-3 мл раствора уксуснокислого натрия CH3COONa и добавить немного раствора соляной кислоты. Образующаяся при реакции уксусная кислота обнаруживается по запаху.
Написать молекулярное, ионно-молекулярное и краткое ионное уравнения реакции.
б) В небольшом количестве воды взболтать щепотку растёртого в порошок мела CaCO3 и прилить немного раствора соляной кислоты. Какой газ выделяется при этом? Составить молекулярное, ионно-молекулярное и краткое ионное уравнения реакции.
КОНТРОЛЬНОЕ ЗАДАНИЕ
Cоставьте ионно-молекулярные уравнения следующих
реакций:
Al2(SO4)3 + Pb(NO3)2 →
ZnS + HCl →
Fe(OH)3 + HNO3 →
HCN + NaOH →
Cu(OH)2 + Na2S →
Cu(OH)2 + H2S →
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какие вещества называются электролитами?
2. Что такое электролитическая диссоциация?
3. Какие вещества называются сильными, средними и слабыми электролитами?
4. Какие реакции называют ионообменными?
5. В каких случаях происходят ионообменные реакции?
6. Как определяется направление ионообменных реакций?
7. Уметь составить ионно-молекулярные уравнения реакций при взаимодействии двух данных электролитов, пользуясь таблицей растворимости.
ЛАБОРАТОРНАЯ РАБОТА
«ПРОИЗВЕДЕНИЕ РАСТВОРИМОСТИ»
Цель работы: изучение зависимости процессов образования или растворения осадков от значений произведений растворимости малорастворимых соединений.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Произведение растворимости
Возьмем какую-либо трудно растворимую соль, например, AgCl и приведем ее в соприкосновение с водой. При этом ионы Ag+ и Cl–, испытывая притяжение со стороны близлежащих диполей воды, будут постепенно отрываться от поверхности кристаллов и в виде гидратированных ионов переходить в раствор, т.е. происходит процесс растворения. Наряду с этим происходит и противоположный процесс — осаждения ионов Ag+ и Cl– из раствора. Гидратированные ионы Ag+ и Cl–, сталкиваясь при своем движении с поверхностью кристаллов AgCl, испытывают притяжение со стороны противоположно заряженных ионов кристаллической решетки. Они, в некоторых случаях, дегидратируются (теряют диполи воды) и осаждаются на поверхности кристалла. Протекание взаимно противоположных процессов (растворения и осаждения) приводит к состоянию динамического равновесия, при котором в единицу времени ровно столько ионов Ag+ и Cl– покидает поверхность твердой фазы, сколько их осаждается на поверхности этой фазы из раствора. При наступлении равновесия дальнейшее накопление ионов в растворе, как и их осаждение из раствора, прекращается и получается насыщенный раствор соли. Следовательно, насыщенным раствором называется раствор, находящийся в динамическом равновесии с твердой фазой (осадком).
Напишем выражения для скоростей растворения υ1 и осаждения υ2. Скорость υ1 (т.е. количество ионов, отдаваемых в раствор единицей поверхности твердой фазы в единицу времени) пропорциональна числу ионов, находящихся на единице поверхности. Это число не изменяется с течением времени, поэтому скорость растворения можно считать постоянной при неизменной температуре:
υ1 = K1 . (8)
Скорость υ2 (процесса осаждения ионов Ag+ и Cl– на поверхности кристаллов) зависит от числа столкновений этих ионов в единицу времени с единицей поверхности. Если бы в растворе не существовало межионных сил, уменьшающих скорость движения ионов, а значит, и число их столкновений с твердой фазой, то число этих столкновений было бы пропорционально концентрации ионов Ag+ и Cl– в растворе. Чтобы учесть действие межионных сил, надо концентрации ионов заменить их активностями:
υ2 = K2 · aAg+ · aCl– , (9)
где К2 – коэффициент пропорциональности, т.е. величина постоянная при данной температуре.
Поскольку при равновесии скорости растворения и осаждения одинаковы, то равны и правые части формул (8) и (9),
следовательно:
K1 = K2 · aAg+ · aCl– ,
откуда можно выразить:
aAg+ · aCl– = 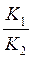 = ПРAgCl .
= ПРAgCl .
Таким образом, произведение активностей ионов данного малорастворимого электролита в насыщенном растворе есть величина постоянная при данной температуре. Эта константа характеризует способность вещества растворяться и называется произведением растворимости, обозначают ее ПР. Растворимость и ПР некоторых малорастворимых электролитов приведены в таблице 5.
Если в уравнении диссоциации электролита коэффициенты, стоящие при отдельных ионах, не равны единице, то значения активностей ионов входят в выражение произведения растворимости в степенях, равных соответствующим коэффициентам:
Ca(PO4)2 = 3Ca2+ + 2PO43–
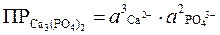
или
Ag2SO4 = 2Ag+ + SO42–
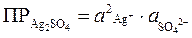 .
.
5 Таблица
Растворимость и ПР малорастворимых электролитов при температуре 18°С
| Формула вещества | Растворимость (моль/л) | ПР | Формула вещества | Растворимость (моль/л) | ПР |
| Mg(OH)2 | 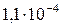 | 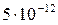 | MnS | 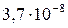 | 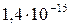 |
| BaCO3 | 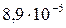 | 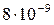 | Zn(OH)2 | 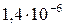 | 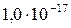 |
| BaC2O4 | 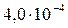 | 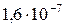 | ZnS | 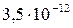 | 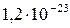 |
| BaCrO4 | 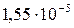 | 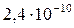 | NiS | 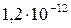 | 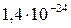 |
| BaSO4 | 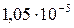 | 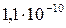 | AgBr | 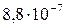 | 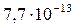 |
| SrCO3 | 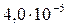 | 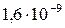 | AgCl | 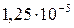 | 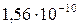 |
| SrC2O4 | 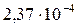 | 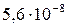 | AgI | 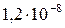 | 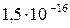 |
| SrSO4 | 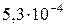 | 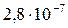 | Ag2S | 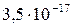 | 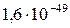 |
| CaCO3 | 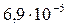 | 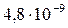 | PbCl2 | 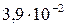 | 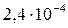 |
| CaC2O4 | 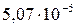 | 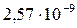 | PbI2 | 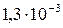 | 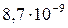 |
| CaSO4 | 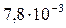 | 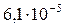 | PbS | 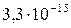 | 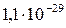 |
| Fe(OH)2 | 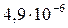 | 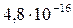 | PbSO4 | 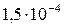 | 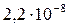 |
| Fe(OH)3 | 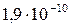 | 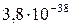 | HgS | 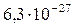 | 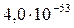 |
| FeS | 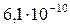 | 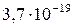 | CuS | 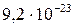 | 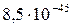 |
| Mn(OH)2 | 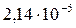 | 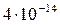 | CdS | 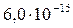 | 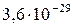 |
Так как активности ионов равны их концентрациям, умноженным на коэффициент активности f для соответствующего иона, то выражение ПРAgCl можно записать в следующем виде:
ПРAgCl = fAg+ ·[Ag+] · fCl– ·[Cl-] .
Поскольку AgCl — очень мало растворимое вещество, то концентрация его ионов в насыщенном растворе также очень мала, а межионные силы практически не играют роли. Поэтому без заметной погрешности коэффициенты активности можно принять равными единице:
fAg+ = fCl– = 1.
При этом получим приближенное уравнение, которое вполне удовлетворительно можно использовать в практических расчетах:
ПРAgCl = [Ag+]·[Cl–].
1.2. Влияние одноименных ионов на растворимость
и солевой эффект
Согласно правилу произведения растворимости, в тот момент, когда произведение концентраций ионов (в общем случае — активностей ионов) данного малорастворимого электролита (так называемое «ионное произведение») достигнет величины произведения растворимости при данной температуре, раствор этого электролита становится насыщенным. Если ионное произведение меньше произведения растворимости, и раствор имеет меньшую концентрацию, чем в состоянии насыщения, он является ненасыщенным.
Если ионное произведение превысит произведение растворимости, раствор станет пересыщенным и должен будет часть вещества выделить в виде осадка. Например, для AgCl имеем:
1) в насыщенном растворе: [Ag+]·[Cl–] = ПРAgCl
2) в ненасыщенном растворе: [Ag+]·[Cl–] < ПРAgCl
3) в пересыщенном растворе: [Ag+]·[Cl–] > ПРAgCl
Можно ненасыщенный раствор электролита сделать насыщенным и даже пересыщенным, прибавляя к нему электролит с одноименным ионом. Например, если к ненасыщенному раствору PbCl2 добавлять понемногу HCl или NaCl, то ионное произведение, бывшее сначала меньшим, чем ПР, ( 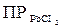 =2,4
=2,4 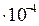 ) постепенно достигнет и, наконец, превысит указанное значение ПР. Раствор из ненасыщенного превратится в насыщенный, а затем пересыщенный раствор.
) постепенно достигнет и, наконец, превысит указанное значение ПР. Раствор из ненасыщенного превратится в насыщенный, а затем пересыщенный раствор.
Таким образом, растворимость малорастворимых электролитов понижается при введении в их растворы каких-либо сильных электролитов с одноименным ионом.
Опыт показывает, что на растворимость электролитов влияют также и те соли, которые не имеют с электролитом общего иона. Например, растворимость PbSO4 в присутствии таких солей, как KNO3, NaNO3, повышается и тем сильней, чем выше концентрация соли. Это явление называется солевым эффектом.
Солевой эффект легко объясняется, если использовать точное уравнение ПР:
[Pb+2][SO42-]· 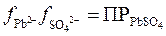 ,
,
откуда следует, что:
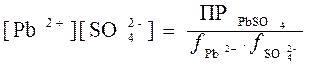 .
.
Поскольку величина 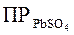 постоянна, а коэффициенты активности
постоянна, а коэффициенты активности 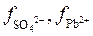 при введении в раствор каких угодно ионов обычно понижаются (табл. 6) из-за возрастания межионных сил взаимодействия, то произведение [Pb2+][SO42–], а, следовательно, и растворимость PbSO4 возрастают. Физическая причина этого явления заключается в том, что стесненные в своих движениях межионными силами, ионы Pb2+ и SO42– будут реже сталкиваться с поверхностью кристаллов PbSO4. Это дает процессу растворения перевес над процессом осаждения ионов из раствора.
при введении в раствор каких угодно ионов обычно понижаются (табл. 6) из-за возрастания межионных сил взаимодействия, то произведение [Pb2+][SO42–], а, следовательно, и растворимость PbSO4 возрастают. Физическая причина этого явления заключается в том, что стесненные в своих движениях межионными силами, ионы Pb2+ и SO42– будут реже сталкиваться с поверхностью кристаллов PbSO4. Это дает процессу растворения перевес над процессом осаждения ионов из раствора.
6 Таблица
Значения коэффициентов активности
| Ионная сила раствора, m | 0,001 | 0,005 | 0,01 | 0,05 | 0,1 |
| Значения f для однозарядных ионов | 0,96 | 0,95 | 0,93 | 0,85 | 0,80 |
| Значения f для двухзарядных ионов | 0,86 | 0,80 | 0,74 | 0,56 | 0,46 |
1.3. Растворимость осаждаемого соединения
и образование осадков
Особенно полезно использование правила ПР в тех случаях, когда соответствующий осадок образуется в результате химической реакции. Например, смешаем раствор соли свинца с раствором NaCl. При этом станет возможным образование осадка PbCl2. Но будет или не будет происходить это осаждение в действительности, зависит от того, окажется ли раствор соли пересыщенным. Это произойдет, только если ионное произведение [Pb2+][Cl–]2 превысит величину 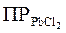 , равную 2,4
, равную 2,4 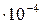 . Исходя из правила ПР можно рассчитать теоретически, будет ли выпадать осадок этой соли. Например, при смешении равных объемов 0,1М растворов Pb(NO3)2 и NaCl объем раствора увеличится вдвое, а концентрации каждого вещества вдвое уменьшатся, т.е. концентрации ионов составят:
. Исходя из правила ПР можно рассчитать теоретически, будет ли выпадать осадок этой соли. Например, при смешении равных объемов 0,1М растворов Pb(NO3)2 и NaCl объем раствора увеличится вдвое, а концентрации каждого вещества вдвое уменьшатся, т.е. концентрации ионов составят:
[Pb2+] = 0,05 моль/л ; [Cl–] = 0,05 моль/л.
Ионное произведение для полученной смеси растворов вычислим из выражения:
[Pb2+][Cl–]2 = 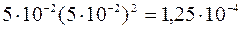 .
.
Рассчитанная величина ионного произведения меньше величины 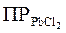 = (
= ( 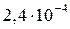 ), поэтому раствор является ненасыщенным, осадок не выпадает.
), поэтому раствор является ненасыщенным, осадок не выпадает.
При смешении 0,1М раствора Pb(NO3)2 с 1М раствором NaCl концентрации ионов составят:
[Pb2+] = 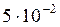 моль/л ; [Cl–] = 0,5 =
моль/л ; [Cl–] = 0,5 = 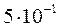 моль/л.
моль/л.
Ионное произведение будет равно:
[Pb2+][Cl–]2 = 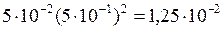 .
.
Полученная величина намного превышает произведение растворимости PbCl2 , равное 2,4·10–4. Поэтому раствор соли PbCl2 является пересыщенным и часть соли выпадет в осадок.
В ряде случаев большое значение имеет полнота осаждения, например, когда ставится задача выделить ценный компонент из раствора или при осуществлении гравиметрического метода химического анализа, когда исследуемое вещество или ион необходимо перевести из растворенного состояния в осадок (по массе осадка судят затем о содержании вещества в растворе).
Совершенно нерастворимых в воде веществ не существует, и величина произведения растворимости никогда не равна нулю, поэтому, ни одно осаждение иона не может быть совершенно полным. Всегда часть осаждаемого иона, соответствующая величине ПР осаждаемого соединения, остается в растворе. Если эта часть очень мала, условно можно считать осаждение практически полным. Но нередки случаи, когда даже условно осаждение не является полным.
Осаждение всегда тем полнее, чем меньше растворимо соединение, в виде которого осаждается ион. Например, ион Pb2+ можно осадить в виде хлорида, сульфата или сульфида. Данные по растворимости этих солей и величины ПР приведены в таблице 7.
7 Таблица
| Вещество | PbCl2 | PbSO4 | PbS |
| Растворимость, моль/л | 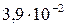 | 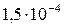 | 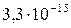 |
| ПР | 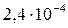 | 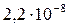 | 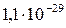 |
Из сопоставления приведенных значений видно, что наиболее растворимым соединением является хлорид, а наименее растворимым — сульфид свинца. Следовательно, в виде PbS свинец может быть осажден наиболее полно, а в виде PbCl2 — наименее полно.
Примеры решения задач
Пример 1. Вычислить ПРAgCl, если известно, что насыщенный раствор AgCl содержит 1,8 10–3 г этой соли в 1л при 25°С.
Решение. Определим молярную концентрацию насыщенного раствора AgCl:
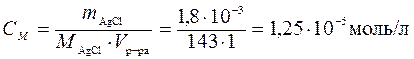 ,
,
где МAgCl — молярная масса хлорида серебра, 143 г/моль.
Поскольку каждая молекула AgCl дает при растворении по одному иону Ag+ и Cl–, (это так называемый бинарный электролит), то концентрации ионов Ag+ и Cl– в насыщенном растворе соли будут такими же:
[AgCl] = [Ag]+ = [Cl–] = 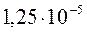 моль/л.
моль/л.
Поэтому рассчитываем ПР:
ПРAgCl= [Ag+] [Cl–] = 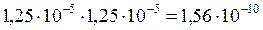 .
.
Пример 2. Вычислить 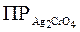 , если насыщенный раствор при 25°С содержит
, если насыщенный раствор при 25°С содержит 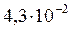 г этой соли в 1л.
г этой соли в 1л.
Решение. Вычислим молярную концентрацию насыщенного раствора Ag2CrO4:
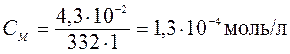 ,
,
где 332 — молярная масса хромата серебра, г/моль.
Так как из одной молекулы Ag2CrO4 при растворении образуется 2 иона Ag+ и один ион CrO42–:
Ag2CrO4 = 2Ag+ + CrO42– ,
то их концентрации в насыщенном растворе составят:
[CrO42–] = 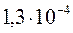 моль/л ,
моль/л ,
[Ag+] = 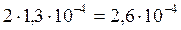 моль/л .
моль/л .
Рассчитываем ПР:
ПРAgCl= [Ag+]2·[CrO42–] = 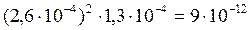 .
.
Обратите внимание на то, что растворимость AgCl (1,25·10–5) меньше, чем растворимость Ag2CrO4 ( 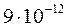 ). Это объясняется тем, что при вычислении
). Это объясняется тем, что при вычислении 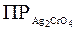 приходится возводить в квадрат малую величину — концентрацию ионов Ag+ (
приходится возводить в квадрат малую величину — концентрацию ионов Ag+ ( 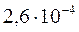 ), чего не делается при вычислении ПРAgCl .
), чего не делается при вычислении ПРAgCl .
Таким образом, о сравнительной растворимости каких-либо электролитов можно судить по величинам их произведений растворимости только в тех случаях, когда их формулы построены однотипно: AgCl, BaSO4, CaCO3 или Ag2CrO4, Ag2CO3, PbI2.
Пример 3. Определить растворимость Mg(OH)2 при 25°С, если произведение растворимости его равно 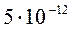 .
.
Решение. Примем искомую величину — растворимость Mg(OH)2 за х моль/л.
Уравнение диссоциации:
Mg(OH)2 = Mg2+ + 2OH–.
В результате диссоциации х молей Mg(OH)2 в растворе создаются следующие концентрации ионов:
[Mg+2] = x; [OH–] = 2x .
Тогда:
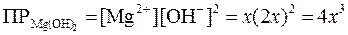 ;
;
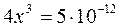 ;
;
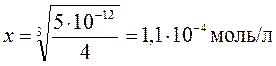 .
.
Чтобы определить растворимость в г/л, необходимо найденную величину умножить на молярную массу Mg(OH)2, которая равна 58 г/моль:
Растворимость Mg(OH)2 = 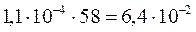 г/л.
г/л.
Пример 4. Рассчитать растворимость йодата бария Ba(IO3)2 в 0,03 М растворе Ba(NO3)2 приближенно и с учетом коэффициентов активности ионов.
Решение
1) Приближенный расчет
При диссоциации соли на один ион Ва2+ образуется 2 иона IO–3:
Ba(IO3)2 = Ba2+ + 2IO3–.
Поскольку концентрация насыщенного раствора Ba(IO3)2 при температуре 25°С равна 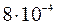 моль/л, то
моль/л, то
[Ba2+] = 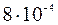 моль/л;
моль/л;
[IO3–] = 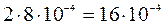 моль/л;
моль/л;
и следовательно:
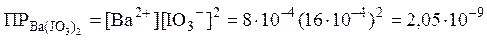 .
.
Обозначим растворимость Ba(IO3)2 в присутствии Ba(NO3)2 через х моль/л. Тогда концентрация ионов [IO3–] = 2х.
Концентрация ионов Ва2+ складывается из ионов, образующихся при диссоциации раствора Ba(NO3)2 и ионов, образующихся в результате растворения осадка Ba(IO3)2 (их концентрация равна х). Следовательно, в присутствии 0,03М Ba(NO3)2 произведение растворимости Ba(IO3)2 составит:
[Ba+2][IO3–]2 = (0,03 + х)(2х)2 = 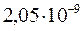 .
.
По сравнению с величиной 0,03, величиной х, как очень малой, можно пренебречь; тогда:
0,12х2 = 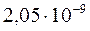 ,
,
откуда
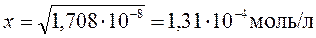 .
.
Следовательно, расчет по упрощенной формуле ПР дает, что растворимость Ba(IO3)2 при замене воды 0,03 М раствором Ba(NO3)2 понизится с 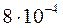 моль/л до
моль/л до 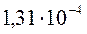 , т.е. примерно
, т.е. примерно
в 6 раз.
2) Расчет с учетом коэффициентов активности
Произведем вычисления по точной формуле:
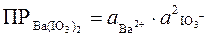
Для определения активностей ионов необходимо величины их концентраций умножить на коэффициенты активности. Коэффициенты активности зависят от ионной силы раствора, которая определяется по формуле:
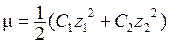 ,
,
где С — молярные концентрация ионов; z — их степень окисления.
Определим ионную силу в насыщенном растворе Ba(IO3)2:
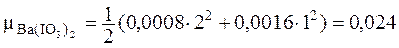 .
.
Путем интерполяции величин коэффициентов активности, приведенных в таблице Х, найдем, что ионной силе 0,0024 отвечают значения 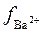 = 0,84;
= 0,84; 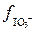 = 0,96.
= 0,96.
Интерполяцию производим следующим образом. Значение
m = 0,0024 лежит между значениями 0,001 и 0,005, разница между которыми 0,004. Этой разнице в величинах mдля двухвалентных ионов отвечает уменьшение f от 0,86 до 0,8, т.е. 0,06. Составим пропорцию:
0,004 —— 0,06
0,0014 —— х ;
откуда 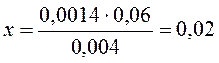 .
.
Затем рассчитываем:
fBa2+=0,86 – 0,02 = 0,84.
Аналогично производим расчет коэффициент активности для иодат-иона.
Рассчитываем активности ионов:
aBa2+= 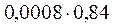 ;
;
aIO3– = 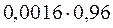 .
.
Точное значение ПР соли составит:
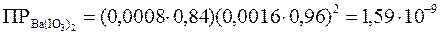 .
.
Из найденной точной величины 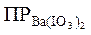 , вычислим растворимость Ba(IO3)2 в 0,03М растворе Ba(NO3)2. Для этого снова определим ионную силу раствора. Поскольку Ba(IO3)2 дает в раствор очень мало ионов по сравнению с Ba(NO3)2, для вычисления ионной силы можно учитывать только присутствие Ba(NO3)2:
, вычислим растворимость Ba(IO3)2 в 0,03М растворе Ba(NO3)2. Для этого снова определим ионную силу раствора. Поскольку Ba(IO3)2 дает в раствор очень мало ионов по сравнению с Ba(NO3)2, для вычисления ионной силы можно учитывать только присутствие Ba(NO3)2:
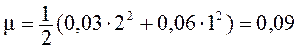 .
.
Этой ионной силе отвечают следующие значения коэффициентов активности ионов: 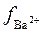 = 0,48;
= 0,48; 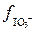 =0,81.
=0,81.
Обозначим неизвестную нам величину молярной концентрации Ba(IO3)2 через х, при этом [IO3-] =2х.
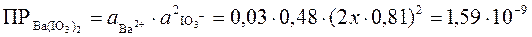 ;
;
х = 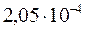 моль/л.
моль/л.
Таким образом, при точном вычислении получается, что в присутствии 0,03 моль/л Ba(NO3)2 растворимость Ba(IO3)2 понизится с 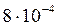 моль/л до
моль/л до 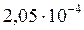 моль/л, т.е. в 4 раза (вместо шестикратного уменьшения, полученного при приближенном расчете).
моль/л, т.е. в 4 раза (вместо шестикратного уменьшения, полученного при приближенном расчете).
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Содержание работы:
1. После ознакомления с теоретическим материалом выполнить опыты и записать результаты наблюдений и уравнения
реакций.
2. На основании эксперимента
