II. Теория кристаллического поля
Достоинство этой теории в том, что она объясняет магнитные свойства комплексов и их окраску. Между центральным ионом и лигандами осуществляется ионная или ионо-дипольная связь. При этом учитывается заряд иона-комплексообразователя и его электронная структура, а лиганды рассматривают как бесструктурные заряженные точки. 5 незаполненных d – орбиталей центрального иона имеют одинаковую энергию и называются «вырожденные». При образовании комплексного иона лиганды по-разному действуют на d – орбитали и происходит их расщепление:
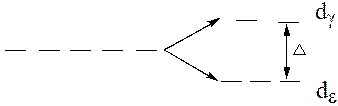
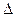 - энергия расщепления, она может быть определена по спектрам поглощения. Величина её зависит как от природы центрального иона, так и от природы лигандов. По величине
- энергия расщепления, она может быть определена по спектрам поглощения. Величина её зависит как от природы центрального иона, так и от природы лигандов. По величине 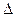 лиганды образуют спектрохимический ряд:
лиганды образуют спектрохимический ряд:
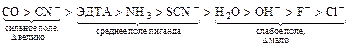
а) В случае сильного поля электроны заселяют de и dg не по правилу Гунда: сначала полностью de орбитали, а затем оставшиеся dg. Количество неспаренных электронов минимально и комплекс как правило диамагнитен, низкоспиновый.
б) Если лиганды создают слабое поле, то  меньше и d–орбитали заселяются электронами по правилу Гунда: de и dg (все 5 орбиталей) вначале по одному электрону, а уже потом по второму. Как правило образуется комплекс парамагнитный, высокоспиновый.
меньше и d–орбитали заселяются электронами по правилу Гунда: de и dg (все 5 орбиталей) вначале по одному электрону, а уже потом по второму. Как правило образуется комплекс парамагнитный, высокоспиновый.
Цвет комплекса
Если при образовании комплексного иона все d – орбитали заселены (например у 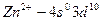 ), то комплексы как правило бесцветны. Если же d–орбитали заселены не полностью, то при затрате какой-либо энергии электроны с подуровня de переходят на верхний подуровень dg и этот переход связан с поглощением света определённой длины волны, что и приводит в результате к окраске комплекса.
), то комплексы как правило бесцветны. Если же d–орбитали заселены не полностью, то при затрате какой-либо энергии электроны с подуровня de переходят на верхний подуровень dg и этот переход связан с поглощением света определённой длины волны, что и приводит в результате к окраске комплекса.
Применение комплексных соединений в медицине
И фармации
1. Гемоглобин (М » 67000 а.е.м.) отвечает за перенос кислорода в крови, содержит группу
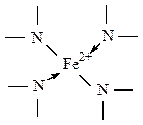
2. Хлорофиллы (пигменты), с их помощью высшими растениями и зелёными водорослями осуществляется фотосинтез.
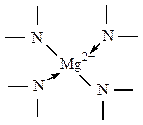
3. В организме животных и человека имеются металлоферменты, где в качестве центральных атомов выступают Fe, Zn, Co, Mo, Cu, Mn. Так, например, цинк входит в состав » 70 биологических катализаторов.
4. Комплексонометрия: раздел количественного анализа, когда в качестве рабочих растворов используют комплексоны (ЭДТУ, ЭДТА и др.).
Применяют:
а) в санэпиднадзоре при определении жёсткости воды;
б) для определения тяжёлых металлов в фармацевтических препаратах и в лекарственном растительном сырье;
в) для определения кальция в плазме крови и тяжёлых металлов в желудочном соке;
г) для определения сахара в моче;
5. для диагностики и лечения некоторых видов злокачественных опухолей используют комплексы золота и платины.
Вопросы для закрепления материала:
1.Какой комплекс получится из хлорида меди (2) и аммиака? Назовите его.
2.Запишите Кнест. для этого комплексного соединения.
