Адсорбция на границах раздела газ - раствор, жидкость - раствор
Поверхности раздела между газом и жидкостью или жидкостью и жидкостью образуются в пенах, в эмульсиях и газовых эмульсиях, в частности, в эмульсионных и аэрированных буровых растворах.
При растворении в жидкости какого-либо вещества в результате его адсорбции поверхностным слоем поверхностное натяжение жидкости меняется (увеличивается или уменьшается).
Количественная зависимость между величиной адсорбции и изменением поверхностного натяжения для разбавленных растворов
выражается уравнением Гиббса
r C RT
, (15)
C
где r - избыточная концентрация растворенного вещества на 1 м2 поверхности раствора (удельная адсорбция); С - молярная концентрация раствора; R - универсальная газовая постоянная; Т - абсолютная температура;
- изменение поверхностного натяжения раствора, соответствующее
изменению концентрации ΔС. Величину -
, характеризующуюспособность растворенного вещества уменьшать поверхностное натяжение и, следовательно, свободную энергию (при S=const), называют поверхностной активностью. Единицами измерения поверхностной активности являются Дж*м/моль или Н.м2/кмодь и 1 мН.м2/кмоль. Поверхностная активность является важнейшей адсорбционной характеристикой веществ, определяющей многие их свойства и области применения.
Из уравнения (15) следует, что если поверхностное натяжение уменьшается с увеличением концентрации (Δσ/ΔС<0), то r>0, т.е. концентрация растворенного вещества в поверхностном слое больше, чем в объеме раствора.
Если же σ увеличивается с увеличением С (Δσ/ΔС>0), то r <0, т.е. концентрация растворенного вещества в поверхностном слое меньше, чем в растворе. Увеличение концентрации растворенного вещества в поверхностном слое по сравнению с объемом называется положительной адсорбцией (или сокращенно - адсорбцией), а само вещество - поверхностно- активным (ПАВ); уменьшение концентрации - отрицательной адсорбцией, а растворенное вещество - поверхностно-инактивным.
Поверхностно-активные вещества должны обладать: 1) поверхностным натяжением меньше поверхностного натяжения растворителя, иначе самопроизвольное накопление вещества в поверхностном слое термодинамически невыгодно; 2) сравнительно малой растворимостью, так как в противном случае они стремились бы уйти с поверхности в глубь жидкости.
Поверхностно-активными веществами относительно воды являются многие органические соединения, молекулы которых содержат полярную функциональную группу (-ОН, -СОOН, -NH2, -SO3Н, -SН и др.) и неполярный углеводородный радикал. Таким образом, молекулы ПАВ имеют
двойственную природу (дифильные).
Подобные вещества содержатся и в нефтях: нафтеновые и жирные кислоты, фенолы, эфиры, металлопорфириновые комплексы, асфальтосмолистые вещества.
На поверхности раздела фаз дифильные молекулы ПАВ ориентируются таким образом, что их полярные группы погружаются в полярную жидкость (например, воду), а углеводородные радикалы выталкиваются в неполярную жидкость или в газ. Расположение адсорбированных молекул в адсорбционном поверхностном слое существенно зависит от их концентрации (рис. 12).
При низких концентрациях ПАВ в растворе и соответственно в адсорбционном слое гибкие углеводородные радикалы лежат на поверхности воды, так как между молекулами воды и радикалом существуют силы вандерваальсовского притяжения (рис. 12,а). С увеличением концентрации происходит сжатие адсорбционного слоя, углеводородные радикалы отрываются от воды, образуя агрегаты молекул (рис. 12,6),
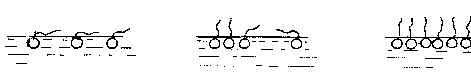
а б в
Рис. 12. Расположение молекул ПАВ в адсорбционном слое на границе раздела жидкость-газ:
а - при малых концентрациях; б -при средних концентрациях;
в - в насыщенном мономолекулярном слое (о - полярная группа, ~ - радикал).
При большой концентрации молекулы ПАВ располагаются пер- пендикулярно к поверхности раздела, образуя мономолекулярный адсорбционный слой (рис. 12,в).
Зависимости поверхностного натяжения и величины адсорбции от
концентрации растворённого ПАВ имеют вид графиков, представленных на рис. 13. Зависимость r=f(C) при постоянной температуре называется изотермой адсорбции Гиббса, а σ=f(C)-изотермой поверхностного натяжения.
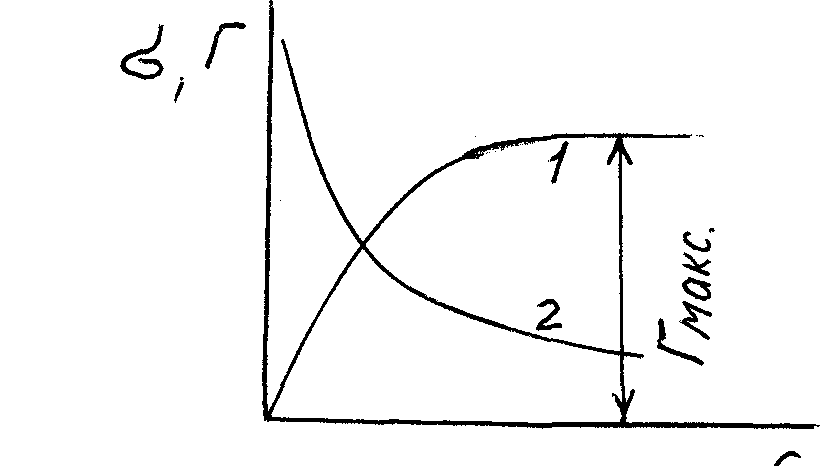
Рис. 13. Изотермы поверхностного натяжения (1) и адсорбции (2) ПАВ
По мере заполнения поверхностного слоя адсорбируемыми молекулами интенсивность уменьшения σ с увеличением концентрации ПАВ уменьшается и практически прекращается, когда адсорбция достигает максимального значения rмакс, соответствующего полному насыщению поверхности мономолекулярным слоем молекул ПАВ.
Поверхностная активность дифильных молекул ПАВ зависит от длины углеводородного радикала и природы полярной группы. Углеводородные радикалы выталкиваются из воды на поверхность, поэтому адсорбция ПАВ положительна.
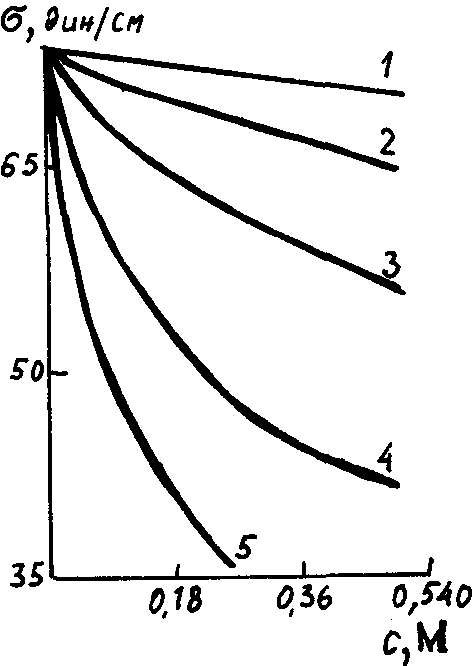
Чем длиннее неполярная углеводородная цепь, тем в большей степени молекулы ПАВ вытесняются на поверхность и тем больше снижается поверхностное натяжение (рис. 14).
Рис. 14. Поверхностное натяжение растворов
ПАВ - органических кислот:
1 - муравьиная; 2 - уксусная;
3 - пропионовая; 4 - масляная;
5 - изовалериановая
 |
Увеличение углеводородной цепи в гомологических рядах жирных кислот, спиртов, аминов на группу –СН2- увеличивает поверхностную активность вещества в 3-3,5 раза (правило - Дюкло-Траубе).
Поверхностно-инактивные вещества должны иметь более высокое, чем у растворителя, поверхностное натяжение и высокую растворимость. В противном случае они накапливались бы у поверхности. Относительно воды поверхностно-инактивными веществами являются все неорганические электролиты: кислоты, щелочи, соли. Их ионы взаимодействуют с водой сильнее, чем молекулы воды между собой. Поэтому ионы электролита втягивают в объемную фазу сильнее, чем молекулы воды. В результате поверхностный слой обедняется электролитом, т.е. имеет место отрицательная адсорбция.
С увеличением концентрации неорганического электролита поверхностное натяжение раствора повышается (рис. 15). Но в связи с тем, что адсорбция отрицательная, увеличение концентрации в поверхностном слое отстает от роста её в объеме. Поэтому поверхностное натяжение раствора с увеличением концентрации поверхностно-инактивных веществ растет очень медленно.
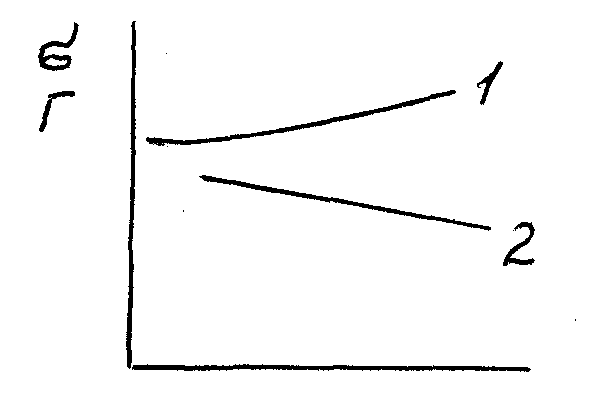
Рис. 15. Изотермы поверхностного натяжения (1) и адсорбции (2)
поверх-ностно-инактивного вещества
