Теория строения атомных ядер. Радиоактивность.
Атомное ядро - это центральная часть атома, в которой сосредоточена основная часть его массы (около 99,9%). Ядра атомов представляют собой сложные образования, структурными элементами которых являются элементарные частицы.Современное представление о строении ядра атома изложено в протонно-нейтронной теории Д. Иваненко и В. Гейзенберга (1932 г.), которая может быть сведена к следующим положениям:
1. Ядро состоит из протонов и нейтронов, их объединяют под общим названием нуклон. Число нуклонов в атомном ядре называется массовым числом (А). Так как массы протона и нейтрона в а.е.м. близки к единице, то массовое число ядра равно атомной массе, округленной до целого числа. Число протонов в ядре (Z) равно заряду ядра, совпадающему с порядковым номером элемента в периодической системы, число нейтронов можно определить по следующей формуле:
N = A - Z
При записи формул атомных ядер верхним левым индексом при химическом символе элемента указывается массовое число, нижним левым - число протонов, например, 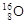 .
.
Ядра атомов, имеющие одинаковое число протонов при разном числе нейтронов (например, 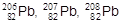 ), называются изотопами. Термин "изотоп" распространяется и на атомы, содержащие соответствующие ядра.
), называются изотопами. Термин "изотоп" распространяется и на атомы, содержащие соответствующие ядра.
2. В атомных ядрах непрерывно протекают процессы взаимопревращения протонов в нейтроны и наоборот, что обусловливает стабильность ядер. Превращения происходят в результате обмена элементарными частицами - пи-мезонами (p+; p- или p0):
p + n ® n + p+ + n ® n + p
n + p ® p + p- + р ® p + n
Время жизни пи-мезонов в ядре не превышает 10-23 - 10-24 с. Таким образом, протон и нейтрон можно рассматривать как разные квантово-механические состояния одной элементарной частицы - нуклона.
3. Между нуклонами действуют силы притяжения, называемые ядерными силами. Их действие проявляется лишь на расстояниях порядка 10-3 пм и быстро падает при удалении нуклонов друг от друга. Ядерные силы необычайно велики, следствием этого являются малые размеры атомных ядер и высокая плотность ядерного вещества, достигающая 1014 г/см3 (для сравнения плотность наиболее тяжелого металла осмия равна 22,5 г/см3).
Наряду с ядерными силами в ядре действуют электростатические силы отталкивания одноименно заряженных протонов, понижающие устойчивость ядер, особенно имеющих высокий заряд. Так, у элементов, расположенных в периодической системе после висмута (порядковый номер - 83), не существует стабильных изотопов. Лишенные зарядов нейтроны стабилизируют ядра, ослабляя взаимное отталкивание протонов. С увеличением зарядов ядер отношение N:Z в них возрастает: у элементов начала периодической системы отношение близко к единице, а с увеличением порядкового номера повышается до 1,6 у урана.
4. Энергия, которую необходимо затратить, чтобы расщепить ядро на отдельные нуклоны, называется энергией связи ядра (Есв). Такое же количество энергии выделяется при синтезе ядра из нуклонов. Энергию связи, отнесенную к одному нуклону, называют средней (удельной) энергией связи ядра:
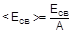
Значения средней энергии связи, в отличие от Есв, изменяются в относительно узких пределах, составляя 6 - 8 мЭв на каждый нуклон. Максимальные значения <Есв> отвечают элементам середины периодической системы, достигая 8,8 мЭв. Взаимодействие одного моля нуклонов сопровождается выделением 8,5·108 кДж, что многократно превышает тепловые эффекты обычных химических реакций. Выделение столь значительных количеств энергии в соответствии с уравнением Эйнштейна (Е = mc2) сказывается на массе ядра. Уменьшение массы ядра сравнительно с массой входящих в состав ядра нуклонов называется дефектом массы:
Dm = Z×mp + N×mn - Mx,
где mp и mn - массы протона и нейтрона, Mx - масса синтезированного ядра.
Для объяснения свойств ядер широко используется оболочечная модель (М. Гепперт-Майер, 1948 г.). Согласно этой модели ядро имеет ряд дискретных ядерных уровней, емкость которых определяется значениями ядерных квантовых чисел. Уровни заполняются нуклонами в соответствии с правилами квантовой механики по аналогии с атомными электронными уровнями. Полному заполнению энергетических уровней ядра соответствуют числа нуклонов, равные 2, 8, 14, 20, 28, 50, 82, 126 и 184. Эти числа называют магическими, а ядра, в которых они реализуются, получили название магических ядер. Магические ядра в какой-то мере аналогичны атомам благородных газов в периодической системе, они характеризуются большей устойчивостью и распространенностью в природе. Ядра могут содержать магическое число протонов ( 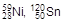 ) или нейтронов (например,
) или нейтронов (например, 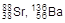 ), а также тех и других (дважды магические ядра). К дважды магическим ядрам относятся: 42He (2p,2n); 168O (8p,8n); 2814Si (14p,14n); 4020Ca (20p,20n); 20882Pb (82p,126n).
), а также тех и других (дважды магические ядра). К дважды магическим ядрам относятся: 42He (2p,2n); 168O (8p,8n); 2814Si (14p,14n); 4020Ca (20p,20n); 20882Pb (82p,126n).
Ядерные реакции - это превращения атомных ядер, обусловленные их взаимодействием с элементарными частицами или другими ядрами. В отличие от химических реакций, ядерные реакции всегда сопровождаются изменением элементного или изотопного состава.
Обычным методом осуществления ядерных реакций является метод бомбардировки, при котором ядра вещества-мишени подвергаются действию пучка частиц, энергия которых достаточна для преодоления электростатического отталкивания одноименно заряженных частиц. Ядерные реакции зачастую протекают по схеме:
X + Y ® U ® X' + Y'
Взаимодействующие частицы X и Y сливаются в короткоживущее ядро U (так называемое компаунд-ядро), которое затем распадается на частицы X' и Y'. При записи уравнения ядерных реакций принято указывать заряды и массовые числа исходных и образующихся ядер. Часто используют сокращенную форму записи подобных уравнений; при этом записывают символы исходного и полученного ядер с указанием массовых чисел, а между ними в круглых скобках через запятую указывают символы бомбардирующей и образующейся легких частиц. При такой форме записи ядро 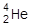 обозначается символом a, ядро атома водорода
обозначается символом a, ядро атома водорода 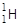 (протон) - символом р, фотон - g. Например:
(протон) - символом р, фотон - g. Например:
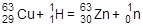 или 63Cu(p,n)Zn
или 63Cu(p,n)Zn
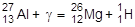 или 27Al(g,p)26Mg
или 27Al(g,p)26Mg
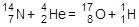 или 14N(a,p)17O
или 14N(a,p)17O
К ядерным реакциям относятся также термоядерные процессы - реакции синтеза тяжелых ядер из более легких. Термоядерным реакциям соответствуют огромные тепловые эффекты, однако для начала протекания таких реакций необходимы очень высокие температуры (порядка 106 градусов). Простейшей термоядерной реакцией является синтез ядер гелия из протонов:
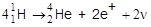 ,
,
где n - элементарная частица нейтрино.
Радиоактивность - это явление самопроизвольного распада неустойчивых атомных ядер, сопровождающееся корпускулярным или электромагнитным излучением.
Явление радиоактивности было открыто французским физиком А. Беккерелем в 1896 г. при работе с ураном и его соединениями. Фундаментальное изучение связано с именами Марии и Пьера Кюри, выделившими из урановых руд радиоактивные элементы полоний и радий, являющиеся в миллионы раз более мощными излучателями, чем уран. М. Кюри предложила и сам термин "радиоактивность". Связь радиоактивности с распадом атомных ядер была установлена Э. Резерфордом и Ф. Содди.
Системной единицей радиоактивности является беккерель (Бк). Беккерель равен активности образца, в котором происходит один акт радиоактивного распада в секунду; размерность беккереля - с-1. Несистемной единицей радиоактивности является кюри (Ки), соответствующая радиоактивности 1 г радия, 1 Ки = 3,700×1010 Бк.
Существует несколько типов радиоактивного распада, важнейшими из которых являются следующие:
1. a-Распад сопровождается испусканием двух протонов и нейтронов в виде ядра гелия 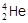 и протекает по уравнению
и протекает по уравнению
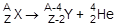
a-Распад характерен для элементов с высокими значениями заряда ядра. Все элементы, располагающиеся в периодической системе после висмута, имеют изотопы, подвергающиеся a-распаду. Примером этого типа распада может служить распад ядер радия:
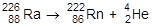
2. b-Распад сопровождается испусканием электрона (b--распад) или позитрона (b+-распад). При b--распаде ядро испускает электрон за счет превращения одного нейтрона ядра в протон:
10n ® 11p + е- + 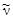
Часть энергии при распаде уносится вместе с антинейтрино ( 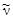 ) – частицей, лишенной заряда и отличающейся от нейтрино спином. При b--распаде заряд ядра увеличивается на единицу, массовое же число не изменяется, т.е. образуется ядро другого элемента, атомный номер которого на единицу больше, чем у исходного, например:
) – частицей, лишенной заряда и отличающейся от нейтрино спином. При b--распаде заряд ядра увеличивается на единицу, массовое же число не изменяется, т.е. образуется ядро другого элемента, атомный номер которого на единицу больше, чем у исходного, например:
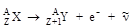 или 21083Bi ® 21084Po + е- +
или 21083Bi ® 21084Po + е- + 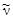
Этот тип радиоактивности присущ как легким, так и тяжелым элементам. При этом изотопы одного и того же элемента могут подвергаться как b--распаду, так и b+-распаду (позитронный распад). Позитрон – элементарная частица с положительным зарядом и массой электрона. Позитронный распад является следствием превращения одного протона в нейтрон, при этом заряд ядра уменьшается на единицу, а массовое число не изменяется.
11p ® 10n + е+ + n; 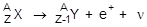
Если масса радиоактивного ядра больше массы стабильного изотопа данного элемента, то оно обычно подвергается b--распаду, если меньше - то b+-распаду. Например, масса стабильного изотопа углерода равна 12 а.е.м., ядра углерода 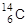 и
и 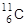 распадаются согласно уравнениям:
распадаются согласно уравнениям:
146C ® 147N + e- + 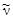 ; 116C ® 115B + е+ + n
; 116C ® 115B + е+ + n
3. Электронный захват приводит к такому же изменению ядер как и позитронный распад, его часто рассматривают как третий вид b-распада. Это явление состоит в том, что электрон, находящийся на одном из ближайших к ядру слоев, захватывается ядром. При этом один из протонов превращается в нейтрон:
11p + е- ® 10n + n; 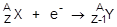 + n
+ n
Чаще всего захват электрона происходит с ближайшего к ядру К-слоя (К-захват), реже с L- или М-слоев. Электронный захват, как и b+-распад, присущ нейтронодефицитным изотопам. Например, К-захвату подвергается ядро 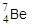 :
:
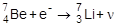
Благодаря эффекту К-захвата небольшая часть изотопов калия-40 (около 12 %) превращается в аргон:
4019K ® 4018Ar + n
Эта ядерная реакции используется при определении возраста калиевых минералов (так называемый "аргоновый метод"), аргон в минералах накапливается прямо пропорционально их возрасту.
4. Спонтанное деление ядер - самопроизвольное деление тяжелого ядра на два (реже на три или четыре) осколка, являющиеся ядрами элементов середины периодической системы. Известно очень мало изотопов, для которых спонтанное деление является единственным видом радиоактивного распада. Примером таких ядер может служить изотоп менделевия - 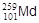 . Обычно ядра, способные к спонтанному делению, одновременно подвергаются также a- или b-распаду, являющемуся для них основным. При спонтанном делении образуются самые разнообразные осколки, однако их массы и заряды чаще всего относятся как 3:2.
. Обычно ядра, способные к спонтанному делению, одновременно подвергаются также a- или b-распаду, являющемуся для них основным. При спонтанном делении образуются самые разнообразные осколки, однако их массы и заряды чаще всего относятся как 3:2.
Рассмотренные типы радиоактивного превращения ядер часто сопровождаются гамма-излучением, связанным в основном с переходом образовавшегося ядра из возбужденного в нормальное состояние.
Если радиоактивный распад сопровождается изменением зарядов ядер, то образующиеся ядра занимают в периодической системе иные места, нежели исходные. Для характеристики подобных перемещений пользуются правилом смещения(К. Фаянс, Ф. Содди, 1913 г.): нуклид, образующийся в результате a-распада смещается в периодической системе на две клетки влево, а нуклид, образующийся в результате b--распада - на одну клетку вправо от исходного радионуклида. К правилу можно добавить, что позитронный распад и электронный захват смещают ядро на одну клетку влево, при этом b-распад на массу ядра не влияет, а испускание a-частицы изменяет массу ядра и массовое число на четыре единицы.
Основной закон радиоактивного распада - закон радиоактивной постоянной: число ядер, распадающихся в единицу времени, пропорционально их числу. Закон обусловлен тем, что распад каждого атомного ядра не зависит от поведения других ядер.
Пусть за отрезок времени t число радиоактивных ядер изменилось от N0 до N. В соответствии с законом радиоактивной постоянной скорость распада в каждый момент времени будет пропорциональна величине N:
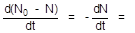 lN (1)
lN (1)
или
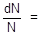 -lt (2)
-lt (2)
Коэффициент пропорциональности l называется радиоактивной постоянной или константой радиоактивного распада, значения которой зависят от природы радиоактивного изотопа. Величина, обратная радиоактивной постоянной, называется средним временем жизни ядра:
t = 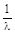
Проинтегрировав левую часть уравнения (2) в пределах от N0 до N, а правую - от нуля до t, получим математическое выражение основного закона радиоактивного распада в интегральной форме:
N = N0e-lt (3)
Следствием из закона радиоактивной постоянной является правило полураспада: отрезок времени, за который распадается половина имеющихся радиоактивных ядер, есть величина постоянная для данного изотопа, называемая периодом полураспада (Т1/2).
Если t = Т1/2, то N = 1/2N0, то в соответствии с уравнением (3):
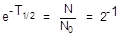 или
или 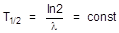
Значения периода полураспада изменяются в широком диапазоне – от нескольких долей секунды до многих миллионов лет.
Естественная радиоактивность присуща изотопам, существующим в природе. Естественные радиоактивные изотопы достаточно многочисленны и содержатся в различных природных объектах (горные породы, минералы, атмосфера, гидросфера, космические тела), к ним относятся все изотопы элементов, порядковый номер которых превышает 83. В результате непрерывно протекающего распада ядер этих изотопов Земля получает значительное количество энергии - около 5,7×1010 кДж/с. За счет этой энергии повышается температура при углублении в земные недра.
Очевидно, что на земле имеются те элементы, которые не подверглись радиоактивному распаду за 4,5 – 5 млрд. лет (время существования нашей планеты) или запасы которых постоянно пополняются за счет соответствующих ядерных превращений. Так, ядра тория 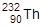 (период полураспада 1,4·1010 лет), урана
(период полураспада 1,4·1010 лет), урана 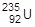 (7·108 лет),
(7·108 лет), 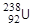 (4,5 109 лет) могли сохраниться на Земле. Другие элементы, расположенные за висмутом, постоянно образуются за счет естественного радиоактивного распада.
(4,5 109 лет) могли сохраниться на Земле. Другие элементы, расположенные за висмутом, постоянно образуются за счет естественного радиоактивного распада.
При распаде изотопов урана и тория протекает ряд последовательных ядерных превращений, при которых нуклид, образующийся на определенной стадии, становится исходным ядром для следующей стадии. Совокупность генетически связанных нуклидов, последовательно образующихся один из другого, называется радиоактивным рядом. Радиоактивный ряд начинается нуклидом с периодом полураспада, достаточным для того, чтобы этот изотоп не исчез за время существования земной коры (Т1/2 > 108 лет), завершается каким-либо стабильным изотопом. В настоящее время известны три естественных радиоактивных ряда, в которых происходят только a- и b--превращения. Все существующие в земной коре изотопы тяжелых радиоактивных элементов являются членами этих рядов.
1. Ряд урана. Родоначальником ряда является 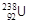 , завершает ряд стабильный изотоп свинца
, завершает ряд стабильный изотоп свинца 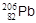 . Превращение осуществляется в 14 стадий (8 a-распадов, 6 b--распадов). Часть радиоактивного ряда урана приведена ниже:
. Превращение осуществляется в 14 стадий (8 a-распадов, 6 b--распадов). Часть радиоактивного ряда урана приведена ниже:
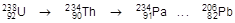
Изменение массового числа членов ряда происходит только при a-распаде, для любого нуклида ряда справедлива формула A = 4n + 2, где А - массовое число изотопа, n - целое число.
2. Ряд тория открывается изотопом 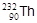 , включает 10 стадий (6 a- и 4 b--распадов) и заканчивается изотопом
, включает 10 стадий (6 a- и 4 b--распадов) и заканчивается изотопом 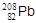 . Массовые числа членов ряда отвечают формуле A = 4n.
. Массовые числа членов ряда отвечают формуле A = 4n.
3. Ряд актиноурана. Актиноуран - одно из названий изотопа 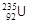 . В результате 11 ядерных превращений (7a, 4b-) заряд ядра понижается на 10 единиц, а массовое число - на 28, что приводит к образованию стабильного изотопа свинца
. В результате 11 ядерных превращений (7a, 4b-) заряд ядра понижается на 10 единиц, а массовое число - на 28, что приводит к образованию стабильного изотопа свинца 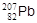 . Массовое число членов ряда соответствует формуле А = 4n +3.
. Массовое число членов ряда соответствует формуле А = 4n +3.
На определении точного соотношения количеств радиоактивного элемента и продукта его распада основаны методы определения абсолютного возраста минералов. Так называемый "свинцовый метод" определения возраста природных объектов основан на сравнении соотношений количеств изотопов 206Pb; 207Pb; 208Pb к количеству изотопа свинца-204. Изотоп 204Pb не имеет радиоактивных предшественников, поэтому его количество в земной коре остается неизменным, в то время как количества изотопов 206Pb; 207Pb и 208Pb все время нарастает в результате радиоактивного распада урана и тория. Между значениями изотопных соотношений свинцовых месторождений и их возрастом наблюдается строгая закономерность.
Четвертый ряд радиоактивности 23793Np ® 20983Bi возможно когда-то реализовывался на Земле, но начиная с нептуния (Т1/2 = 2,14×106 лет) элементы отличаются сравнительно короткими периодами полураспада (максимально 6580 лет у плутония-240, 7800 лет у америция) и поэтому подверглись распаду сравнительно быстро. В настоящее время удалось искусственно воссоздать четвертый радиоактивный ряд, образуемый изотопами, для которых массовое число А = 4n + 1. Родоначальник ряда - изотоп нептуния 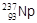 , ряд включает 7a- и 4b--превращений и заканчивается стабильным изотопом
, ряд включает 7a- и 4b--превращений и заканчивается стабильным изотопом 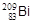 .
.
В свете представлений о радиоактивных рядах становится понятным, почему в природных образованиях можно обнаружить радиоизотопы с малыми периодами полураспада (например, полоний, периоды полураспада изотопов которого не превышают 102 года, или радон, для самого устойчивого изотопа которого период полураспада равен 2,8 сут), тогда как некоторые изотопы с периодами распада порядка сотен тысяч и миллионов лет в природе отсутствуют (например, 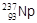 ). Действительно, ядра изотопов полония, радона, актиния, являющиеся членами радиоактивных рядов, непрерывно образуются при распаде урана и тория, тогда как количество ядер нептуния, родоначальника ряда, могло только уменьшаться.
). Действительно, ядра изотопов полония, радона, актиния, являющиеся членами радиоактивных рядов, непрерывно образуются при распаде урана и тория, тогда как количество ядер нептуния, родоначальника ряда, могло только уменьшаться.
Естественная радиоактивность присуща и некоторым элементам, имеющим стабильные изотопы. Примером такого элемента может служить калий, который представлен в земной коре, наряду со стабильным 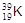 , радиоактивным изотопом
, радиоактивным изотопом 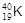 ; содержание последнего составляет 0,012% от общего числа ядер изотопов калия. Период полураспада
; содержание последнего составляет 0,012% от общего числа ядер изотопов калия. Период полураспада 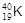 - 1,25×109 лет, этот изотоп на 88 % распадается по уравнению:
- 1,25×109 лет, этот изотоп на 88 % распадается по уравнению: