Лекция № 1. Предмет химии. Современное атомно-молекулярное учение.
ТАВРИЧЕСКИЙ НАЦИОНАЛЬНЫЙ УНИВЕРСИТЕТ
Им. В.И. ВЕРНАДСКОГО
В.Ф. ШУЛЬГИН, Н.С. ПЕВЗНЕР
ЛЕКЦИИ ПО ОБЩЕЙ И
НЕОРГАНИЧЕСКОЙ ХИМИИ
учебное пособие
для студентов нехимических специальностей
Симферополь - 2004
Учебное пособие издается по решению научно-методического совета
Таврического национального университета им. В.И. Вернадского от 21.01.04 г.
Рекомендовано методической комиссией химического факультета Таврического
национального университета им. В.И. Вернадского
Рецензент: почетный профессор Э.А.Гюннер (Таврический национальный университет
им. В.И. Вернадского)
В.Ф. Шульгин, Н.С. Певзнер. Лекции по общей и неорганической химии / Учебное пособие для студентов нехимических специальностей. Симферополь: Таврический национальный университет им. В.И. Вернадского, 2004. - 127 с.; ил.
В учебном пособии кратко освещены основные вопросы программы по общей и неорганической химии для студентов нехимических специальностей Таврического национального университета (биология, география, экология). Материал, изложенный в книге, может быть использован студентами вузов другого профиля, например, сельскохозяйственного или медицинского, а также студентами химических специальностей.
©В.Ф. Шульгин, Н.С. Певзнер, 2004
Лекция № 1. Предмет химии. Современное атомно-молекулярное учение.
Основные понятия химии, законы стехиометрии
Химия - это наука, изучающая состав, строение и свойства химических веществ, а также закономерности их взаимных превращений.
Особенностью окружающего нас мира является материальность его объектов том смысле, что они существуют вне и независимо от нашего сознания. Все известные к настоящему времени проявления материи можно свести к двум ее видам - веществу и полю. Вещество - это форма материи, носители которой имеют ненулевую массу покоя. Примерами таких носителей могут служить протон, нейтрон и электрон - элементарные частицы, из которых построены атомы. Носители свойств поля (например, фотоны) характеризуются нулевой массой покоя. Под химическим веществом подразумевают конкретный вид материи, образованный атомами химических элементов.
Особенностью материи является постоянное ее движение, под которым понимают любое изменение материального объекта. Различают несколько форм движения материи, основными из которых являются физическая, химическая и биологическая. Под химической формой движения подразумеваются превращения веществ в другие вещества, при которых сохраняются неизменными ядра атомов - носителей химических свойств материи. В основе химической формы движения лежит перестройка структуры валентных электронных оболочек атомов - явление физическое. Тем не менее, химическая форма является самостоятельным видом изменения материи и не может рассматриваться как частный случай физической формы ее движения. В свою очередь, химическая форма движения является основой биологической, поскольку в основе жизнедеятельности любого живого организма лежит сложный комплекс химических реакций.
Поскольку химия занимается изучением как химических, так физических явлений, важным является проведение границы между ними. В настоящее время критериями протекания химического процесса (химической реакции) считают:
· образование новых химических частиц;
· тепловой эффект процесса более 20-40 кДж/моль.
Тем не менее, в ряде случаев процесс не удается четко отнести к физическому или химическому. Примерами таких явлений могут служить растворение или испарение некоторых веществ. Так, процесс испарения вольфрама идет с образованием в газовой фазе двухатомных молекул W2, которые отсутствуют в кристаллическом состоянии, и сопровождается значительным по величине тепловым эффектом (770 кДж/моль). Несмотря на то, что новых химических веществ не образуется, этот процесс нельзя считать чисто физическим, в подобном случае лучше подходит термин "физико-химическое явление".
Являясь самостоятельной наукой, химия связана с другими естественными науками - физикой, биологией, геологией. Связь иногда бывает столь тесной, что на границе наук возникают новые их ветви, которые можно рассматривать как самостоятельные науки, такие, как физическая химия и биохимия, гидро- и геохимия. Широкое применение математического аппарата и вычислительной техники в современной химии привело к возникновению таких специфических наук, как математическая и компьютерная химия. В свою очередь для химии, как и для других естественных наук, характерна тенденция к дифференциации, т.е. выделению в относительно самостоятельные науки ее отдельных частей. Современная химия представляет собой комплекс наук, включающий общую и неорганическую химию, аналитическую химию, органическую химию, химию элементоорганических соединений, физическую и коллоидную химию, бионеорганическую и биоорганическую химию, квантовую и компьютерную химию, радиохимию, плазмохимию, криохимию и т.д.
Основу современной общей химии составляет ряд концепций, главными из которых являются:
· химическая атомистика (атомно-молекулярное учение);
· учение о строении вещества (теория строения атома и химической связи);
· учение о химическом процессе (химическая кинетика и химическая термодинамика);
· теория растворов и дисперсных систем.
Современную атомно-молекулярную теорию можно изложить в виде ряда положений:
1. Химические вещества имеют дискретное (прерывистое) строение. Частицы вещества находятся в постоянном хаотическом тепловом движении.
2. Основной структурной единицей химического вещества является атом.
3. Атомы в химическом веществе связаны друг с другом, образуя молекулярные частицы или атомные агрегаты (надмолекулярные структуры).
4. Сложные вещества (или химические соединения) состоят из атомов разных элементов. Вещества простые состоят из атомов одного элемента и должны рассматриваться как гомоядерные химические соединения.
При формулировании основных положений атомно-молекулярной теории нам пришлось ввести несколько понятий, на которых необходимо остановиться более подробно, поскольку они являются основными в современной химии. Это понятия "атом" и "молекула", точнее атомные и молекулярные частицы.
Атомные частицы включают в себя собственно атом, атомные ионы, атомные радикалы и атомные ион-радикалы.
Атом - это наименьшая электронейтральная частица химического элемента, являющаяся носителем его химических свойств, и состоящая из положительно заряженного ядра и электронной оболочки.
Атомный ион - это атомная частица, обладающая электростатическим зарядом, но не имеющая неспаренных электронов, например, Cl- - хлорид-анион, Na+ - катион натрия.
Атомный радикал - электронейтральная атомная частица, содержащая неспаренные электроны. Например, атом водорода фактически представляет собой атомный радикал - Н×.
Атомная частица, имеющая электростатический заряд и неспаренные электроны, называется атомным ион-радикалом. Примером такой частицы может служить катион Mn2+, содержащий пять неспаренных электронов на d-подуровне (3d5).
Одной из важнейших физических характеристик атома является его масса. Поскольку абсолютное значение массы атома ничтожно мало (масса атома водорода равна 1,67×10-27 кг), в химии используется относительная шкала масс, в которой за единицу выбрана 1/12 часть массы атома углерода изотопа-12. Относительная атомная масса - это отношение массы атома к 1/12 массы атома углерода изотопа 12С.
Следует отметить, что в периодической системе Д.И. Менделеева приведены среднеизотопические атомные массы элементов, которые в большинстве своем представлены несколькими изотопами, вносящими свой вклад в атомную массу элемента пропорционально своему содержанию в природе. Так, элемент хлор представлен двумя изотопами - 35Cl (75 мол.%) и 37Cl (25 мол.%). Среднеизотопическая масса элемента хлор составляет 35,453 а.е.м. (атомных единиц массы) (35×0,75 + 37×0,25).
Аналогично атомным частицам, молекулярные частицы включают в себя собственно молекулы, молекулярные ионы, молекулярные радикалы и ион-радикалы.
Молекула - это наименьшая устойчивая совокупность взаимосвязанных атомных частиц, являющаяся носителем химических свойств вещества. Молекула лишена электростатического заряда и не имеет неспаренных электронов.
Молекулярный ион - это молекулярная частица, обладающая электростатическим зарядом, но не имеющая неспаренных электронов, например, NO3- - нитрат-анион, NH4+ - катион аммония.
Молекулярный радикал - электронейтральная молекулярная частица, содержащая неспаренные электроны, например, метильный радикал - ×СН3. В обычных условиях радикалы представляют собой реакционно-способные частицы с небольшим временем жизни (порядка 10-3 с).
Молекулярная частица, имеющая электростатический заряд и неспаренные электроны, называется молекулярным ион-радикалом. Примером такой частицы может служить анион-радикал, образующийся при растворении металлического натрия в бензольном растворе нафталина:
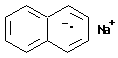
Важной характеристикой молекулы является ее относительная молекулярная масса. Относительная молекулярная масса (Мr) - это отношение среднеизотопической массы молекулы, вычисленной с учетом естественного природного содержания изотопов, к 1/12 массы атома углерода изотопа 12C.
Таким образом, мы выяснили, что мельчайшей структурной единицей любого химического вещества является атом, точнее атомная частица. В свою очередь в любом веществе, исключая инертные газы, атомы связаны друг с другом химическими связями. При этом возможно образование двух типов веществ: молекулярных соединений, у которых можно выделить мельчайшие носители химических свойств, обладающие устойчивой структурой, и соединений надмолекулярной структуры, которые представляют собой атомные агрегаты, в которых атомные частицы связаны ковалентной, ионной или металлической связью. Соответственно, эти вещества представляют собой атомные, ионные или металлические кристаллы. В свою очередь, молекулярные вещества образуют молекулярные или молекулярно-ионные кристаллы. Фактически, работая с конкретным химическим веществом, мы имеем дело не с отдельными атомами или молекулами, а с совокупностью очень большого числа частиц, уровни организации которых можно отобразить следующей схемой:
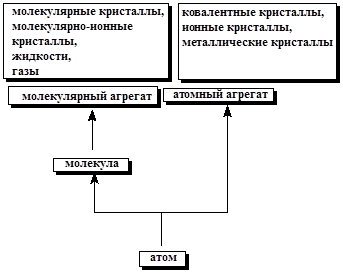
Для количественного описания больших массивов частиц, которыми являются макротела, было введено специальное понятие "количество вещества", как строго определенное число его структурных элементов. Единицей количества вещества является моль. Моль - это количество вещества (n), содержащее столько структурных или формульных единиц, сколько атомов содержится в 12 г углерода изотопа 12С. В настоящее время это число довольно точно измерено и составляет 6,022×1023 (число Авогадро, NA). В качестве структурных единиц могут выступать атомы, молекулы, ионы, химические связи и другие объекты микромира. Понятие "формульная единица" используется для веществ с надмолекулярной структурой и определяется как простейшее соотношение между составляющими его элементами (брутто-формула). В данном случае формульная единица берет на себя роль молекулы. Например, 1 моль хлорида кальция содержит 6,022×1023 формульных единиц - CaCl2.
Одной из важных характеристик вещества является его молярная масса (М, кг/кмоль, г/моль). Молярная масса - это масса одного моля вещества. Относительная молекулярная масса и молярная масса вещества численно совпадают, но имеют разную размерность, например, для воды Мr = 18 (относительная атомная и молекулярная массы величины безразмерные), М = 18 г/моль. Количество вещества и молярная масса связаны простым соотношением:
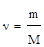
Большую роль в формировании химической атомистики сыграли основные стехиометрические законы, которые были сформулированы на рубеже XVII и XVIII столетий.
1. Закон сохранения массы (М.В. Ломоносов,1748).
Сумма масс продуктов реакции равна сумме масс исходных веществ. В качестве дополнения к этому закону может служить закон сохранения массы элемента (1789, А.Л. Лавуазье) - масса химического элемента в результате реакции не изменяется. Эти законы имеют для современной химии определяющее значение, поскольку позволяют моделировать химические реакции уравнениями и выполнять на их основе количественные вычисления.
2. Закон постоянства состава (Ж. Пруст,1799-1804).
Индивидуальное химическое вещество молекулярного строения имеет постоянный качественный и количественный состав, не зависящий от способа его получения. Соединения, подчиняющиеся закону постоянства состава, называют дальтонидами. Дальтонидами являются все известные к настоящему времени органические соединения (около 30 миллионов) и часть (около 100 тыс.) неорганических веществ. Вещества, имеющие немолекулярное строение (бертолиды), не подчиняются данному закону и могут иметь переменный состав, зависящий от способа получения образца. К ним относятся большинство (около 500 тыс.) неорганических веществ. В основном это бинарные соединения d-элементов (оксиды, сульфиды, нитриды, карбиды и т.д.). Примером соединения переменного состава может служить оксид титана(III), состав которого варьирует в пределах от TiO1,46 до TiO1,56. Причиной переменного состава и иррациональности формул бертолидов являются изменения состава части элементарных ячеек кристалла (дефекты кристаллической структуры), не влекущие за собой резкого изменения свойств вещества. Для дальтонидов подобное явление невозможно, поскольку изменение состава молекулы ведет к образованию нового химического соединения.
3. Закон эквивалентов (И. Рихтер, Дж. Дальтон, 1792-1804).
Массы реагирующих веществ прямо пропорциональны их эквивалентным массам.
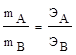 ,
,
где ЭА и ЭВ - эквивалентные массы реагирующих веществ.
Эквивалентной массой вещества называется молярная масса его эквивалента.
Эквивалент - это реальная или условная частица, отдающая или присоединяющая один катион водорода в реакциях кислотно-основного взаимодействия, один электрон в окислительно-восстановительных реакциях или взаимодействующая с одним эквивалентом любого другого вещества в реакциях обмена. Например, при взаимодействии металлического цинка с кислотой один атом цинка вытесняет два атома водорода, отдавая при этом два электрона:
Zn + 2H+ = Zn2+ + H2
Zn0 - 2e- = Zn2+
Следовательно, эквивалентом цинка является 1/2 его атома, т.е. 1/2 Zn (условная частица).
Число, показывающее, какая часть молекулы или формульной единицы вещества является его эквивалентом, называется фактором эквивалентности - fэ. Эквивалентная масса, или молярная масса эквивалента, определяется как произведение фактора эквивалентности на молярную массу:
Э = М·fэ
Например, в реакции нейтрализации серная кислота отдает два катиона водорода:
H2SO4 + 2KOH = K2SO4 + 2H2O
Соответственно, эквивалентом серной кислоты является 1/2 H2SO4, фактор эквивалентности равен 1/2, а эквивалентная масса составляет (1/2)×98 = 49 г/моль. Гидроксид калия связывает один катион водорода, поэтому его эквивалентом является формульная единица, фактор эквивалентности равен единице, а эквивалентная масса равна молярной массе, т.е. 56 г/моль.
Из рассмотренных примеров видно, что при расчете эквивалентной массы необходимо определить фактор эквивалентности. Для этого существует ряд правил:
1. Фактор эквивалентности кислоты равен 1/n, где n - число отданных в реакции катионов водорода.
2. Фактор эквивалентности основания равен 1/n, где n - число отданных в реакции гидроксид-анионов.
3. Фактор эквивалентности соли равен частному от деления единицы на произведение валентности (v) катиона металла или кислотного остатка и их числа (n) в составе соли (стехиометрический индекс в формуле):
fэ = 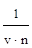
Например, для Al2(SO4)3 - fэ = 1/6
4. Фактор эквивалентности окислителя (восстановителя) равен частному от деления единицы на число присоединенных (отданных) им электронов.
Следует обратить внимание на то обстоятельство, что одно и то же соединение может иметь разный фактор эквивалентности в разных реакциях. Например, в реакциях кислотно-основного взаимодействия:
H3PO4 + KOH = KH2PO4 + H2O; fэ(H3PO4) = 1
H3PO4 + 2KOH = K2HPO4 + 2H2O; fэ(H3PO4) = 1/2
H3PO4 + 3KOH = K3PO4 + 3H2O; fэ(H3PO4) = 1/3
или в окислительно-восстановительных реакциях:
KMn7+O4 + NaNO2 + H2SO4 ® Mn2+SO4 + NaNO3 + K2SO4 + H2O
MnO4- + 8H+ + 5e- ® Mn2+ + 4H2O fэ(KMnO4) = 1/5
KMn7+O4 + NaNO2 + H2O ® Mn4+O2 + NaNO3 + KOH
MnO4- + 2H2O + 3e- ® MnO2 + 4OH- fэ(KMnO4) = 1/3
4. Закон Авогадро(А. Авогадро,1811).
В равных объемах разных газов, измеренных в одинаковых условиях (давление, температура), содержится одинаковое число молекул.
Из закона следует, что:
Ø При нормальных условиях (н.у., Т = 273 К, р = 101,325 кПа) один моль любого газа занимает одинаковый объем - молярный объем (Vm), равный 22,4 л/моль.
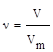
Ø Отношение масс равных объемов разных газов, измеренных в одинаковых условиях (относительная плотность газа по газу), равна отношению их молекулярных (молярных) масс.

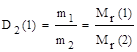
Чаще всего определяют относительную плотность по водороду или воздуху. Соответственно,
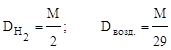 ,
,
где 29 - средняя, точнее средневзвешенная, молекулярная масса воздуха.
Ø Объемы реагирующих газов относятся друг к другу и к объемам газообразных продуктов реакции как простые целые числа (закон объемных отношений Гей-Люссака).
Литература: [1] c. 11 - 45; [2] с. 4 - 42
Лекция № 18. Водород
Водород расположен в первом периоде периодической системы химических элементов (элемент № 1), представлен в природе тремя изотопами: протий 1H, дейтерий 2H (D), тритий 3H (T). Протий и дейтерий стабильные изотопы (содержание дейтерия в природном водороде составляет 0,015%), тритий радиоактивен (период полураспада 12,26 года), образуется в верхних слоях атмосферы под действием космических лучей и содержится в природном водороде в исчезающе малом количестве.
Атом водорода содержит на внешнем и единственном энергетическом уровне один электрон (1s1) и является электронным аналогом щелочных металлов. В то же время, до завершения валентного уровня атому водорода недостает одного электрона, что роднит его с галогенами. По этой причине водород часто помещают как в первую, так и в седьмую группу периодической системы.
Водород, наряду с гелием, самый распространенный элемент Вселенной, он составляет до половины массы звезд и основную массу межзвездной материи. Содержание водорода в земной коре (кларк) составляет 3 мол.%. Водород - элемент-органоген и входит в состав органических соединений.
Простое вещество водород - H2 - бесцветный газ, не имеющий вкуса и запаха, не обладающий физиологическим действием, т.пл. -259,2 °С (14 К), т.кип. -252,8 °С (20 К). Водород - самый легкий из газов (в 14,5 раз легче воздуха), с высокой скоростью диффузии, легко проникает через разнообразные перегородки. Плохо растворим в воде, но хорошо растворим в некоторых металлах (Ni, Pt, Pd).
Получение водорода. В промышленности водород получают конверсией метана или угля водяным паром, а также неполным окислением метана:
t
CH4 + H2O = CO + 3H2
t
C + H2O = CO + H2
t
2CH4 + O2 = 2CO + 4H2
Лабораторные методы получения водорода:
1. Действие кислот на металлы (обычно действуют на цинк соляной кислотой в аппарате Киппа).
Zn + 2HCl = ZnCl2 + H2
2. Действие щелочей на алюминий.
2Al + 6KOH + 6H2O = 2K3[Al(OH)6] + 3H2
3. Электролиз водных растворов щелочей на никелевых электродах.
эл.ток
2H2O = 2H2 + O2
4. Взаимодействие гидрида кальция с водой.
CaH2 + 2H2O = Ca(OH)2 + 2H2
Химические свойства. Особенности строения электронной оболочки атома водорода обуславливают его способность к присоединению одного электрона. Поэтому водород может выступать как окислитель, образуя соединения в степени окисления -1. В то же время невысокая электроотрицательность водорода (2,2 по Л. Полингу) способствует потере одного электрона и образованию соединений в степени окисления +1.
+e- -e-
H- ¾ H ¾® H+
Довольно высокая энергия диссоциации молекулы Н2(435 кДж/моль) обуславливает инертность водорода в обычных условиях. При комнатной температуре водород реагирует только со фтором:
H2 + F2 = 2HF
При нагревании водород реагирует со многими неметаллами (Cl2, Br2, O2, N2, S, C), проявляя при этом свойства восстановителя. Взаимодействие с хлором и кислородом инициируется ультрафиолетовым облучением и протекает по радикальному механизму. При этом реакция с хлором протекает по неразветвленному цепному механизму и включает ряд стадий:
1. Инициация цепи (фотохимическая диссоциация):
Cl2 + hn ® 2Cl×
2. Рост (развитие) цепи:
Cl× + H2 ® HCl + H×
H× + Cl2 ® HCl + Cl×
3. Обрыв цепи:
H× + Cl× ® HCl
Реакция водорода с кислородом идет по механизму цепной разветвленной реакции, включая следующие стадии:
1. Инициация цепи: H2 + O2 ® ×OH + HO×
2. Рост цепи: HO× + H2 ® H2O + H×
3. Разветвление цепи: H× + O2 ® ×OH + ×O×
×O× + H2 ® ×OH + ×H
4. Обрыв цепи: HO× + ×H ® H2O
При нагревании водород реагирует со щелочными и щелочноземельными металлами, образуя соответствующие гидриды - бинарные соединения водорода в степени окисления -1.
t
2Na + H2 = 2NaH-1
гидрид натрия
При повышенных температурах водород восстанавливает металлы из их оксидов и галогенидов:
t t
CuO + H2 = Cu + H2O; CuCl2 + H2 = Cu + 2HCl
Восстановительные свойства водород способен проявлять также и по отношению к оксидам неметаллов и органическим соединениям, например,
t
N2O + H2 = N2 + H2O
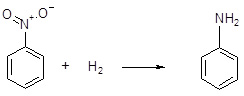
нитробензол анилин
Большое значение для синтеза органических соединений имеет реакция каталитического присоединения водорода по кратным связям углерод - углерод (гидрогенизация или гидрирование):
t
C2H4 + H2 ® C2H6
Pd
Соединения водорода
Если учесть органические вещества, то следует признать, что водород - элемент, образующий наибольшее число соединений. Важнейшими неорганическими соединениями водорода являются гидриды и бинарные соединения водорода в степени окисления +1. Последние также часто называют гидридами, что не совсем корректно, ибо гидриды - это бинарные соединения водорода в степени окисления -1. "Классические гидриды" могут образовывать только те элементы, электроотрицательность у которых значительно меньше, чем у водорода. Это щелочные и щелочноземельные металлы, а также магний и бериллий. Они образуют типичные солеподобные гидриды, при электролизе расплавов которых водород выделяется на аноде:
2H- - 2e- ® H20
При взаимодействии гидридов данного типа с водой также выделяется водород:
NaH-1 + H2+1O = NaOH + H20
Элементы, электроотрицательность которых незначительно отличается от водорода, образуют ковалентные гидриды (B2H6, SiH4). Известно небольшое число комплексных гидридов, например, Li[AlH4], Na[BH4], которые широко применяются в органическом синтезе в качестве восстановителей.
Из бинарных соединений водорода в степени окисления +1 в данном разделе будет рассмотрен оксид водорода (вода) и его пероксид (перекись водорода).
Химически чистая вода представляет собой бесцветную жидкость без вкуса и запаха. Молекула воды - Н2О - имеет угловое строение. Образование молекулы воды происходит с участием sp3-гибридных орбиталей атома кислорода, две из которых заняты неподеленными электронными парами и поэтому вклада в геометрию молекулы не вносят. Перекрывание одноэлектронных облаков двух гибридных орбиталей кислорода и 1s-орбиталей двух атомов водорода приводит к образованию уголковой молекулы. Отталкивающие действие двух неподеленных пар электронов уменьшает валентный угол HOH до 104,5° (см. стр. 19).
В кристаллическом состоянии молекула воды, окруженная четырьмя соседями, образует с ними очень прочные водородные связи, вследствие чего вода обладает аномально высокой температурой кристаллизации (0 °) и кипения (100 °С). Согласно клатратной теории в жидкой воде существуют микроскопические фрагменты кристаллической структуры льда - клатраты, находящиеся в равновесии с жидкой фазой.
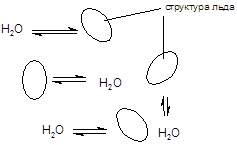
За счет образования прочных водородных связей, а также координационных соединений, вода является хорошим растворителем для многих типов органических и неорганических соединений, частицы которых существуют в растворах в виде аддуктов с молекулами воды - гидратов. При выделении из водных растворов многие вещества кристаллизуются в виде гидратов, образуя кристаллогидраты. Можно выделить три типа кристаллогидратов, отличающихся характером связывания воды:
1. Клатраты - имеющие кристаллическую структуру льда, полости которой заняты частицами вещества. Такое строение имеют кристаллогидраты солей щелочных металлов, содержащие большое количество воды, например, Na2SO4×10H2O, а также кристаллогидраты, образуемые галогенами и инертными газами - Cl2×8H2O, или Ar 6H2O.
2. Аквакомплексы, содержащие воду, координированную катионом металла, чаще всего переходного, например, CoCl2×6H2O, точнее [Co(OH2)6]Cl2.
3. Кристаллогидраты, содержащие воду, связанную с частицами вещества водородными связями. Часто этот тип связывания воды реализуется в кристаллогидратах органических веществ.
С химической точки зрения вода довольно реакционноспособное соединение, вступающее во взаимодействие с различными простыми и сложными веществами, в том числе с органическими соединениями.
Кроме оксида водорода хорошо изучен его аналог - оксид дейтерия - D2O, более известный под названием "тяжелая вода". Тяжелая вода широко применяется в атомной энергетике как замедлитель нейтронов. Реакции с участием тяжелой воды идут медленней, а температура ее кипения (101,4 °С) несколько выше по сравнению с H2O, поэтому при проведении электролиза или дистилляции большого количества воды тяжелая вода накапливается в остатке.
Пероксид водорода (перекись) - Н2О2 - бесцветная сиропообразная жидкость (d = 1,45 г/см3), неустойчивая в чистом виде, но устойчивая в водных растворах до 30% концентрации. Распад пероксида водорода катализируется соединениями тяжелых металлов, например, MnO2.
2Н2О2 = 2Н2О + О2
Получают пероксид водорода электролизом водных растворов серной кислоты или гидросульфата аммония. При этом на аноде образуется пероксосерная кислота, гидролиз которой приводит к образованию пероксида водорода:
2HSO4- - 2e- ® H2S2O8
H2S2O8 + 2H2O = 2H2SO4 + H2O2
Вследствие промежуточной степени окисления кислорода (-1), пероксид водорода, в зависимости от условий проведения реакции, может быть как окислителем, так и восстановителем. В кислой среде H2O2 довольно сильный окислитель:
H2O2 + 2H+ + 2e- ® 2H2O; E0 = 1,78 В
В то же время пероксид водорода окисляется более сильными окислителями, например, перманганатом калия:
2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + 5O2 + K2SO4 + 8H2O
Водные растворы пероксида водорода (в основном 3%) применяются для отбелки тканей и меха, дезинфекции, консервации, протравливания семян. Важную роль пероксид водорода играет в процессах самоочищения природных водоемов, в которых он содержится в ничтожной концентрации (порядка 3×10-5 моль/л), но тем не менее, эффективно окисляет биологические загрязнения.
Литература: [1] с. 330 - 338, [2] с. 411 - 415, [3] с. 262 - 270
Cоединения галогенов
Наиболее важными соединениями галогенов в степени окисления -1 являются галогеноводороды, галогеноводородные кислоты и их соли.
Галогеноводороды, кроме HF, представляют собой токсичные газы с резким удушающим запахом. Молекулы фтороводорода сильно ассоциированы за счет прочных водородных связей, по этой причине HF имеет аномально высокую температуру кипения (19,6 °С). Фтороводород получают действием концентрированной серной кислоты на фториды. Эта же реакция используется для лабораторного получения хлороводорода. В промышленности хлороводород получают прямым синтезом, бромоводород и иодоводород - гидролизом тригалогенидов фосфора, которые получают непосредственно в реакторе:
t
2P + 3Br2 + 6H2O = 2H3PO3 + 6HBr
Жидкий фтороводород является прекрасным ионизирующим растворителем, в котором многие вещества ведут себя как основания, поскольку взаимодействуя с HF, увеличивают концентрацию отрицательных ионов растворителя:
2HF  H+ + HF2-
H+ + HF2-
HNO3 + 2HF  NO3H2+ + HF2-
NO3H2+ + HF2-
основание
Кислотами в жидком фтористом водороде являются акцепторы фторид-аниона, например, фториды некоторых металлов:
SbF5 + HF  H+ + [SbF6]-
H+ + [SbF6]-
Галогеноводороды хорошо растворимы в воде, образуя растворы соответствующих кислот: HF - фтороводородная или плавиковая кислота, HCl - хлороводородная или соляная кислота, HBr - бромоводородная и HI - иодоводородная кислоты. Плавиковая кислота - кислота средней силы (К = 7×10-4), остальные галогеноводородные кислоты - сильные, при переходе от HCl к HI сила кислоты увеличивается.
Концентрированная соляная кислота обычно представляет собой 37% раствор хлороводорода.
Бромистоводородная и иодистоводородная кислоты напоминают соляную, но менее устойчивы к окислению. Иодистый водород окисляется уже кислородом воздуха:
4HI + O2 = 2I2 + 2H2O
Фтороводород, а также плавиковая кислота энергично разрушают стекло, поэтому кислоту хранят в пластиковой или парафинированной посуде:
SiO2 + 6HF = H2[SiF6] + 2H2O
Плавиковая кислота и фториды металлов токсичны, кислота при попадании на кожу вызывает сильные и долго не заживающие ожоги. Большинство солей плавиковой кислоты в воде плохо растворимы. Хорошо растворимы фториды натрия, калия, алюминия, олова и серебра. В отличие от других галогеноводородных кислот, плавиковая кислота образует кислые соли - производные димера H2F2, например, KHF2 или KF×HF.
Большинство хлоридов (солей соляной кислоты) хорошо растворимы в воде. Малорастворимы AgCl, PbCl2, CuCl, Hg2Cl2. Образование белого творожистого осадка хлорида серебра используется как качественная реакция на хлорид-анион:
Ag+ + Cl- = AgCl¯
Хлорид натрия применяется для консервации и как пищевкусовая добавка. Хлорид калия используется в качестве удобрения. Бромиды натрия и калия используют в медицине в качестве транквилизаторов. Иодид калия применяют при лечении заболеваний щитовидной железы. Бромид серебра используется в фотоделе в качестве светочувствительного материала.
Из кислородсодержащих соединений галогенов наибольший интерес представляют фториды кислорода, оксиды и кислородсодержащие кислоты хлора.
Газообразный OF2 получают, пропуская фтор через разбавленный раствор гидроксида натрия при охлаждении:
2NaOH + 2F2 = 2NaF + H2O + OF2
При пропускании через смесь фтора и кислорода электрического разряда образуется O2F2 - желто-оранжевое кристаллическое вещество. Фториды кислорода - сильные окислители и фторирующие реагенты.
Из оксидов хлора наиболее устойчивы оксид хлора(I) - Cl2O, оксид хлора(IV) - ClO2 и оксид хлора(VII) - Cl2O7. Все эти вещества нестабильны, сильнейшие окислители, типичные кислотные оксиды.
Cl2O + H2O = 2HClO
2ClO2 + H2O = HClO2 + HClO3
Cl2O7 + H2O = 2HClO4
Хлор образует четыре кислородсодержащие кислоты.
| C.О. хлора | Формула кислоты | Название кислоты | Соли |
| +1 | HClO | хлорноватистая | гипохлориты |
| +3 | HClO2 | хлористая | хлориты |
| +5 | HClO3 | хлорноватая | хлораты |
| +7 | HClO4 | хлорная | перхлораты |
С увеличением степени окисления сила кислоты и ее устойчивость увеличивается. Хлорноватистая и хлористая кислота - слабые кислоты, хлорная - одна из самых сильных минеральных кислот. В свободном виде выделена только хлорная кислота (очень неустойчива и взрывоопасна), остальные кислоты существуют только в разбавленных растворах. Хлорноватистая кислота и гипохлориты - очень сильные окислители. При переходе к хлорной кислоте и перхлоратам окислительная способность соединений уменьшается.
Из солей кислородсодержащих кислот хлора наибольшее применение находит хлорная известь - смешанный гипохлорит- хлорид кальция, Ca(ClO)Cl.
Литература: [1] с. 338 - 359, [2] с. 415 - 423, [3] с. 270 - 296
Соединения серы
Наиболее важными соединениями серыв степени окисления -2 являются сероводород и сульфиды.
Сероводород - H2S - бесцветный газ с характерным запахом гниющего белка, токсичен. Образуется при непосредственном взаимодействии водорода с парами серы. В лаборатории сероводород получают действием сильных кислот на сульфиды металлов:
Na2S + 2HCl = 2NaCl + H2S
Сероводород сильный восстановитель, окисляется даже оксидом серы(IV).
2H2S-2 + S+4O2 = 3S0 + 2H2O
На воздухе и в атмосфере кислорода сероводород горит, образуя серу или SO2 в зависимости от условий.
В воде сероводород малорастворим (2,5 объема H2S на 1 объем воды) и ведет себя как слабая двухосновная кислота.
H2S  H+ + HS-; К1 = 1×10-7
H+ + HS-; К1 = 1×10-7
HS-  H+ + S2-; К2 = 2,5×10-13
H+ + S2-; К2 = 2,5×10-13
Как двухосновная кислота сероводород образует два ряда солей: гидросульфиды (кислые соли) и сульфиды (средние соли). Например, NaНS - гидросульфид и Na2S - сульфид натрия.
Сульфиды большинства металлов в воде малорастворимы, окрашены в характерные цвета и
