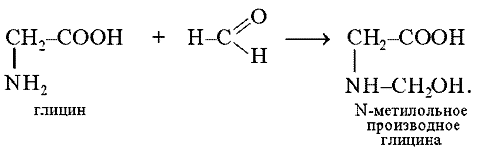
Аминокислоты. Номенклатура. Классификация.
Аминокислоты – гетерофункциональные соединения содержащие карбоксильную и аминогруппы. По взаимному расположению групп различают α- β- и γ-кислоты.
Классификация аминокислот:
1)По функциональным группам:
-Алифатические
-Нейтральные
*Основные
*Кислые
-Ароматические
-Гетероциклические
2)По R-группам:
-Неполярные
-Неполярные незаряженные
-Полярные положительно заряженные
Кислотно-основные свойства аминокислот. Биполярная структура. Строение в кислой и щелочной средах.
Аминокислоты – амфотерные соединения, что обусловлено одновременным присутствием основной(NH2) и кислотной (COOH)групп. Аминокислоты существуют в виде внутренней соли – биполярного иона, так же называемого цвиттер-ионом.
В кислой среде в аминокислотах полностью протонированна аминогруппа и не диссоциированна карбоксильная группа. В сильнощелочной среде напротив, аминогруппа свободна, а карбоксильная полностью ионизирована
Строение пептидов. Первичная структура пептидов и белков.
Пептиды и белки – соединения построенные из остатков аминокислот(от 100 и выше)
В группе пептидов принято различать:
-олигопептиды(не более 10 остатков аминокислот)
-полипептиды (до 100 аминокислотных остатков)
Пептидную или белковую молекулу формально можно представить как продукт полной диссоциации α-аминокислот, протекающей с образованием пептидной связи между мономерными звеньями.
Первичная структура пептидов и белков – аминокислотная последовательность т.е. порядок чередования α-аминокислоты.
Качественные реакции на пептидную группу и отдельные аминокислоты.
БИУРЕТОВАЯ РЕАКЦИЯ
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
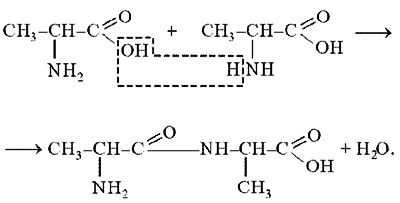
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
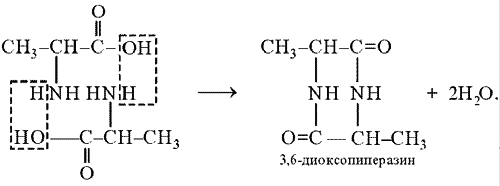
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Описание опыта. 2–3 мл раствора белка нагревают с 2–3 мл 20%-го раствора едкого кали или натра и несколькими каплями раствора медного купороса. Появляется фиолетовое окрашивание вследствие образования комплексных соединений меди с белками.
- РЕАКЦИЯ С ФОРМАЛЬДЕГИДОМ
При взаимодействии a-аминокислот с формальдегидом образуются относительно устойчивые карбиноламины – N-метилольные производные, содержащие свободную карбоксильную группу, которую затем титруют щелочью: 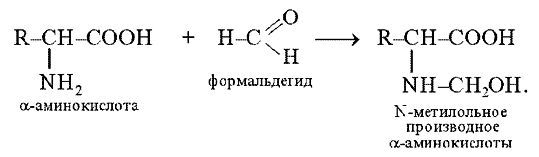
Эта реакция лежит в основе количественного определения a-аминокислот методом формального титрования (метод Сёренсена).
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):