Компьютеризированная лабораторная работа № 3 (УИРС)
Определение теплоты растворения хорошо
Растворимых солей
Цель работы:определить теплоту растворения неизвестной соли. Для этого необходимо:
- определить изменение температуры при растворении известной соли;
- определить интегральную теплоту растворения данной соли (по справочнику);
- рассчитать постоянную калориметра;
- определить ∆T при растворении неизвестной соли;
- рассчитать интегральную теплоту растворения неизвестной соли.
Теоретическая часть
Теплота растворения твердого соединения с ионной кристаллической решеткой определяется в основном суммой двух величин: теплоты разрушения кристаллической решетки и теплоты сольватации ионов молекулами растворителя. В связи с тем, что на разрушение кристаллической решетки теплота затрачивается, а процесс сольватации сопровождается выделением теплоты, знак теплоты растворения может оказаться как положительным, так и отрицательным, в зависимости от того, какое из двух слагаемых больше по абсолютной величине.
Теплота растворения зависит от концентрации образующегося раствора. Например, при растворении одного моль CuCO3 · 2 H2O в 8 моль воды поглощается 3,35 кДж теплоты, при растворении того же количества кристаллогидрата в 12 молях воды теплота растворения равна нулю, а при растворении в очень большом количестве воды выделяется 17,67 кДж теплоты.
Различают интегральную и дифференциальную теплоты растворения. Теплота, которая поглощается или выделяется при растворении одного моль вещества в таком количестве растворителя, чтобы образовался раствор с определенной моляльностью m, называется интегральной теплотой растворения. Дифференциальной теплотой растворения называется тепловой эффект, сопровождающий процесс растворения одного моль вещества в бесконечно большом количестве растворителя.
Дифференциальные теплоты растворения определяются расчетным методом. Интегральные теплоты растворения находятся экспериментально.
Рекомендации по проведению расчетов
Расчет теплоты растворения проводят на основе уравнения теплового баланса
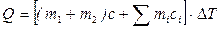 , (1)
, (1)
где m1 и m2 – масса воды и соли, соответственно, г;
с – теплоемкость образующегося раствора, Дж г-1×К-1, (для водных растворов с небольшой концентрацией растворенного вещества можно принять, что с = 4,18 Дж г-1× К-1); mi и сi – масса и теплоемкость составных частей калориметра.
Точно определить mi и сi не представляется возможным. Поэтому ∑miсi обозначают символом К, называемым постоянной калориметра и определяют его значение по изменению температуры при растворении определенного количества соли с известной теплотой растворения. Постоянная калориметра – количество тепла, которое необходимо подвести к участвующей в теплообмене части калориметра, чтобы поднять его температуру на 1°С. В этом случае уравнение теплового баланса запишется в виде:
Q = [(m1+m2)c + K]×∆Т. (2)
Отсюда
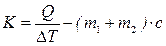 . (3)
. (3)
В качестве соли с известной теплотой растворения можно использовать КСl или NH4Cl. Интегральные теплоты растворения солей даны в справочнике.
В справочнике интегральные теплоты растворения даны для стандартной температуры 298 К. Если температура воды, в которой растворяют соль, отличается от стандартной, то теплота растворения будет иной. Поэтому опыт нужно проводить при стандартной температуре или рассчитывать интегральную теплоту растворения для данной температуры с помощью уравнений типа ∆H =∆H298k (298 – T), где k –коэффициент, характерный для каждой соли. Например, для КСl – ∆Hуд = 256,9 – 3,89(298 - T), Дж × г-1.
Теплота растворения соли зависит от концентрации образующегося раствора. Поэтому необходимо рассчитать концентрацию раствора, образующегося при растворении соли с известной теплотой растворения и, в соответствии с этим, интерполяцией определить теплоту растворения этой соли для данной концентрации, а затем рассчитать постоянную калориметра.
Зная постоянную калориметра легко рассчитать теплоту растворения неизвестной соли. Для этого определяют изменение температуры при растворении неизвестной соли и рассчитывают Q по формуле, а также рассчитывают удельную теплоту растворения неизвестной соли q по формуле
q = Q / m2. (4)
Значение удельной теплоты растворения соли можно использовать (наряду с другими данными) для определения соли. Для этого сравнивают полученное значение со справочными значениями удельных теплот растворения различных солей.
Экспериментальная часть
Приборы и реактивы
1. Учебно-лабораторный комплекс «Химия» в следующей комплектации:
- центральный контроллер;
- модуль «Термостат» в комплекте со стеклянным стаканчиком (150 см3), термодатчиком и устройством для размещения навески соли в термостате.
2. Навеска соли с известной теплотой растворения (2 г) и навеска неизвестной соли (2 г).
