Второй закон термодинамики. Энтропия как мера упорядоченности.
Любая термодинамическая система обладает не только определенным запасом внутренней энергии, но и характеризуется определенной степенью упорядоченности.
Второй термодинамической функцией состояния является энтропия – функция, ответственная за неупорядоченность состояния данной химической системы: чем большей хаотичностью и беспорядком (т.е. большей неупорядоченностью) характеризуется данная система, тем больше величина энтропии. Энтропия обозначается латинской буквой S и измеряется в Дж/K. Это значит, что любая изолированная система, представленная самой себе, самопроизвольно изменяется в направлении максимальной хаотичности своего состояния.
Рассмотрим пример: Поместим в сосуд с перегородкой два газа азот и аргон. Обозначим это состояние системы S1. В данном состоянии оба газа имеют определенную степень упорядоченности (степень беспорядка). После того, как уберем перегородку, газы начнут смешиваться. Это второе состояние системы обозначим S2. Степень беспорядка увеличилась. Произошло самопроизвольное увеличение энтропии ΔS = S2 – S1
8.Энергия Гиббса. Стандартные значения свободной энергии.Изменение свободной энергии в химической реакции.
8) Свободная энергия Гиббса — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на принципиальную возможность химической реакции; это термодинамический потенциал следующего вида:
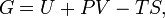 где U — внутренняя энергия, P — давление, V — объем, T — абсолютная температура, S —энтропия.
где U — внутренняя энергия, P — давление, V — объем, T — абсолютная температура, S —энтропия.
Энергия Гиббса и направление протекания реакции
В химических процессах одновременно действуют два противоположных фактора — энтропийный (TΔS) и энтальпийный (ΔH). Суммарный эффект этих противоположных факторов в процессах, протекающих при постоянном давлении и температуре, определяет изменение энергии Гиббса (G):
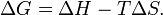
Из этого выражения следует, что 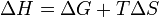 , то есть некоторое количество теплоты расходуется на увеличение энтропии (TΔS), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (ΔG) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.
, то есть некоторое количество теплоты расходуется на увеличение энтропии (TΔS), эта часть энергии потеряна для совершения полезной работы, её часто называют связанной энергией. Другая часть теплоты (ΔG) может быть использована для совершения работы, поэтому энергию Гиббса часто называют также свободной энергией.
При ΔG < 0 процесс может протекать, при ΔG > 0 не может, Если же ΔG = 0- состояние равновесия.
Существует полезное соотношение, связывающее изменение свободной энергии Гиббса 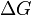 в ходе химической реакции с еёконстантой равновесия
в ходе химической реакции с еёконстантой равновесия 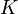 :
:
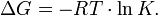
Вообще говоря, любая реакция может быть рассмотрена как обратимая (даже если на практике она таковой не является). При этом константа равновесия определяется как
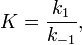
где 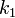 — константа скорости прямой реакции,
— константа скорости прямой реакции, 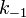 — константа скорости обратной реакции.
— константа скорости обратной реакции.
