Высокомолекулярные соединения (вмс)
Синтез соединений с большим молекулярным весом, то есть высокомолекулярных соединений является в настоящее время одним из основных направлений в современной химическое науке и промышленности. Общеизвестно огромное значение этих соединений в нашей жизни, позволяющих получать такие продукты, как каучук и резину, пластмассы, искусственные волокна, смолы, лаки и краски, специальные масла. В разработке методов исследования и получения ВМС, выдающаяся роль принадлежит русским химикам. Еще в 1859 г. А.М Бутлеров получил полимер формальдегида, а в 1873 г. исследовал реакцию полимеризации изобутилена. Этими работами Бутлеров по выражению академика Арбузова, “открыл дверь в область высокомолекулярных соединений”. ВМС получают двумя основными методами:
1) полимеризации и сополимеризации;
2) поликонденсации.
Метод полимеризации
Полимеризацией называют реакции соединения между собой большого числа молекул одного и того же вещества или разных веществ в одну большую молекулу. Реакцию соединения молекул различных веществ называют сополимеризацией. В самом общем виде уравнение реакции полимеризации можно представить следующим образом:
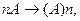
где А обозначает молекулу мономера, а n- количество соединившихся молекул, т.е степень полимеризации.
Коротко можно сказать, что полимеризация- образование полимера из мономера. Мономер - термин, имеющий смысл только по отношению к его полимеру. Если нет полимера - нет и мономера. Принципиально полимеризация представляет собой реакцию присоединения за счет разрыва двойных связей в молекуле мономера. Однако эта реакция часто осложняется процессами изомеризации с перемещением двойных связей и групп атомов или вовлечением в реакцию различных других веществ (катализаторов, регуляторов роста, эмульгаторов и т.д.)
Различают два основных типа процесса нарастания полимерной цепи:
1) Ступенчатая полимеризация - когда соединение молекул сопровождается перемещением атомов водорода или целых групп атомов. Продукты реакции на каждой стадии могут быть выделены.
2) Цепная или линейная полимеризация, когда перемещения атомов не происходит. Продукты начальных стадий не могут быть выделены изолированно; продукт реакции - ВМС.
Примером реакции первого типа является изученная А.М Бутлеровым полимеризация изобутилена. Реакция катализируется кислотами (H2SО4), в ходе ее можно выделить диизобутилены, гидрирование которых дает изооктан, или провести реакцию дальше с получением полиизобутилена. Механизм реакции таков:
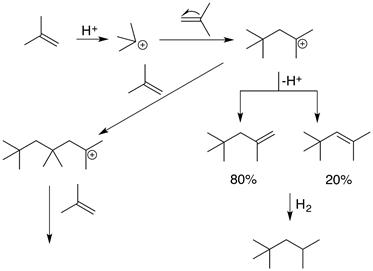
Цепная полимеризация может протекать по двум механизмам: ионному (каталитическому) и радикальному (инициированному).
Радикальная полимеризация вызывается (инициируется):
- веществами, способными в условиях реакции распадаться на свободные радикалы;
- тепловой энергией;
- облучением (УФ, радиация).
При термической полимеризации некоторая часть молекул мономера под влиянием повышенной температуры активируется и реагирует друг с другом. На примере стирола это можно представить себе следующим образом
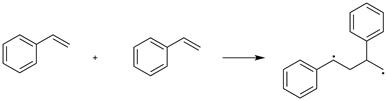
Образовавшаяся таким образом молекула димера стирола - бирадикальная частица и благодаря этому легко присоединяет другие молекулы стирола, образуя полимерные радикалы:
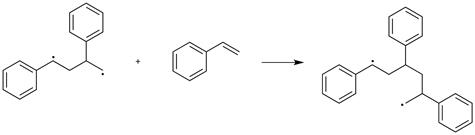
В этом случае полимеризации процесс представляет собой типичную ценную реакцию: возникший вначале активный центр (т.е. стадия инициирования) вызывает длинную цепь реакций присоединения (стадия роста цепи). Для достижения достаточных скоростей реакции при термическом инициировании обычно требуются высокие температуры, при которых происходит нежелательные побочные процессы. Гораздо более удобен способ инициирования реакции полимеризации введением в реакционную зону веществ, способных генерировать свободные радикалы. Такими соединениями являются перекиси, гидроперекиси, некоторые другие соединения. Часто используют перекись бензоила:
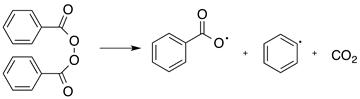
В общем виде: (RCOO)2 → RCOO + R + CO2.
Эти свободные радикалы и являются теми активными центрами, которые начинают процесс образования полимерной цепи. Например, полимеризация стирола в этом случае может быть так представлена:
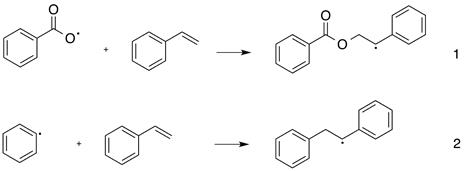
К образовавшимся радикалам 1 и 2 присоединяются следующие молекулы стирола и т.д. (рост цепи). В общем виде эти процессы могут быть так представлены:
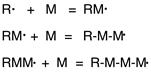
До образования макромолекулы. На некоторой стадии рост цепи прекращается (обрыв цепи) и выросший макрорадикал превращается в устойчивую макромолекулу полимера.
Причиной обрыва цепи являются:
- рекомбинация, т.е. соединение, двух макрорадикалов
R-(M)n-M + M-(M)n-R → R-(M)n-M-M-(M)n-R;
- рекомбинация макрорадикала с каким-то другим малоактивным радикалом;
- взаимодействие макрорадикала с какими-то другими веществами;
- изомеризация макрорадикала в устойчивое соединение;
- пространственные затруднения.
В производстве огромную роль играет скорость процесса полимеризации. Она определяется как природой инициатора (катализатора), так и структурой мономера и методикой проведения процесса.
Процесс полимеризации может проводиться:
- в массе, когда непосредственно в жидкую массу мономера добавляется катализатор и при определенной температуре происходит накопление полимера, сопровождающиеся загустеванием и затем затвердевание массы;
- в растворах;
- в эмульсиях;
- в газовой фазе.
Первый способ широко применяется в производстве синтетических смол. Он удобен для практического осуществления, но в этом случае трудно проводить отвод тепла, выделяющегося в ходе реакции, затрудняется перемешивание из-за высокой вязкости, что приводит к неоднородности полимера. При полимеризации в растворах несколько снижается скорость, и возникают трудности при удалении растворителя.
Полимеризация в эмульсии получила большое распространение, особенно при производстве синтетического каучука. Способ этот заключается в том, что мономер распределяется среди какой-либо жидкости (чаще всего воды), в которой он не растворяется, в виде мельчайших капелек, образуя типичную эмульсию (жидкость в жидкости). Добавляется инициатор, растворимый в той или другой фазе, затем вещества, придающие эмульсии устойчивость – эмульгаторы и другие ненужные вещества – активаторы, регуляторы роста цепи, и смесь перемешивается в закрытых реакторах – полимеризаторах при определенной температуре. В отличие от первых двух процессов, этот процесс проходит в гетерогенной высокодисперсной системе. Установлено, что в этих условиях легче происходит распад инициатора, менее развиты процессы обрыва цепи, на поверхности раздела фаз больше сказываются явления полярности молекул и другие явления. Все это приводит к тому, что скорость полимеризации в эмульсиях в десятки раз больше, чем в гомогенной среде.
Условия полимеризации имеют решающее значение в деле получения полимеров с желаемыми свойствами, так как от этих условий зависят порядок роста цепи и структура молекул полимера, а значит, и его физические и технические свойства. Впервые реакция полимеризации в эмульсии была проведена русским химиком и инженером Остромысленским в 1915 году. С тех пор вопросы эмульсионной полимеризации в нашей стране усиленно разрабатывались таким учеными, как Б.А. Догадкин, Б.А.Долгоплоск, П.М. Хомиковский, С.С Медведев, и др.
Основные углеводородные полимеры получают полимеризацией этиленовых производных. Рассмотрим некоторые их них.
1) Полиэтилен (ПЭ): этилен полимеризуется с трудом, реакция проводится при высоких температурах (до 200оС) и давлениях (до 1000 атм). Образуются ВМС с Мr 20000 и выше.
Впервые полиэтилен был получен Густавсоном в 1884 г каталитической (AlBr3) полимеризацией этилена. Молекула ПЭ представляет собой длинную, зигзагообразную цепь из метиловых групп.
ПЭ при обычных температурах не растворяется в органических растворителях, но при t>80°С – хорошо растворяется в R-Hal и ароматических углеводородах. Кислоты и щелочи не действуют на ПЭ. ПЭ весьма прочен, хорошо обрабатывается и сваривается. Область применения – изолирующие и защитные покрытия, бытовые изделия.
При полимеризации ПЭ в присутствие AlCl3 в качестве катализатора при t=120-200°С и Р=100атм получают смеси углеводородов с разветвленными цепями, которые используют после их разбавления эфирами кислот в качестве специальных смазочных масел.
2) Полистирол: полимеризация стирола идет легче, чем этилена - осуществляется в радикальных условиях (перекиси). Строение полистирола:
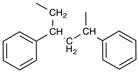
Получают полимеры с Мr от 3 до 600 тысяч. Высшие полимеры – твердые прозрачные стеклообразные продукты. Выше 150оС он начинает деполимеризоваться с образованием стирола. Сополимеризацией стирола с бутадиеном получают бутадиен-стирольный каучук. Область применения – электроизолятор, в технике, в быту.
3) Полиизобутилен, бутилкаучук: полимеризация идет в присутствие кислот (бутлеров) при низких температурах (80оС, Лебедев С.В). Низкомолекулярные полимеры изобутилена – жидкие или маслообразные вязкие вещества – добавки к смазочным маслам. При Mr>50000 – каучукоподобные или твердые полимеры. Строение цепи
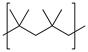
Полиизобутилен – насыщенное соединение не способное вулканизироваться.
Процесс протекает при температуре 80-100оС в присутствие AlCl3 или BF3 с очень высокой скоростью (секунды). Чем ниже температура, тем выше Mr. Так при 80oС Mr = 70000, а при 103oС Mr= 200000.
Полимеризацию проводят, разбавляя изобутилен до 25% пропаном, бутаном.
Полиизобутилен применяется для электроизоляции, защитных покрытий, химических стойких связующих материалов, пропитки тканей и т.д.
Сополимер изопрена называется бутилкаучук
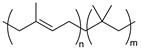
Смысл добавки изопрена – введение двойной связи в молекулу сополимера, тогда можно вулканизировать Mr до 100000. Бутилкаучук идет на производство резины для камер, т.к. обладает повышенной газонепронициаемостью, диэлектрик, защитных покрытий, пропиточных материалов, клеев.
Метод поликонденсации
Поликонденсацией называют процесс образования больших молекул (полимерных) путем сочетания молекул одного и того же или различных веществ, сопровождающихся выделением каких-нибудь низкомолекулярных продуктов (молекул воды, аммиака, галоид водорода и т.д.). В основе этого процесса лежит известные в органической химии реакция конденсации двух молекул, содержащих те или иные функциональные группы. Примером такой конденсации может служить реакция этерификации:
R-COOH + R-OH ↔ RCOOR + H2O
или в общем виде:
A-x + B-y ↔ A-B + X-y
A, B – остатки реагирующих молекул;
x,y – функциональные группы;
x-y – низкомолекулярный побочный продукт.
В этом случае не образуется ВМС, т.к. в продукте реакции отсутствует группы COOH и OH, необходимые для дальнейшего связывания остатков между собой. Однако, если молекулы каждого из исходных соединений не менее двух функциональных групп, конденсация может повторяться сколько угодно раз, и в каждом случае в молекуле продукта реакции останутся неиспользованные на предыдущем этапе функциональные группы и произойдет многократная конденсация, или поликонденсация , приводящая к образованию ВМС.
Растущие цепи могут реагировать не только с мономерами, но и между собой, благодаря наличию в них функциональных групп.
При поликонденсации можно в принципе остановить реакцию путем охлаждения на любой стадии и выделить промежуточные продукты. В рассмотренном нами примере образовывались макромолекулы линейного строения, так как рост цепи происходит в одном направлении. Однако возможны варианты, когда один или оба мономера содержат более двух функциональных групп. В этих случаях макромолекула может расти в нескольких направлениях, что приводит к образованию в зависимости от условий реакции и природы мономера, разветвленной или трехмерной частицы.
Схематично с условием выбранной нами символики этот процесс может быть представлен следующим образом:
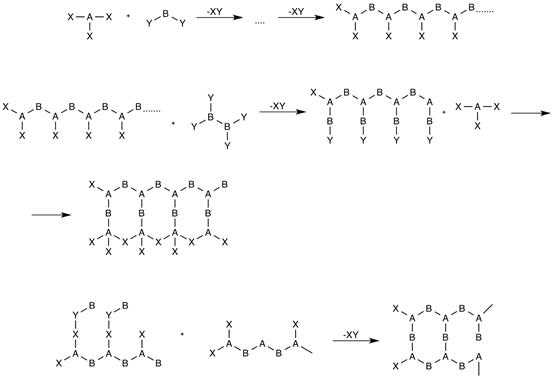
Теоретически рост макромолекулы при поликонденсации прекратится при полном “исчерпании” всех функциональных групп в мономерах и промежуточных продуктах реакции, однако на деле поликонденсат состоит из достаточного большого числа молекул, отличающихся друг от друга величиной (молекулярная полидисперсность). Это объясняется протеканием ряда побочных процессов, обратимостью реакции, возрастанием пространственных затруднений.
В силу всех этих причин реакция поликонденсации обычно останавливается, не доходя до конца. Рассмотрим некоторые понятия и термины, используемые в области процессов поликонденсации:
1) Функциональность мономера - это количество функциональных групп в его молекуле. Таким образом, существуют бифункциональные, трифункциональные, полифункциональные мономеры.
2) Степень исчерпания функциональных групп, называемая полнотой или глубиной поликонденсации, зависит прежде всего от тщательности удаления из зоны реакции низкомолекулярных продуктов, препятствующих смещению равновесия в сторону образования полимера.
3) Степень полимеризации – число элементарных звеньев в макромолекуле. Между молекулярным весом M полимера и степенью полимеризации X существует соотношение X=M/m, где m – молекулярный вес элементарного звена..
Между степенью полимеризации x и глубиной реакции p существует математическая зависимость:
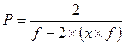 - уравнение Карозерса,
- уравнение Карозерса,
где f-количество функциональных групп, приходящееся в среднем на одну молекулу мономера.
Уравнение Карозерса можно привести к виду:
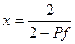
откуда следует, что степень полимеризации x тем больше, чем полнее прошла поликонденсация. Поскольку глубина реакции определяется ее продолжительностью, величина макромолекулы закономерно возрастает в зависимости от времени поликонденсации.
На практике чаще всего поликонденсацию проводят с двумя различными мономерами, каждый из которых содержит функциональные группы только одного типа (например x-A-x и y-B-y), при этом, как было показано В.В. Коршаком, наибольший молекулярный вес полимера наблюдается при строго эквимольном соотношении мономеров. В случае поликонденсации адипиновой кислоты с гексаматилендиалеином (COOH-(CH2)4-COOH + NH2-(CH2)6-NH2), например избыток одного из мономеров всего на 0,09% снижает молекулярный вес полимера в 10 раз.
Поскольку, как уже отмечалось, поликонденсация – процесс равновесный, то для получения большого молекулярного веса полимера необходимо удалять низкомолекулярные продукты из реакционной зоны. Это достигается проведением следующих операций:
1) Продуванием реакционной массы инертным газом (азот, аргон).
2) Применением глубокого вакуума.
3) Проведение поликонденсации на поверхности раздела фаз. (органический растворитель, в котором растворен один из мономеров + водный раствор другого мономера, содержащий агент, связывающий побочный продукт, например, основание, если выделяется HCl).
4) Использование катализаторов.
Важнейшие полимеры, получаемые поликонденсацией:
1) Полиэфиры – образуются в результате конденсации двухатомного спирта с дикарбоновой кислотой.
Например, при реакции терефталевой кислоты и этиленгликоля получают лавсан (терилен - Англия, дакрон - США)
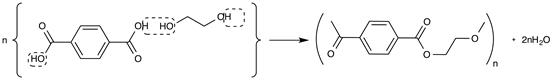
2) Полиамиды – образуются в результате конденсации диаминов с дикарбоновыми кислотами или их дихлорангидридами.
Например, найлон-6,6 идет на получение синтетического волокна:
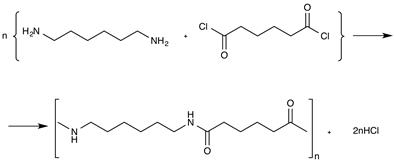
3) Силиконы или силоксаны:
R2SiCl2 + 2H2O → R2Si(OH)2 + 2HCl
nR2Si(OH)2 → (-R2Si-О-)n + nH2O
Получают каучукоподобный пластичный и эластичный полимер, отличающийся термостойкостью до 250оС. Низкомолекулярные жидкие силиконовые олигомеры – смазочные термостойкие масла.
4) Полимочевины – получают при поликонденсации мочевины с формальдегидом или другими альдегидами. Образуются как линейные, так и трехмерные системы:
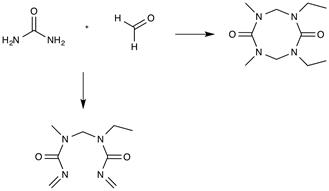
На основе этих полимеров, или смол, горячим прессованием в смеси с целлюлозой, красителями получают бытовые изделия, слоистые облицовочные материалы и т.д.
4) Фенопласты – при конденсации фенолов с альдегидами реакция проводится как с кислым катализатором, так и с основным:
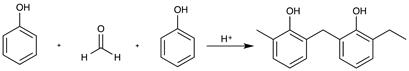
Фенол-альдегидные смолы применяют в виде прессовочных композиций с различными наполнителями, для производства лаков, клеев.
Контрольные вопросы:
1. Схематично запишите реакцию получения полиэтилена.
2. Как осуществляют полимеризацию в промышленных условиях?
3. Приведите структурную формулу бутилкаучука.
4. В чем различие реакций конденсации и поликонденсации?
5. Поликонденсацией можно получить следующие полимеры: а) бутилкаучук; б) полиэфиры; в) полиэтилен; г) полиамиды.
6. Приведите уравнение реакции получения мочевино-формальдегидной смолы.
