Высокомолекулярные углеводы (полисахариды)
Высокомолекулярные углеводы представляют собой основ-ную составляющую органической материи в биосфере планеты. Они выступают в роли структурных компонентов клеток и тканей, энергетического резерва и защитных веществ.
К высокомолекулярным углеводам относятся целлюлоза, крахмал, гликоген, хитин, хитозан, инулин, камеди и пектиновые вещества.
Целлюлоза, или клетчатка, – самый распространенный орга-нический природный полимер, основа клеточных стенок растений. Мономер целлюлозы – циклическая β-глюкоза (рис. 15).
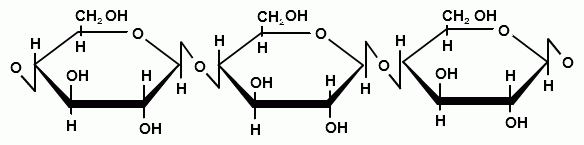
Рис. 15. Целлюлоза – линейный полисахарид
Целлюлоза является жесткоцепным полимерам. Ее макромо-лекулы не образуют спирали. Полимерные цепочки соединяются между собой водородными связями. Такое строение обусловли-вает склонность целлюлозы к образованию волокон. На основе целлюлозы получают искусственные полимеры: метилцеллюлозу, ацетилцеллюлозу, нитроцеллюлозу.
Крахмал накапливается в клубнях, плодах, семенах растений в качестве основного источника резервного питания. Мономеры крах-мала – циклическая α-глюкоза. Крахмал представляет собой смесь двух полимеров: амилозы и амилопектина. Макромолекулы амилозы (рис. 16) имеют степень полимеризации 200 ÷ 1000 и образуют спирали, обусловленные существованием водородных связей.
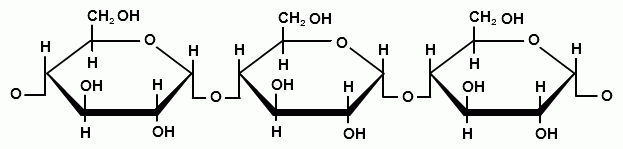
Рис. 16. Амилоза – линейный полисахарид
Амилопектин имеет разветвленное строение и содержит более 10000 структурных звеньев (рис. 17).
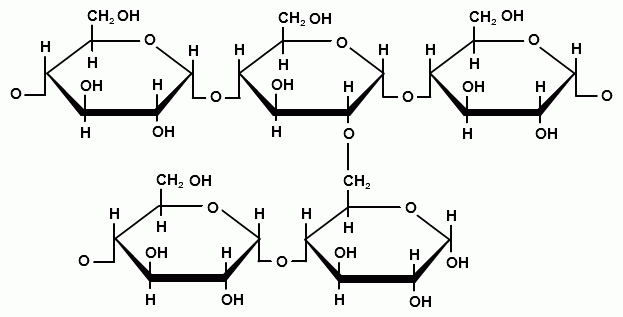
Рис. 17. Амилопектин – разветвленный полисахарид
При нагревании раствора крахмала образуется «клейстер» – коллоидный гель.
Углевод, образующий питательный резерв животных клеток, называется гликогеном. Он имеет химический состав, аналогичный крахмалу, и сильно разветвленную пространственную структуру. При дефиците в живом организме глюкозы гликоген под дей-ствием ферментов распадается и глюкоза поступает в кровь. Синтез и разложение гликогена регулируются с помощью гормонов и нервной системы.
Белки
К белкам (протеинам, полипептидам) относятся органические природные полимеры, образованные α-аминокислотами (рис. 18), которые соединены пептидной связью. Аминокислоты могут содержать в своем составе железо, серу, кобальт, фосфор. В состав белков входят остатки не более 22 α-аминокислот.
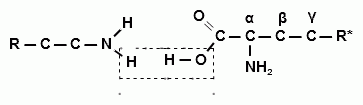
Рис. 18. Поликонденсация α-аминокислот с образованием пептидной связи
На поведение и биохимические свойства белков влияет как химический состав аминокислот, так и их сочетание в макро-молекулах. Разнообразие в химическом составе белков тесно свя-зано с многообразностью их функций.
Основные функции белков:
· транспортная, например гемоглобин;
· регуляторная или гормональная, например инсулин;
· каталитическая – ферменты;
· структурная, механическая, например коллаген;
· резервная – казеин;
· иммунологическая – иммуноглобулины.
Приведем некоторые примеры белков:
· гемоглобин – железосодержащий белок крови, способный обратимо связываться с кислородом. Функция гемоглобина – доставлять кислород к органам и тканям живых организмов;
· инсулин – гормон, вырабатываемый поджелудочной железой. Он оказывает влияние на обмен веществ практически во всех тканях. Основное действие инсулина – снижение концентрации глюкозы в крови;
· коллаген – основа соединительной ткани организма, обус-ловливающий ее прочность и эластичность;
· ферменты – природные катализаторы с их помощью ката-лизируются биохимические процессы в организме.
Молекулярная масса белков может достигать нескольких миллионов у.е. Одна из самых маленьких – молекула инсулина – состоит из 60 аминокислотных звеньев и весит 12000 у.е.
Макромолекулы имеют стереорегулярную структуру, что важно для проявления белками определенных биохимических свойств.
Существуют четыре уровня структурной организации белков:
· первичная структура – линейная последовательность α-ами-нокислотных звеньев (рис. 19);
· вторичные структуры: α-спираль, β-структура (складчатый лист). Вторичные структуры образуются за счет водородных свя-
зей между звеньями одной цепи (α-спираль) и межмолекулярных (β-структура) (рис. 20);
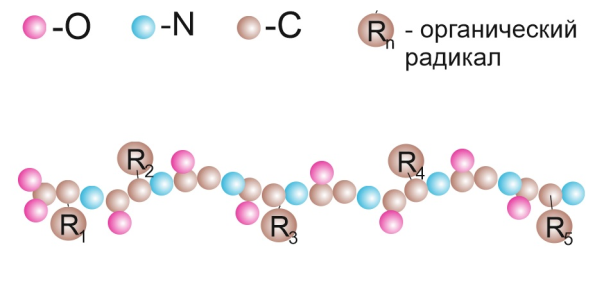
Рис. 19. Первичная структура белка
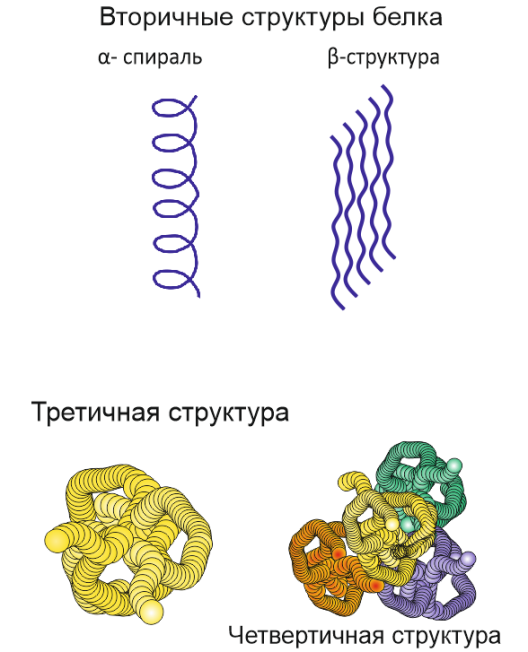
Рис. 20. Уровни структурной организации белков
· третичная структура – способ укладки макромолекул вто-ричной структуры в пространстве. α-спирали чаще образуют эллипсовидные глобулы (глобулярные белки), а β-структуры – вытянутые (фибриллярные белки) (рис. 20). Третичные структуры закрепляются как силами Ван-дер-Ваальса, так и ковалентными дисульфидными мостиками (–S–S–);
· четвертичная структура – способ укладки нескольких макромолекул белка третичной структуры в пространстве (рис. 20).
В природе существует около 1012 всевозможных белков, обеспечивающих жизнь различных организмов, от вирусов до человека. Каждому виду присущ свой набор белков. Последовательность α-аминокислот в полипептидной цепи предопределяет информация, содержащаяся в ДНК живых организмов.
Полинуклеиновые кислоты
Полимерные нуклеиновые кислоты – дезоксирибонуклеиновая (ДНК) и рибонуклеиновая (РНК) – природные ВМС, выполняющие функцию хранения и передачи наследственной информации.
Мономерное звено нуклеиновых кислот – нуклеотиды. В состав нуклеотидов входят:
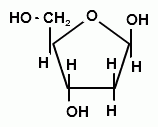
1) моносахарид – рибоза или дезоксирибоза (рис. 21);
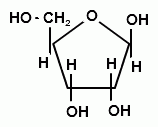
| а) |
| б) |
Рис. 21. Моносахариды нуклеотидов: а – рибоза, б – дезоксирибоза
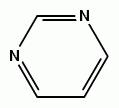
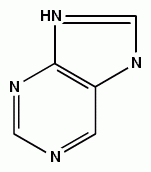
2) азотистое основание – пуриновое или пиримидиновое (рис. 22). Пиримидиновые основания нуклеотидов ДНК: тимин (T) и цитозин (C). Пуриновые основания нуклеотидов: гуанин (G) и аденин (A). В молекулах РНК вместо тимина присутствует урацил (У);
| а) |
| б) |
Рис. 22. Азотистые основания: а – пиримидин, б – пурин
3) остаток фосфорной кислоты (рис. 23).
Чередование фрагментов в нуклеиновых кислотах показано на рис. 24. Нуклеиновые кислоты подобно белкам имеют первичную структуру – последовательность нуклеотидов (рис. 24), вторичную структуру – две комплементарные цепи – двойная спираль ДНК, и третичную – пространственную структуру.
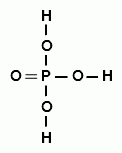
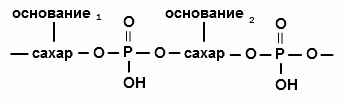
| Рис. 23. Фосфорная кислота |
| Рис. 24. Чередование фрагментов в нуклеиновых кислотах |
Две макромолекулы ДНК образуют двойную спираль, закру-ченную по часовой стрелке (правую спираль), и удерживаются друг с другом за счет водородных связей между азотистыми основаниями (рис. 25, 26).
Причем тот или другой пурин в одной молекуле связан во-дородными связями с тем или иным пиримидином в другой. Аде-нин связывается с тимином, а гуанин с цитозином. Такое соответствие называется комплементарным (взаимодополняющим).
Функции ДНК:
· хранение наследственной (генетической информации). Химическая база этой функции – комплементарность;
· способность к репликации (удвоению) и копированию рас-положения в цепи азотистых оснований, определяемая свойством ДНК хранить и использовать генетическую информацию;
· способность молекул ДНК управлять синтезом белков, характерных для организмов данного вида.
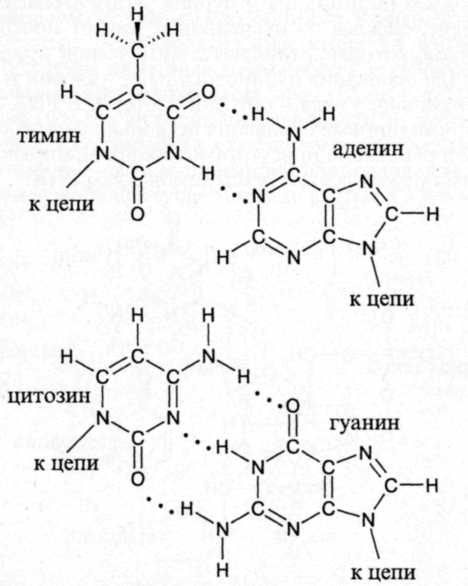
Рис. 25. Попарно связанные водородными связями тимин с аденином и цитозин с гуанином при образовании спирали при скручивании двух макромолекул ДНК вокруг общей оси
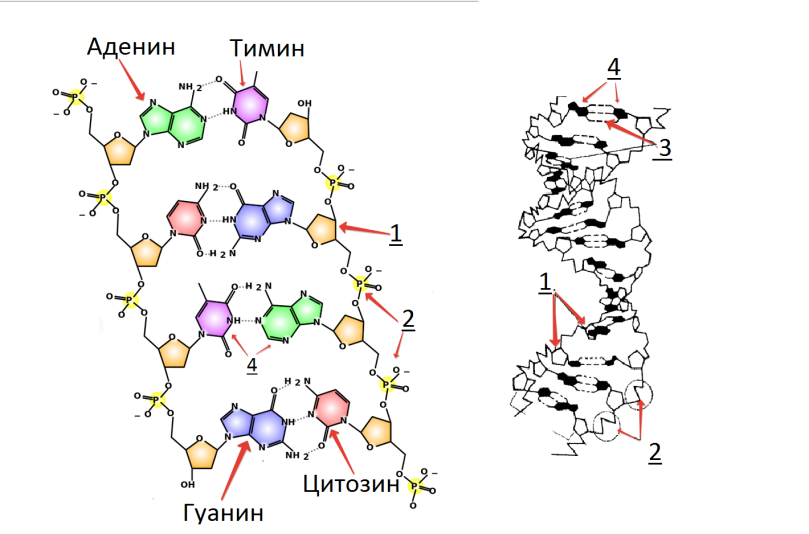
Рис. 26. Двойная спираль ДНК: 1 – сахар (дезоксирибоза), 2 – остаток фосфорной кислоты, 3 – водородная связь, 4 – пара оснований
Функции РНК:
· транспортная (осуществляется транспортной т-РНК) – перенос аминокислот к месту синтеза белка, в рибосомы. Рибосомы представляют собой нуклеопротеид, в составе которого находятся РНК и белок. Рибосомы служат для биосинтеза белка из ами-нокислот по заданной матрице на основе генетической информа-ции, предоставляемой матричной РНК (м-РНК). Этот процесс называется трансляцией. Трансляция (осуществляется рибосомной р-РНК) – считывание информации с м-РНК при помощи молекул т-РНК и катализ создания пептидных связей между доставленными к т-РНК α-аминокислотами;
· информационная (осуществляется матричной м-РНК) – пере-нос информации о структуре белка от ДНК к месту синтеза белка в рибосомах. М-РНК синтезируется на основе ДНК в ходе тран-скрипции;
· транскри́пция – процесс синтеза РНК с использованием ДНК в качестве матрицы, происходящий во всех живых клетках. Другими словами, это перенос генетической информации с ДНК на РНК.
8. Неорганические
и элементорганические полимеры
Круг соединений, которые по своему строению можно отнести к высокомолекулярным, не ограничивается полимерами с угле-родными цепями. Многие неорганические природные и синтети-ческие вещества также имеют полимерное строение. В общем случае все минералы земной коры представляют собой высокомолекулярные вещества.
Асбест, базальт, кварц и песок, корунд и многие другие ми-нералы состоят из повторяющихся по составу и структуре моно-мерных звеньев, связанных в длинные, разветвленные цепочки или объемные структуры.
Диоксид кремния (кремнезем) встречается в природе в виде песка или кварца и входит в состав большинства природных минералов. Каждый атом кремния в кристаллах (SiO2)n окружен четырьмя атомами кислорода, каждый из которых является мостиком к следующему атому кремния (рис. 27).
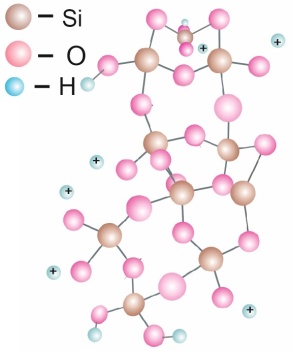
| Рис. 28. Поликремниевая кислота |
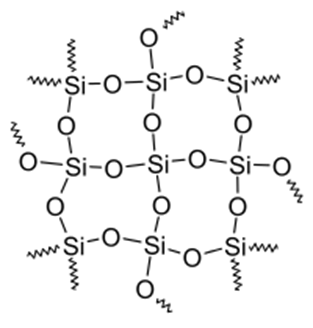
| Рис. 27. Диоксид кремния |
Через общий атом кислорода тетраэдры SiO4 под разными углами связываются друг с другом, образуя трехмерную решетку; взаимное расположение тетраэдров SiO4 в пространстве опреде-ляет ту или иную модификацию кремнезема. Поверхностные атомы образуют Si–O–Н- или Si–O–Si-группы. Таким образом, кремнезем можно представить как поликремниевую кислоту состава n(SiO2)∙mН2O (рис. 28).
Глину можно представить как смесь высокомолекулярных соединений, построенных из плоских полимерных блоков двух типов: кремнийкислородного и алюмокислородного.
В гранитах полимерная цепь построена из атомов кремния и алюминия, связанных между собою через кислородные мостики.
Асбесты – тонковолокнистые минералы из класса силикатов. По химическому составу асбесты представляют собой водные силикаты магния с примесями оксидов железа. Природные асбесты состоят из тонких гибких волокон. Способность асбеста к волокнообразованию позволяет использовать его для создания огнестойких тканей, шнуров и т.д.
Огнестойкие теплоизоляционные материалы также изготавли-вают из базальтового волокна, которое получают из базальта путем расплава природного минерала и последующего преобра-зования в волокно без применения химических добавок.
Природные минералы, как правило, представляют собой гете-роцепные полимеры.
К гомоцепным неорганическим полимерам относят аллотроп-ные модификации углерода, серы, селена, бора и проч.
К синтетическим неорганическим соединениям можно отнести как многочисленные силикатные строительные материалы, стекла, так и цеолиты, искусственные минералы.
Следует упомянуть неорганический каучук – полифосфо-
нитрилхлорид, негорючий аналог синтетических каучуков.
К элементорганическим относят полимеры, содержащие в эле-ментарном звене макромолекулы наряду с углеводородными груп-пами неорганические фрагменты, т.е. углерод связан с атомами, отличными от кислорода, водорода, азота, серы, галогенов.
Известны элементорганические полимеры, содержащие фос-фор, бор, кремний, алюминий, олово и проч., с широким спектром свойств. Среди них существуют термостойкие полимеры, по-лимеры с хорошей электропроводностью и полупроводнико-
выми свойствами, с высокой твердостью и эластичностью и др. Элементорганические полимеры часто используют в качестве стабилизаторов полимеров, антигрибкових и антимикробных добавок в лакокрасочные материалы.
Наибольшее применение находят кремнийорганические поли-меры – полиорганосилоксаны.
Полисилоксаны содержат в основной неорганической цепи кислород и кремний (…–Si–O–Si–O–Si–O–…). К атомам кремния присоединяются боковые органические группы. Иногда боковые группы могут соединять вместе две (или более) кремнийоргани-ческие цепи. Варьируя длину основной цепи и боковые группы, можно синтезировать полимеры с разными свойствами.
Основное применение кремнийорганические полимерные материалы находят для создания термостойких и атмосферостойких покрытий, термостойких материалов, гидрофобизирующих жидкостей, герметиков и смазок.
Вопросы для самопроверки
1. Какая кислота имеет полимерное строение?
Варианты ответов:
1) олеиновая CH3-(CH2)7-CH=CH-(CH2)7-COOH,
2) кремниевая,
3) серная,
4) ортофосфорная.
2. Укажите структурное звено макромолекулы:
...-CH2-CH=CH-CH2-CH2-CH=CH-CH2-CH2-CH=CH-CH2-...
Варианты ответов:
1) -CH2-CH=CH- ,
2) -CH=CH-CH2-CH2- ,
3) =CH-CH2-CH2-CH= ,
4) -CH2-CH=CH-CH2- .
3. Степень полимеризации макромолекулы равна ...
Варианты ответов:
1) отношению массы мономера к массе образовавшегося полимера,
2) выходу полимера в реакции его образования,
3) отношению молекулярной массы структурного звена к молекулярной массе макромолекулы,
4) отношению молекулярной массы макромолекулы к молекулярной массе структурного звена.
4. Чему равна молекулярная масса макромолекулы полиэти-лена, если степень полимеризации n = 1000 ?
Варианты ответов:
1) 140 000 ,
2) 42 000 ,
3) 28 000 ,
4) 10 000.
5. Какова геометрическая форма макромолекул:
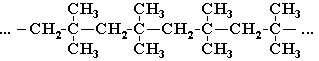
Варианты ответов:
1) разветвленная,
2) линейная,
3) пространственная,
4) перпендикулярная.
6. Определите геометрическую форму макромолекул полимеров А и Б
Варианты ответов:
1) А – линейная форма, Б – пространственная форма;
2) А – линейная форма, Б – разветвленная форма;
3) А – разветвленная форма, Б – пространственная форма;
4) А – пространственная форма, Б – разветвленная форма.
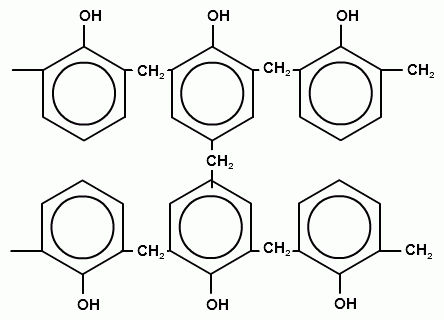
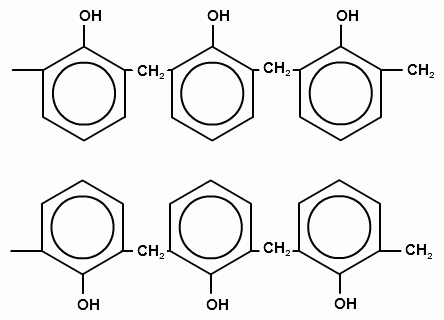
А Б
7. При переработке полимеров в изделия часто используют метод литья расплава полимера в заготовленные формы. Какие полимеры можно использовать на этой стадии переработки?
Варианты ответов:
1) только линейные,
2) линейные и разветвленные,
3) пространственные,
4) любые.
8. Какие признаки отличают полимеры от низкомолекулярных соединений:
а) плохая растворимость; е) эластичность;
б) набухание при растворении; ж) низкая хрупкость;
в) низкая вязкость растворов; з) термопластичность;
г) высокая вязкость растворов; и) термореактивность;
д) неспособность к кристаллизации; к) электропроводность?
Варианты ответов:
1) б, г, е, ж;
2) а, б, д, з, и, к;
3) б, г, д, е, з, и;
4) а, б, в, ж, к.
9. Какие свойства полимеров можно объяснить гибкостью макромолекул:
а) высокая температура разложения;
б) эластичность каучуков;
в) прочность органических стекол;
г) анизотропию свойств?
Варианты ответов:
1) а, б;
2) г;
3) б, в, г;
4) б, в.
10. Сравните гибкость макромолекул:
А. [-СО-(CH2)5-NН-]n; Б. [-CH2-CH(CH3)-]n.
Варианты ответов:
1) А = Б,
2) А > Б,
3) А < Б,
4) в таких полимерах гибкость не проявляется.
11. Какие полимеры могут использоваться в производстве волокон?
Варианты ответов:
1) линейные, гибкоцепные;
2) пространственные, жесткоцепные;
3) линейные, жесткоцепные;
4) линейные и разветвленные, гибкоцепные.
12. Укажите признаки реакции полимеризации:
а) реакция замещения; д) процесс ступенчатый;
б) реакция отщепления; е) разный элементный состав
полимера и мономера;
в) реакция присоединения; ж) одинаковый элементный
состав полимера
г) процесс цепной;
Варианты ответов:
1) б, д, ж;
2) в, г, ж;
3) в, д, е;
4) а, г, е.
13. К какому типу реакций относится поликонденсация?
Варианты ответов:
1) присоединения,
2) замещения,
3) изомеризации,
4) окисления-восстановления.
14. Укажите соединения, которые можно использовать в каче-стве мономеров в полимеризации:
а) HOOC-CH=CH-COOH г) C2H5-C6H4-COOH
б) CH2=CCl2 д) H2N-(CH2)5-COOH
в) HO-CH2CH2-OH е) HO-CH2CH2CH2-COOH
Варианты ответов:
1) в, д, е;
2) б;
3) в, д;
4) а, б.
15. Укажите соединения, которые можно использовать в каче-стве мономеров в поликонденсации:
а) CH3(CH2)3COOH г) CH2=CH-COOH
б) NH2(CH2)2COOH д) HOOC-CH=CH-COOH
в) HO(CH2)3COOH e) HOCH2CH2OH
Варианты ответов:
1) г,д;
2) в, г;
3) б, в, д+е;
4) а+г, б, е.
16. Какой мономер использован для получения полимера:
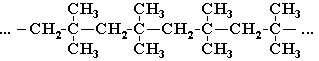
Варианты ответов:
1) CH2=CH-CH3,
2) CH2=C(CH3)-CH=CH2,
3) CH2= C(CH3)2,
4) CH2=CH-CH=CH2.
17. Какова формула мономера, если при его полимеризации образуются макромолекулы следующего строения:
...-CH2-CCl=CH-CH2-CH2-CCl=CH-CH2-... ?
Варианты ответов:
1) Cl-CH2-CH=CH-CH2-Cl,
2) CH2=CCl-CH=CH2,
3) CH2=CH-CH=CH2-Cl,
4) CH2Cl-CH=CH-CH=CH2.
18. Какая формула соответствует капрону?
Варианты ответов:
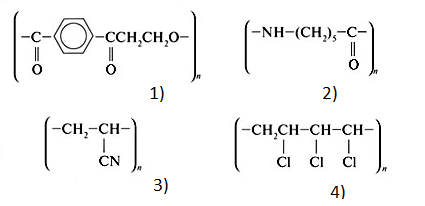
19. Укажите составные части структурного звена полинуклео-тидов (нуклеиновых кислот).
Варианты ответов:
1) азотистое основание, остаток глюкозы и остаток фосфор-ной кислоты;
2) азотистое основание, рибоза (или дезоксирибоза) и остаток фосфорной кислоты;
3) гетероциклическое основание, рибоза (или дезоксирибоза) и остаток фтороводородной кислоты;
4) азотистое гетероциклическое основание, углеводородный остаток и остаток фтороводородной кислоты.
20. Макромолекулы каких природных полимеров склонны к образованию спиралей:
а) амилоза; г) нуклеиновые кислоты;
б) амилопектин; д) натуральный каучук;
в) белки; ж) целлюлоза?
Варианты ответов:
1) а, б, д, ж;
2) г, ж;
3) б, в, г;
4) а, в, г, д.
21. Какой способ используется для получения искусственных полимеров?
Варианты ответов:
1) полимеризация,
2) химическое превращение природных полимеров,
3) сополиконденсация,
4) химическое превращение синтетических полимеров.
22. Какой полимер обладает термопластичностью?
Варианты ответов:
1) каучук,
2) резина,
3) эбонит,
4) асбест.
23. Какое вещество относиться к реактопластам?
Варианты ответов:
1) каучук,
2) резина,
3) эбонит,
4) полиэтилен низкого давления.
24. К неорганическим природным полимерам относится:
Варианты ответов:
1) эбонит,
2) лавсан,
3) целлюлоза,
4) асбест.
25. К кремнийорганическим полимерам относится:
Варианты ответов:
1) кремнезем,
2) силоксан,
3) целлюлоза,
4) фторопласт.
26. Белок, который осуществляет перенос кислорода из легких к органам и тканям человека и животных, называется ...
Варианты ответов:
1) альбумин,
2) инсулин,
3) протеин,
4) гемоглобин.
27. Протекание процесса вулканизации каучука обусловлено наличием в макромолекулах …
Варианты ответов:
1) двойных связей,
2) тройных связей,
3) сил Ван-дер-Ваальса,
4) карбонильных групп.
28. Макромолекулы белков построены из остатков:
Варианты ответов:
1) b-глюкозы,
2) a-глюкозы,
3) b-аминокислот,
4) a-аминокислот.
29. Полимеры, образующиеся в результате сшивки цепей при вулканизации и при получении термореактивных смол, называ-ются ...
Варианты ответов:
1) стереорегулярными,
2) сетчатыми,
3) аморфными,
4) кристаллическими.
30. Как называется полимер по номенклатуре IUPAK
(-CH2-CH2-)n?
Варианты ответов:
1) лавсан,
2) полиэтилен,
3) полиметилен,
4) полистирол.
Вопросы к зачету и экзамену
1. Полимерное состояние вещества. Физические свойства полиме-ров.
2. Строение и химические свойства полимеров. Номенклатура.
3. Термомеханические свойства полимеров.
4. Конформации полимеров.
5. Получение полимеров. Реакции полимеризации и поликонденсации.
6. Классификация ВМС по происхождению и составу.
7. Органические природные полимеры. Белки.
8. Органические природные полимеры. Углеводы.
9. Органические природные полимеры. Нуклеиновые кислоты.
10. Неорганические и элементорганические полимеры.
11. Полимерные материалы. Наполнители и пластификаторы.
12. Растворы полимеров. Коллигативные свойства.
О Г Л А В Л Е Н И Е
1. Общие сведения о высокомолекулярных соединениях. 3
1.1. Классификация веществ по молекулярной массе. 3
1.2. Классификация ВМС по происхождению и элементарному составу. 4
2. Основные понятия физикохимии полимеров. 5
2.1. Классификация ВМС по химическому составу и структуре. 5
2.2. Тривиальная, рациональная и систематическая номенклатура поли-меров. 9
2.3. Молекулярно-массовые характеристики полимеров. 12
2.4. Физическая структура и состояния полимеров. 13
2.4.1. Гибкость цепей полимеров. 13
2.4.2. Физические и фазовые состояния полимеров. 16
3. Производство высокомолекулярных соединений. 25
3.1. Методы получения синтетических полимеров. 26
4. Химические реакции полимеров. 29
5. Растворы полимеров. 32
6. Полимерные материалы и их групповая классификация. 34
6.1. Пластификация полимеров. 36
7. Природные органические полимеры.. 37
7.1. Натуральный каучук. 38
7.2. Высокомолекулярные углеводы (полисахариды) 39
7.3. Белки. 41
7.4. Полинуклеиновые кислоты.. 44
8. Неорганические и элементорганические полимеры.. 47
Вопросы для самопроверки. 49
Вопросы к зачету и экзамену. 57
Барунин Анатолий Анатольевич, Маслобоев Дмитрий Степанович, Фатина Александра Анатольевна
