Агрегатные состояния веществ
Вещества могут находиться в четырех агрегатных состояниях: газообразном, жидком, твердом или плазменном.
Газообразное состояние вещества характеризуется большими расстояниями между частицами (молекулами, атомами). В газах силы взаимодействия между частицами малы и частицы движутся хаотически. Форма и объем газа определяются формой и объемом сосуда, в котором находится газ.
В жидкости расстояние между составляющими ее частицами (молекулами, атомами, ионами) меньше, чем в газе, и частицы не могут перемещаться свободно и независимо друг от друга. Жидкость занимает определенный объем, а ее форма определяется формой сосуда, в котором она находится. Только в очень малых количествах жидкость сохраняет форму капли. Поэтому жидкости занимают промежуточное положение между газами и твердыми веществами.
В твердом веществе расстояния между частицами (молекулами, атомами, ионами) малы и силы их взаимодействия велики. Твердое тело имеет определенный объем и форму, его частицы не перемещаются свободно, а расположены определенным образом в пространстве по отношению друг к другу. Частицы твердого вещества колеблются около равновесных положений. Различают две формы твердого вещества — кристаллическую и аморфную. В кристаллическом веществе частицы располагаются в пространстве в определенном порядке и образуют кристаллическую решетку. В аморфном веществе они располагаются беспорядочно. Одно и то же вещество можно получить как в кристаллической, так и в аморфной форме.
Плазма — это газ, состоящий из положительно и отрицательно заряженных частиц, общий заряд которых равен нулю. Чтобы перевести вещество из газообразного состояния в плазму, нужно его атомы превратить в ионы (т. е. ионизировать газ), оторвав от них электроны (все или часть). Ионизация газа происходит при нагревании до высоких температур порядка нескольких десятков тысяч градусов и больше, при действии ультрафиолетового излучения или электрического разряда.
Верхние слои атмосферы состоят из плазмы. Молнии, северное сияние, световые рекламы (аргоновые или неоновые) — это явления плазмы. На Солнце вещества находятся в плазменном состоянии.
Кристаллические решетки
Кристаллы каждого вещества имеют характерную форму (кристаллы хлорида натрия NaCl имеют форму куба, кристаллы сульфата калия K2SO4 — форму ромба, нитрата кальция Ca(NO3)2 – октаэдров).
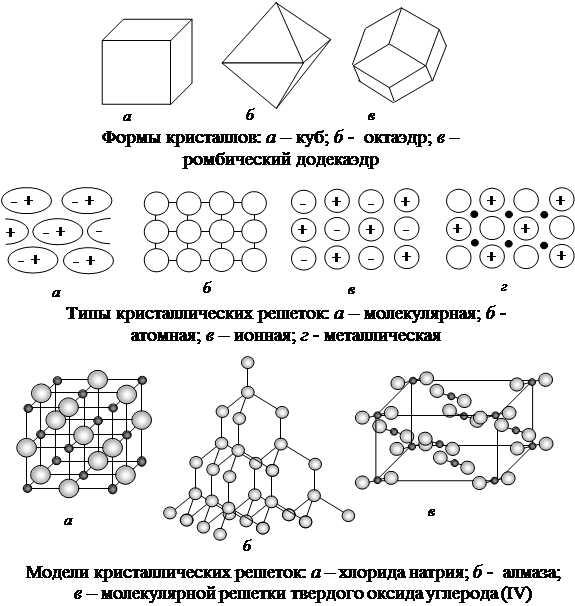 |
В узлах ионной решетки расположены положительные и отрицательные ионы. Вокруг каждого положительного иона располагаются отрицательные ионы, а вокруг отрицательного иона – положительные. Например, в кристаллической решетке хлорида натрия каждый ион С1- окружают шесть ионов Na+, а каждый ион Na+ – шесть хлорид-ионов.
Число частиц (атомов, молекул, ионов), которые окружают данную частицу в кристаллической решетке или в молекуле, называется координационным числом.
Все ионные соединения имеют высокую температуру плавления и нелетучи.
В узлах атомной решетки располагаются атомы, связанные между собой электронными парами (кристаллы алмаза). Для веществ с атомной решеткой характерны высокая твердость и высокие температуры плавления.
В узлах молекулярной решетки располагаются полярные или неполярные молекулы. Они связаны между собой более слабыми силами, чем атомы или ионы. Поэтому вещества с молекулярными решетками имеют сравнительно невысокую температуру плавления, они летучи (сахар, вода, аммиак).
В узлах металлической решетки располагаются нейтральные атомы и положительные ионы данного металла. Между ними свободно перемещаются электроны. Этим обусловлены общие свойства металлов: металлический блеск, пластичность, электрическая проводимость и теплопроводность.
ХИМИЧЕСКИЕ РЕАКЦИИ И ЗАКОНОМЕРНОСТИ
ИХ ПРОТЕКАНИЯ
Химические свойства веществ проявляются в химических реакциях. Химическая реакция изображается в общем виде уравнением
aA + bB = cC + dD,
где вещества А и В, вступающие в реакцию, называют реагентами (или исходными веществами), а новые вещества C и D, образующиеся в результате протекания реакции, - продуктами (или конечными веществами). Целочисленные параметры a, b, c и d в уравнении реакции называют стехиометрическими коэффициентами.
Типы химических реакций
I. По типу взаимодействия реакции можно разделить на такие типы:
1) реакции соединения, при которыхиз двух или нескольких веществ получают одно вещество:
в общем виде А + В+. . . = С;
2Mg + О2 = 2MgO; SO2 + Н2О = Н2SО3
2) реакции разложения, при которыхиз одноговеществаобразуется несколько веществ:
в общем виде С = А + В. . . ;
2HgO = 2Hg + O2; Сu (ОН)2 = СuО + Н2О
3) реакции замещения, при которых простое вещество замещает составную часть сложного вещества и в результате образуются новое простое и новое сложное вещества:
в общем виде АВ + С = АС + В;
Н2SО4 + Zn = ZnSO4 + Н2
4) реакции двойного обмена, при которых молекулы сложных веществ обмениваются своими составными частями:
в общим виде AB + CD = AD + CB,
Fе(ОН)3 + 3НС1 = FeCl3 +3H2O
II. По изменению степеней окисления элементов, которые входят в состав реагирующих веществ, выделяют
1) обменные реакции, протекающие без изменения степеней окисления всех элементов, входящих в исходные вещества
K+1O-2H+1 + H+1Br-1 = K+1Br-1 + H2+1O-2.
2) окислительно-восстановительные реакции, протекающие с изменением степеней окисления всех или некоторых элементов
C0 + O20 = C+4O2-2
III. По тепловому эффектуреакции делят на
1) экзотермические реакции, протекающие с выделением энергии в форме теплоты (+Q)
H2 + Cl2 = 2HCl + Q.
2) эндотермические реакции, протекающие с поглощением энергии в форме теплоты (-Q)
N2 + O2 = 2NO – Q.
IV. По направлению:
1) необратимые реакции, которые протекают только в прямом направлении и завершаются полным превращением реагентов в продукты (т.е. реакции идут до конца слева направо)
Al2S3 + 6H2O = 2Al(OH)3↓ + 3H2S↑
2) обратимые реакции, которые протекают одновременно в прямом и обратном направлениях, при этом реагенты превращаются в продукты лишь частично (т.е. реакции не идут до конца слева направо)
3H2 + N2 ↔ 2NH3
Существуют и другие признаки, по которым классифицируют химические реакции.Одна и та же реакция в зависимостиот признака классификации может относиться к разным типам реакций.
Химическая кинетика
Количественной характеристикой быстроты течения химической реакции является ее скорость. За скорость химической реакции принимают изменение количества реагирующего вещества (или продукта) во времени в единице объема реакционной системы. Учение о механизмах и скоростях химических реакций называется химической кинетикой.
Например, Ai – одно из реагирующих веществ или продуктов реакции. В момент времени t1, в объеме V содержалось вещество A количеством n1(Ai), в момент времени t2 в том же объеме количество вещества A равно n2(Ai). Тогда скорость реакции u по веществу Ai составит:
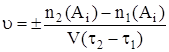
Введем обозначения: 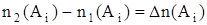 - изменение количества вещества Ai;
- изменение количества вещества Ai; 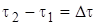 - промежуток (изменение) времени и, подставив их в уравнение, получаем
- промежуток (изменение) времени и, подставив их в уравнение, получаем
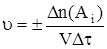
Учитывая, что
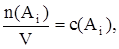
получаем
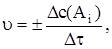
где c(Ai) – молярная концентрация – количество вещества, содержащееся в единице объема, моль/л или моль/м3.
Таким образом, скорость реакции – это изменение концентрации реагирующего вещества в единицу времени. Единица измерения скорости – моль/(м3´с) или моль/(л´с).
Скорость химической реакции зависит от нескольких факторов.
1. Природа реагентов. Энергией активации Еа (в кДж/моль) называют избыточную энергию, которой должны обладать молекулы для того, чтобы их столкновение могло привести к образованию нового вещества. Еа различных реакций различна. Посредством этого фактора сказывается влияние природы реагирующих веществ на vх.р.. Если Еа<40 кДж/моль (т.е. мала), то скорость такой реакции велика (например, ионные реакции в растворах, протекающие практически мгновенно). Если Еа>120 кДж/моль (т.е. очень значительна), то скорость такой реакции незначительна (например, реакция синтеза аммиака N2+3H2=2NH3 – скорость этой реакции при обычных Т вследствии высоких значений Еа настолько мала, что заметить её протекание практически невозможно).
В 1889 г. знаменитый шведский химик Аррениус вывел из опытных данных уравнение, связывающее константу скорости с температурой и энергией активации. Позднее это уравнение получило теоретическое обоснование. Согласно Аррениусу, константа скорости находится в экспоненциальной зависимости от температуры: k=kmax×exp(-Ea/RT), где R - универсальная газовая постоянная, равная 8,31 Дж/моль×К; kmax - предэкспоненциальный фактор, имеющий смысл максимально возможного значения константы скорости при нулевой энергии активации или бесконечно высокой температуре, когда все столкновения молекул реагентов становятся активными. Уравнение Аррениуса используют чаще в логарифмической форме: lnk=lnkmax-Ea/RT.
2. Концентрация реагирующих веществ. В соответствии с основным законом химической кинетики для реакции
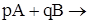 продукты
продукты
скорость выражается следующим соотношением:
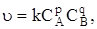
где k – константа скорости реакции; p и q – коэффициенты (определяются экспериментально). Для некоторых простейших реакций коэффициенты p и q равны стехиометрическим коэффициентам уравнения реакции. Например, для реакции
H2(г) + I2(г) ® 2HI(г)
можно записать
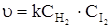
т.е. 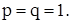
3. Температура реакции. Зависимость скорости реакции от температуры передается уравнением Вант-Гоффа:
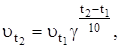
где 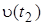 и
и 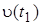 - скорости реакции при температурах t2 и t1; g - температурный коэффициент скорости реакции (для многих реакций
- скорости реакции при температурах t2 и t1; g - температурный коэффициент скорости реакции (для многих реакций
g = 2…4). Это правило говорит о том, что скорость реакций возрастает в 2 - 4 раза при увеличении температуры на 100C.
4. Поверхность соприкосновения реагентов. Чем больше поверхность соприкосновения реагирующих веществ, тем быстрее протекает реакция. Реакция в растворах протекает практически мгновенно.
5. Катализаторы – это вещества, не расходующиеся в реакции, но оказывающие влияние на её скорость. Явление изменения скорости реакции под действием катализаторов называется катализом, а сами эти реакции являются каталитическими. Действие катализатора обусловлено снижением величины энергии активации. Под воздействием катализаторов реакции могут ускоряться в миллионы и более раз.
Различают гомогенный и гетерогенный катализ. При гомогенном катализе катализатор и реагенты образуют одну фазу (газ или раствор), а при гетерогенном катализе – катализатор находится в системе в виде самостоятельной фазы. Примером гомогенного катализа служит разложение перекиси водорода на воду и кислород в присутствии катализаторов К2Cr2O7, К2WO4 и др. Примером гетерогенного катализа является окисление диоксида серы в триоксид при контактном способе получения серной кислоты из отходящих газов металлургических производств: SO2+0,5O2+H2O=(NO2)=H2SO4.
Задание. В сосуде вместимостью 2 л смешали 4,5 моль газа А и
3 моль газа В. Газы А и В реагируют в соответствии с уравнением
А + В = 2С.
Через 2 с в реакционной системе образовался газ С количеством вещества 1 моль. Определите среднюю скорость реакции. Рассчитайте количества веществ газов А и В, которые не прореагировали.
Дано: 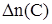 = 1 моль = 1 моль 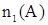 = 4,5 моль = 4,5 моль 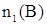 = 3 моль V = 2 л = 3 моль V = 2 л 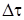 = 2 с = 2 с | Решение: 1.Из уравнения реакции следует, что 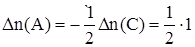 моль = 0,5 моль, где моль = 0,5 моль, где 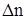 - изменение количества вещества в ходе реакции, знак «-» означает, что вещество А расходуется в ходе реакции. 2. Аналогично получаем для вещества В - изменение количества вещества в ходе реакции, знак «-» означает, что вещество А расходуется в ходе реакции. 2. Аналогично получаем для вещества В 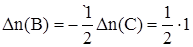 моль = 0,5моль. 3. Вычисляем количество вещества А, которое вступило в реакцию: моль = 0,5моль. 3. Вычисляем количество вещества А, которое вступило в реакцию: 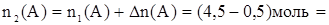 4 моль 4. Количество вещества В, которое осталось в реакционной смеси, равно: 4 моль 4. Количество вещества В, которое осталось в реакционной смеси, равно: 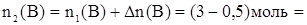 2,5 моль 5. Среднюю скорость реакции за данный промежуток времени вычисляем по формуле 2,5 моль 5. Среднюю скорость реакции за данный промежуток времени вычисляем по формуле 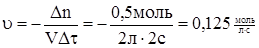 Ответ: 4 моль, 2,5 моль, 0,125 Ответ: 4 моль, 2,5 моль, 0,125 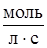 |
Задание. Во сколько раз увеличится скорость реакции
H2 + I2 = 2HI,
если увеличить количества вещества иода и водорода в реакционной системе в два раза при постоянном объеме.
Дано: 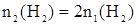 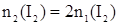 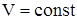 | Решение: В соответствии с основным законом химической кинетики: 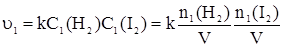 Аналогично для скорости u2, когда количества реагентов увеличились, имеем: Аналогично для скорости u2, когда количества реагентов увеличились, имеем: 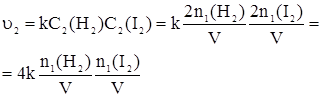 Определяем, во сколько раз увеличилась скорость реакции Определяем, во сколько раз увеличилась скорость реакции 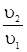 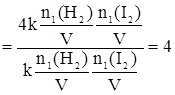 Ответ: Скорость реакции увеличится в 4 раза. Ответ: Скорость реакции увеличится в 4 раза. |
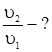 | |
Задание. Реакция при температуре 50 °С протекает за 2 мин 15 с. За сколько времени закончится эта реакция при 70 °С, если в данном температурном интервале температурный коэффициент скорости реакции равен 3?
Дано: t1 = 500C t2 = 700C Dt1= 2 мин.15с = =135 с 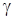 = 3 = 3 | Решение: 1. С использованием правила Вант-Гоффа вычисляем, во сколько раз увеличится скорость реакции при увеличении температуры с 50 до 700С 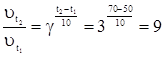 2. По определению скорости 2. По определению скорости 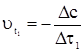 ; ; 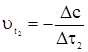 Так как при обеих температурах Так как при обеих температурах 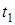 и и 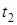 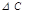 одинаково, получаем: одинаково, получаем: 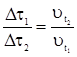 ; ; 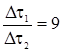 3. Вычисляем время, за которое реакция произойдет при температуре 700C: 3. Вычисляем время, за которое реакция произойдет при температуре 700C: 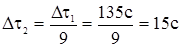 Ответ: 15 с. Ответ: 15 с. |
Константа равновесия
Характерной гомогенной обратимой реакцией является синтез аммиака.
3H2 + N2 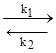 2NH3
2NH3
k1 и k2 – константы скоростей прямой и обратной реакций соответственно. Запишем выражения для скоростей прямой и обратной реакций:
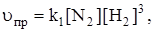
[N2] и [H2] – концентрации азота и водорода в состоянии равновесия, т.е. равновесные концентрации.
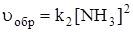 .
.
В начальный момент времени uобр = 0, т.к. [NН3]= 0. По мере увеличения концентрации аммиака и уменьшения концентраций исходных веществ uпр уменьшается, а uобр увеличивается. В определенный момент времени наступает динамическое равновесие, т.е. uпр = uобр и 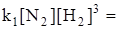
 . Отношение констант скоростей прямой и обратной реакции называется константой равновесия. Она равна произведению концентраций продуктов реакций в степенях их стехиометрических коэффициентов. Деленному на произведение концентраций исходных веществ, также в степенях их стехиометрических коэффициентов.
. Отношение констант скоростей прямой и обратной реакции называется константой равновесия. Она равна произведению концентраций продуктов реакций в степенях их стехиометрических коэффициентов. Деленному на произведение концентраций исходных веществ, также в степенях их стехиометрических коэффициентов.
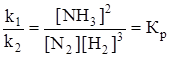
Рассмотрим случай обратимой гетерогенной реакции:
СО2(г) + С(тв) 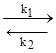 2СО.
2СО.
В реакторе лежит уголь, над которым пропускают СО2. СО2 взаимодействует с верхним слоем угля, при этом открывается следующий слой угля, т.е. концентрация атомов углерода не меняется:
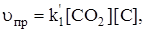
[C] = const, 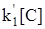 = const = k1,
= const = k1,
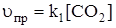 .
.
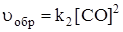
uпр = uобр и 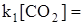
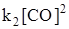 .
.
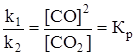
Концентрация твердых фаз не входит в выражение для константы скорости.
Смещение равновесия
В соответствии с принципом Ле Шателье, если на систему, находящуюся в состоянии равновесия, оказать внешнее воздействие, то равновесие сместится в сторону протекания той реакции, которая ослабляет это воздействие.
На примере
3H2 + N2 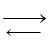 2NH3 – DH.
2NH3 – DH.
1. Влияние концентрации. Если увеличить концентрацию исходных веществ, то равновесие сместится в сторону образования продуктов и, наоборот.
Если уменьшить концентрации исходных веществ N2 и Н2, это приведет к смещению равновесия справа налево, в результате концентрации N2 и Н2 вновь увеличатся за счет разложения аммиака.
2. Влияние давления. При этом учитываются только газообразные участники реакции. При увеличении давления равновесие смещается в сторону системы, состоящей из меньшего числа моль газообразных веществ.
Увеличение давления системы приведет к смещению равновесия слева направо, т.к. в левой части общее число моль газов 4, а в правой 2.
3. Влияние температуры. Зависит от теплового эффекта реакции.
Химические уравнения, в которых указан тепловой эффект реакций называются термохимическими уравнениями. В термохимических уравнениях химических реакций тепловой эффект указывают при помощи величины DH, которая называется изменением энтальпии (теплосодержания) реакции. Энтальпия является мерой энергии, накапливаемой веществом при его образовании.
–DH, теплота выделяется, т.е. реакция – экзотермическая;
+DH, теплота поглощается, т.е. реакция – эндотермическая;
Прямая реакция экзотермическая, т.е. при повышении температуры равновесие будет смещаться справа налево, в сторону эндотермической реакции.
4. Влияние катализатора. Катализаторы одинаково ускоряют как прямую, так и обратную реакцию, и поэтому не смещают химическое равновесие, а только способствуют более быстрому достижению равновесного состояния.
Задание. Газовая системе А + В 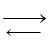 С – DH. Какое влияние на равновесную концентрацию вещества С окажет:
С – DH. Какое влияние на равновесную концентрацию вещества С окажет:
а) увеличение давления. В левой части 2 моль веществ. В правой 1 моль, т.е. равновесие смещается слева направо в сторону образования вещества С, концентрация С увеличивается.(®)
б) увеличение концентрации вещества А. Равновесие смещается слева направо в сторону образования вещества С, концентрация С увеличивается.(®).
в) повышение температуры. Прямая экзо, обратная – эндотермическая. Равновесие сместится справа налево ().
Задание. Как повлияет на равновесие системы увеличение давления?
Fe3O4(тв) + СО(г) 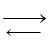 3FeO + CO2(г)
3FeO + CO2(г)
Равновесие в системе не сместится.
Задание. Каким образом надо изменить температуру, давление и концентрацию, чтобы сместить равновесие в сторону прямой реакции?
PCl5(г) 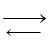 PCl3(г) + Cl2(г) + 92,59 кДж
PCl3(г) + Cl2(г) + 92,59 кДж
а) реакция эндотермическая, температуру надо повысить.
б) давление надо уменьшить
в) либо увеличить концентрацию PCl5, либо уменьшить концентрации PCl3 и Cl2.
Задание.2SO2(г)+О2(г) Û 2SO3(ж). Какое влияние на равновесное состояние окажут:
а) увеличение давления;
При протекании прямой реакции количество газообразных веществ в системе уменьшается (из 2 моль газа SO2 и 1 моль газа О2 образуется жидкость SO3). Повышение давления приведет к смещению равновесия в сторону образования меньшего количества газообразных веществ, т. е. SO3. (®).
б) уменьшение концентрации оксида серы (VI)?
Уменьшение концентрации SO3 (отвод продукта из реакционной системы) вызовет смещение равновесия в сторону образования SO3. (®).
Задание.А + В Û 2С – 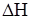
Какое влияние окажут на равновесное состояние:
а) понижение температуры;
Из приведенного термохимического уравнения реакции следует, что прямая реакция является экзотермической (так как 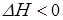 ), следовательно, обратная реакция – эндотермическая, понижение температуры будет способствовать протеканию реакции, которая увеличивает температуру системы, т. е. экзотермической реакции. Поэтому при понижении температуры равновесие сместится в сторону образования вещества С.
), следовательно, обратная реакция – эндотермическая, понижение температуры будет способствовать протеканию реакции, которая увеличивает температуру системы, т. е. экзотермической реакции. Поэтому при понижении температуры равновесие сместится в сторону образования вещества С.
б) катализатор?
Катализатор не приводит к смещению равновесия в системе, так как в одинаковой степени ускоряет прямую и обратную реакции.
