Качественные реакции открытия ионов
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ СВЕРДЛОВСКОЙ ОБЛАСТИ
ГОУ СПО СВЕРДЛОВСКИЙ ОБЛАСТНОЙ ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Качественные реакции открытия ионов
Екатеринбург
Рецензент: преподаватель фармацевтической химии первой категории ГОУ СПО СОФК Журбина Е.В.
Автор:
Антонина Ивановна Серебрякова - преподаватель химии высшей категории, кандидат химических наук.
Учебное пособие: «Качественные реакции открытия ионов»
Содержит перечень качественных реакций на катион и анионы неорганических соединений, необходимых для определения подлинности неорганических лекарственных средств. Реакции приведены по разделам, согласуясь с последовательностью изложения теоретического лекционного материала. Материал раздела структурирован по общему количеству реакций, по отнесению их к окислительно-восстановительным процессам или к кислотно-основным свойствам. Екатеринбург: ГОУ СПО Свердловский областной фармацевтический колледж. 2008 – с.21
Учебное пособие утверждено на заседании цикловой методической комиссии химических дисциплин
Протокол № 1 от 29 августа 2008 года
ГОУ СПО Свердловский областной фармацевтический колледж, 2008
СОДЕРЖАНИЕ
 1. Введение. 4
1. Введение. 4
 2. Элементы 7-ой группы главной подгруппы периодической системы
2. Элементы 7-ой группы главной подгруппы периодической системы
 Д.И.Менделеева. Галогены, галогеноводороды 5
Д.И.Менделеева. Галогены, галогеноводороды 5
3. Элементы 6-ой группы главной подгруппы периодической системы
 Д.И.Менделеева. Халькогены. 7
Д.И.Менделеева. Халькогены. 7
 4. Главная подгруппа V группы (азот и фосфор) 10
4. Главная подгруппа V группы (азот и фосфор) 10
 5. Главная подгруппа IV группы 12
5. Главная подгруппа IV группы 12
 6. Главная подгруппа Ш группы 13
6. Главная подгруппа Ш группы 13

 7. Главная подгруппа П группы14
7. Главная подгруппа П группы14  8. Главная подгруппа IV группы 15
8. Главная подгруппа IV группы 15
 9. Побочная подгруппа I группы. Побочная подгруппа II группы.17
9. Побочная подгруппа I группы. Побочная подгруппа II группы.17
 10.Побочная подгруппа VI группы. Побочная подгруппа VIII группы 19
10.Побочная подгруппа VI группы. Побочная подгруппа VIII группы 19
 11.Литература 21
11.Литература 21
Введение
Качественные реакции необходимы для анализа лекарственных соединений, определения их подлинности. Материал пособия разделен по темам календарно-тематического плана. Реакции, приведенные в пособии, взяты только из программы по неорганической химии и лишь в небольшой степени приведены реакции из курса аналитической химии. Данное пособие представляет собой начальные сведения для изучения качественного анализа в дальнейшем.
Некоторые разделы структурированы по кислотно-основным и окислительно-восстановительным реакциям. Часть реакций повторяется, так как некоторые катионы и анионы можно определять с взаимным использованием. По тексту даются ссылки для просмотра подобных реакций, приведенных ранее.
Материал пособия тесно связан с лекционным курсом по дисциплине и содержит вспомогательный обобщенный учебный материал.
Тема календарно-тематического плана 2.1. р-Элементы
2.1.1. Элементы 7-ой группы главной подгруппы периодической системы Д.И.Менделеева. Галогены, галогеноводороды .
I. Реакции обмена (без изменения степеней окисления химических элементов)
Хлорид-анион ( Cl- ):
a) HCl + AgNO3 à AgCl ↓ + HNO3
Выпадает белый творожистый осадок, растворимый в гидроксиде аммония
AgCl + 2 NH4OH à[Ag(NH3)2]Cl+2H2O
если к раствору добавить конц. HNO3, то снова выпадает белый осадок:
[Ag(NH3)2]Cl+HNO3à AgCl↓+ 2 NH4NO3
Бромид-анион ( Br - ):
a)HBr+ AgNO3 à AgBr↓ + HNO3
Выпадает желтоватый (светло-желтый) осадок, труднорастворимый. в
гидроксиде аммония.
б)Бромид серебра растворяется в растворе тиосульфата натрия:
AgBr + 2 Na2S2O3 à Na3[Ag(S2O3)2] + NaBr
р-р дитиосульфоаргената (1) натрия
Иодид-анион ( I - ):
а)HI + AgNO3 à AgI ↓ + HNO3
Выпадает желтый осадок, нерастворимый в гидроксиде аммония
Вывод:
1. Самые главные реакции на эти ионы – реакции с нитратом серебра. Цвета осадков AgHal изменяют окраску, углубляя ее для элементов, расположенных в таблице Д.И.Менделеева «сверху – вниз» от белого цвета до желтого через желтоватый.
2. Для бромид-аниона ( Br - ) следует запомнить реакцию комплексообразования с тиосульфатом натрия.
II. Реакции окислительно-восстановительные (с изменением степеней окисления химических элементов)
Хлорид-анион ( Cl- ): Не проводят ( реакции не информативны и вредны для здоровья)
Бромид-анион ( Br - ):
Хлорамин + HCl à Cl2
Окислитель Восстановитель
2NaBr + Cl2 à 2NaCl + Br2
выделившийся бром окрашивает слой хлороформа в желто-бурый цвет.


 Cl20 + 2e à2 Cl- 1 окислитель, восстановление
Cl20 + 2e à2 Cl- 1 окислитель, восстановление
2Br- -2e à Br2 1 восстановиетель, окисление
Иодид-анион ( I - ):
a) 2FeCl3 + 2 KI à I2 ↓+ 2 FeCl2 + 2 KCl
Выделившийся иод окрашивает слой хлороформа в фиолетовый цвет
Fe 
 3+ + e à Fe2+ 2 окислитель, восстановление
3+ + e à Fe2+ 2 окислитель, восстановление
2I- -2e à I2 1 восстановиетель, окисление
б)2 NaNO2 +2 NaI + 4 HCl à 4 NaCl + I2 + 2 NO + 2H2O
фиолет.
в х/ф


 NO2- + 2H+ + 1 e à NO + H2O 2 окислитель, восстановление
NO2- + 2H+ + 1 e à NO + H2O 2 окислитель, восстановление
2I- -2e à I2 1 восстановиетель, окисление
Вывод:
1. Самые главные реакции на эти ионы: на бромид-анион - с хлорамином; на иодид-анион – с FeCl3
2. Иногда эти реакции заменяют на реакции с перманганатом калия: при этом раствор перманганата калия обесцвечивается, а хлороформные слои окрашиваются в те же перечисленные выше цвета.
10 KI+ 2KM n O4 + 8 H2SO4 à 2MnSO4 +6K2SO4 + 5I2 +8H 2O
(KBr) (Br2 )


 MnO4- +8H+ + 5 e à Mn2+ + 4 H2O 2 окислитель, восстановление
MnO4- +8H+ + 5 e à Mn2+ + 4 H2O 2 окислитель, восстановление
2I- -2e à I2 5 восстановиетель, окисление
Тема календарно-тематического плана 2.1. р-Элементы
Главная подгруппа IV группы
I. Качественные реакции на карбонат (CO32-) и гидрокарбонат (HCO3-)- анионы:
А) с соляной кислотой (сильными минеральными кислотами):

Na2CO3+2HCl àNaCl +CO2↑ +H2O; NaHCO3 + HClà NaCl + CO2↑ + H2O
выделяются пузырьки углекислого газа, при пропускании которого через известковую воду или баритовую воду происходит ее помутнение, а затем просветление:
Са(ОН)2 + СО2 à CaCO3 ↓ + H2O
белый осадок карбоната кальция
CaCO3 + CO2+H2O à Ca(HCO3)2
гидрокарбонат кальция (раствор)
13
Б) с насыщенным раствором сульфата магния:
 Реакция идет в обычных Реакция идет только при нагревании
Реакция идет в обычных Реакция идет только при нагревании
условиях: t 0
Na2CO3 +MgSO4à MgCO3 + Na2SO4 2NаНСО3 àNa 2СО3 +СО2 + Н2О
Na2CO3 +MgSO4à MgCO3 + Na2SO4
Эти анионы можно отличить друг от друга по реакции среды водного раствора с применением индикатора – фенолфталеина из-за разной силы гидролиза солей:
 |
цвет фиолетовый бесцветный или розовый
(светлее, чем для карбонат аниона в солях)
Тема календарно-тематического плана 2.1. р-Элементы
Главная подгруппа II группы
I. Качественная реакция на катион магния: с гидрофосфатом натрия в среде аммиачного буфера образуется белый мелкокристаллический осадок фосфата магния аммония, растворимый в минеральных кислотах (смотри качественные реакции на фосфат-анион):
NH4Cl
Na2HPO4 + MgSO4 + NH4OH → MgNH4PO4 ↓ + Na2SO4 + H2O
белый
II. Качественные реакции на катион кальция:
1. С оксалатом аммонияобразуется белый кристаллический осадок оксалата кальция, растворимый в минеральных кислотах:
CaCl2 + (NH4)2 C2O4 →CaC2O4 ↓ + 2 NH4Cl
белый
2. Сухим путем: растворимые соли кальция окрашивают пламя горелки в кирпично - красный цвет.
III. Качественные реакции на катион бария:
1. BaCl2 + H2SO4 →BaSO4 ↓ + 2 HCl
белый
С серной кислотой и ее солями образует нерастворимый в воде, щелочах и кислотах мелкокристаллический осадок сульфата бария белого цвета, мелкокристаллический.
2. С хроматом калия образует желтый кристаллический осадок хромата бария, растворимый в соляной и азотной кислотах и нерастворимый в уксусной кислоте.
BaCl2 + K 2CrO4 → BaCrO4 ↓ + 2 KCl
желтый
3. Сухим путем: окрашивает пламя горелки в желто-зеленый цвет.
Тема календарно-тематического плана 2.2 s-элементы
Главная подгруппа I группы
I. Качественные реакции на катион калия:
1. Сухим путем: окрашивает бесцветное пламя горелки в фиолетовый
Цвет.
2.С винной кислотой, в присутствии этанола и ацетата натрия, образуется белый мелкокристаллический осадок гидротартрата калия, растворимый в щелочах (б) и минеральных кислотах (в):
KCl + H2C4H4O6 à KHC4H4O6 ↓ + HCl (а)
гидротартрат калия
KHC4H4O6 ↓ + NaOH à KNaC4H4O6 + H2O (б)
гидротартрат калия, натрия (сегнетова соль)
KHC4H4O6 ↓ + HCl à KCl + H2C4H4O6 (в)
HCl + CH3COONa à CH3COOH + NaCl (г) ацетет натрия
Чтобы реакция (а) не пошла обратно и осадок выпал необходимо связать катионы водорода (Н+) в слабый электролит, например ацетатом натрия в слабую органическую уксусную кислоту (г).
Этиловый спирт используется как осадитель, так как в нем гидротартрат калия растворяется хуже, чем в воде.
3. C гексанитрокобальтатом (Ш) натрия – образуется желтый осадок калия натрия гексанитирокобальтат (Ш):
KCl + Na3[Co(NO2)6] à K2Na[Co(NO2)6] ↓ + 2 NaCl
желтый
II. Качественные реакции на катион натрия:
1. Сухим путем: соли натрия окрашивают пламя горелки в желтый цвет.
2.С цинкуранилацетатом в уксуснокислой среде.Образуетсяжелтый
кристаллический осадокнатрий - цинкуранилацетата:
NaCl +Zn( UO2)3(CH3COO)8 +CH3COOH + 9H2Oà
NaZn(UO2 )3( CH3COO)9 ∙ 9 H2O↓ + HCl

 3.Микрокристаллоскопическая реакция: с пикриновой кислотой: образуются желтые кристаллы пикрата натрия, характерной формы -игольчатые, выходящие из одной точки (из пучка):
3.Микрокристаллоскопическая реакция: с пикриновой кислотой: образуются желтые кристаллы пикрата натрия, характерной формы -игольчатые, выходящие из одной точки (из пучка):

 OH ONa
OH ONa






 O2N NO2 O2N NO2
O2N NO2 O2N NO2
 | 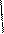 | 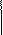 | |||





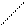
 +NaCl ↓ +HCl
+NaCl ↓ +HCl
 | |||
 |
NO2 NO2
пикриновая кислота пикрат натрия (желтый)↓
4. С гексагидроксостибиатом (+5) калия образуется белыйкристаллический осадок гексагидроксостибиат (+5) натрия. Реакцию проводят в нейтральном или слабо-щелочном растворе (кислоты разлагают реагент, а щелочи растворяют осадок):
NaCl + K[Sb(OH)6] à Na[Sb(OH)6] ↓ + КCl
белый
Тема календарно-тематического плана 2.3. d-Элементы.
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ СВЕРДЛОВСКОЙ ОБЛАСТИ
ГОУ СПО СВЕРДЛОВСКИЙ ОБЛАСТНОЙ ФАРМАЦЕВТИЧЕСКИЙ КОЛЛЕДЖ
НЕОРГАНИЧЕСКАЯ ХИМИЯ
Качественные реакции открытия ионов
Екатеринбург
Рецензент: преподаватель фармацевтической химии первой категории ГОУ СПО СОФК Журбина Е.В.
Автор:
Антонина Ивановна Серебрякова - преподаватель химии высшей категории, кандидат химических наук.
Учебное пособие: «Качественные реакции открытия ионов»
Содержит перечень качественных реакций на катион и анионы неорганических соединений, необходимых для определения подлинности неорганических лекарственных средств. Реакции приведены по разделам, согласуясь с последовательностью изложения теоретического лекционного материала. Материал раздела структурирован по общему количеству реакций, по отнесению их к окислительно-восстановительным процессам или к кислотно-основным свойствам. Екатеринбург: ГОУ СПО Свердловский областной фармацевтический колледж. 2008 – с.21
Учебное пособие утверждено на заседании цикловой методической комиссии химических дисциплин
Протокол № 1 от 29 августа 2008 года
ГОУ СПО Свердловский областной фармацевтический колледж, 2008
СОДЕРЖАНИЕ
 1. Введение. 4
1. Введение. 4
 2. Элементы 7-ой группы главной подгруппы периодической системы
2. Элементы 7-ой группы главной подгруппы периодической системы
 Д.И.Менделеева. Галогены, галогеноводороды 5
Д.И.Менделеева. Галогены, галогеноводороды 5
3. Элементы 6-ой группы главной подгруппы периодической системы
 Д.И.Менделеева. Халькогены. 7
Д.И.Менделеева. Халькогены. 7
 4. Главная подгруппа V группы (азот и фосфор) 10
4. Главная подгруппа V группы (азот и фосфор) 10
 5. Главная подгруппа IV группы 12
5. Главная подгруппа IV группы 12
 6. Главная подгруппа Ш группы 13
6. Главная подгруппа Ш группы 13

 7. Главная подгруппа П группы14
7. Главная подгруппа П группы14  8. Главная подгруппа IV группы 15
8. Главная подгруппа IV группы 15
 9. Побочная подгруппа I группы. Побочная подгруппа II группы.17
9. Побочная подгруппа I группы. Побочная подгруппа II группы.17
 10.Побочная подгруппа VI группы. Побочная подгруппа VIII группы 19
10.Побочная подгруппа VI группы. Побочная подгруппа VIII группы 19
 11.Литература 21
11.Литература 21
Введение
Качественные реакции необходимы для анализа лекарственных соединений, определения их подлинности. Материал пособия разделен по темам календарно-тематического плана. Реакции, приведенные в пособии, взяты только из программы по неорганической химии и лишь в небольшой степени приведены реакции из курса аналитической химии. Данное пособие представляет собой начальные сведения для изучения качественного анализа в дальнейшем.
Некоторые разделы структурированы по кислотно-основным и окислительно-восстановительным реакциям. Часть реакций повторяется, так как некоторые катионы и анионы можно определять с взаимным использованием. По тексту даются ссылки для просмотра подобных реакций, приведенных ранее.
Материал пособия тесно связан с лекционным курсом по дисциплине и содержит вспомогательный обобщенный учебный материал.
Тема календарно-тематического плана 2.1. р-Элементы
2.1.1. Элементы 7-ой группы главной подгруппы периодической системы Д.И.Менделеева. Галогены, галогеноводороды .
I. Реакции обмена (без изменения степеней окисления химических элементов)
Хлорид-анион ( Cl- ):
a) HCl + AgNO3 à AgCl ↓ + HNO3
Выпадает белый творожистый осадок, растворимый в гидроксиде аммония
AgCl + 2 NH4OH à[Ag(NH3)2]Cl+2H2O
если к раствору добавить конц. HNO3, то снова выпадает белый осадок:
[Ag(NH3)2]Cl+HNO3à AgCl↓+ 2 NH4NO3
Бромид-анион ( Br - ):
a)HBr+ AgNO3 à AgBr↓ + HNO3
Выпадает желтоватый (светло-желтый) осадок, труднорастворимый. в
гидроксиде аммония.
б)Бромид серебра растворяется в растворе тиосульфата натрия:
AgBr + 2 Na2S2O3 à Na3[Ag(S2O3)2] + NaBr
р-р дитиосульфоаргената (1) натрия
Иодид-анион ( I - ):
а)HI + AgNO3 à AgI ↓ + HNO3
Выпадает желтый осадок, нерастворимый в гидроксиде аммония
Вывод:
1. Самые главные реакции на эти ионы – реакции с нитратом серебра. Цвета осадков AgHal изменяют окраску, углубляя ее для элементов, расположенных в таблице Д.И.Менделеева «сверху – вниз» от белого цвета до желтого через желтоватый.
2. Для бромид-аниона ( Br - ) следует запомнить реакцию комплексообразования с тиосульфатом натрия.
II. Реакции окислительно-восстановительные (с изменением степеней окисления химических элементов)
Хлорид-анион ( Cl- ): Не проводят ( реакции не информативны и вредны для здоровья)
Бромид-анион ( Br - ):
Хлорамин + HCl à Cl2
Окислитель Восстановитель
2NaBr + Cl2 à 2NaCl + Br2
выделившийся бром окрашивает слой хлороформа в желто-бурый цвет.


 Cl20 + 2e à2 Cl- 1 окислитель, восстановление
Cl20 + 2e à2 Cl- 1 окислитель, восстановление
2Br- -2e à Br2 1 восстановиетель, окисление
Иодид-анион ( I - ):
a) 2FeCl3 + 2 KI à I2 ↓+ 2 FeCl2 + 2 KCl
Выделившийся иод окрашивает слой хлороформа в фиолетовый цвет
Fe 
 3+ + e à Fe2+ 2 окислитель, восстановление
3+ + e à Fe2+ 2 окислитель, восстановление
2I- -2e à I2 1 восстановиетель, окисление
б)2 NaNO2 +2 NaI + 4 HCl à 4 NaCl + I2 + 2 NO + 2H2O
фиолет.
в х/ф


 NO2- + 2H+ + 1 e à NO + H2O 2 окислитель, восстановление
NO2- + 2H+ + 1 e à NO + H2O 2 окислитель, восстановление
2I- -2e à I2 1 восстановиетель, окисление
Вывод:
1. Самые главные реакции на эти ионы: на бромид-анион - с хлорамином; на иодид-анион – с FeCl3
2. Иногда эти реакции заменяют на реакции с перманганатом калия: при этом раствор перманганата калия обесцвечивается, а хлороформные слои окрашиваются в те же перечисленные выше цвета.
10 KI+ 2KM n O4 + 8 H2SO4 à 2MnSO4 +6K2SO4 + 5I2 +8H 2O
(KBr) (Br2 )


 MnO4- +8H+ + 5 e à Mn2+ + 4 H2O 2 окислитель, восстановление
MnO4- +8H+ + 5 e à Mn2+ + 4 H2O 2 окислитель, восстановление
2I- -2e à I2 5 восстановиетель, окисление
Тема календарно-тематического плана 2.1. р-Элементы
