Поверхностные явления. адсорбция
1. Природа поверхностной энергии (сравнить состояние молекулы внутри жидкости и на её поверхности), направление результирующей силы Р. Поверхностное натяжение, физический смысл поверхностного натяжения, энергетическое и силовое выражение поверхностного натяжения. Влияние температуры на поверхностное натяжение. Состояние системы при критической температуре.
2. Зависимость поверхностного натяжения от природы и концентрации растворённого вещества. Деление веществ на: ПАВ (схема строения их молекул), ПИВ и ПНВ. Ориентация молекул ПАВ в поверхностном слое раствора. Правило Дюкло-Траубе.
3. Адсорбция, основные термины: адсорбент, адсорбат, адсорбтив, десорбция. Объясните, чем отличается химическая адсорбция от физической по природе действующих сил между адсорбентом и адсорбатом.
4. Адсорбция на поверхности растворов. Уравнение Гиббса ( Г = - 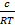 ∙
∙ 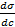 ), изотерма Гиббса, её анализ.
), изотерма Гиббса, её анализ.
5. Адсорбция на твёрдых поверхностях, её количественная характеристика – удельная адсорбция ( Г =  моль/г) . Факторы влияющие на неё.
моль/г) . Факторы влияющие на неё.
6. Теория мономолекулярной адсорбции Ленгмюра, уравнение Ленгмюра (Г = Г∞  ), изотерма адсорбции Ленгмюра, её анализ.
), изотерма адсорбции Ленгмюра, её анализ.
7. Адсорбция на границе твёрдое тело – жидкость. Её особенность, факторы, влияющие на неё.
8. Адсорбция растворённого в жидкости вещества на твёрдом адсорбенте: молекулярная адсорбция и ионная. Факторы влияющие на этот вид адсорбции (химическая природа адсорбента; химическая природа ионов). Ряды Гофмейстера. Влияние заряда иона на адсорбцию. Правило Панетта – Фаянса.
9. Понятие о ионообменной адсорбции. Иониты (катиониты, анирониты и амфолиты). Их использование.
10. Хроматография, её виды. Понятие о подвижной и неподвижной фазе. Применение методов хроматографии в медициине.
КОЛЛОИДНЫЕ СИСТЕМЫ
1. Дисперсные системы (дисперсная фаза и дисперсная среда). Как классифицируют дисперсные системы по размеру частиц дисперсной фазы? Взвеси, коллоидные системы и истинные растворы, их общая характеристика.
2. Молекулярно-кинетические свойства Оптические свойства Эффект Тиндаля.
3. Получение коллоидных систем (диспергирование веществ и конденсация веществ).
4. Очистка коллоидных систем (диализ, электродиализ, ультрафильтрация)
5. Строение мицеллы. Изобразите схемой строение мицеллы, поясните схему. Изоэлектрическое состояние мицеллы.
6. Электрокинетический потенциал. Факторы определяющие его величину. Электрокинетические явления в живых организмах.
7. Строение мицеллы, двойной электрический слой, современные представления о его строении.
8. Виды устойчивости коллоидных систем: седиментационная и агрегативная. Объясните физический смысл этих видов устойчивости коллоидных систем.
9. Коагуляция коллоидных систем, каковы причины этого процесса? Две стадии коагуляции: скрытая и явная коагуляция.
10. Коагуляция коллоидных систем электролитами (работы Б.В. Дерягина и Л.Д. Ландау). Порог коагуляции. Правило Шульце – Гарди.
11. Какое явление в коллоидной химии называют защитой от коагуляции коллоидных частиц? Чем оно обусловлено? Роль «защиты» в организме человека (удерживание карбонатов и фосфатов в коллоидном состоянии). Количественная оценка защитного действия ВМС (золотое число).
12. Сенсибилизация -явление снижения порога коагуляции золя при добавлении в него ВМС. Какие по строению молекулы вызывают это явление, как называют этот вид коагуляции? Что такое флокулы?
13. Коагуляция смесями электрлитов: аддитивность, антагонизм, синергизм.
14. Мембранное равновесие Доннана, его физический смысл. Понятие о мембранном равновесии.
