Изомерия органических соединений
Структурная изомерия
Структурными изомерами называют соединения, имеющие одинаковый состав, но различающиеся строением углерод-углеродного скелета. Например:
н-бутан
изо-бутан
Для циклических:
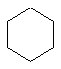 циклогексан,
циклогексан, 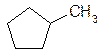 метилциклопентан,
метилциклопентан,
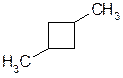 1,3-диметилциклобутан,
1,3-диметилциклобутан, 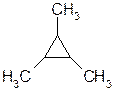 триметилциклопропан
триметилциклопропан
Изомерия положения
Изомерами положения могут быть замещенные алканы, циклоалканы и непредельные соединения:
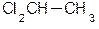 1,1-дихлорэтан,
1,1-дихлорэтан, 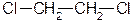 1,2-дихлорэтан
1,2-дихлорэтан
Циклические соединения:
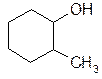 1-метилциклогесанол,
1-метилциклогесанол,  3-метилциклогексанол
3-метилциклогексанол
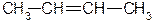 бутен-2,
бутен-2, 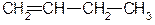 бутен-1.
бутен-1.
5.3 Геометрическая изомерия
(зеркальная, цис- транс- изомерия)
Например, для бутена-2:
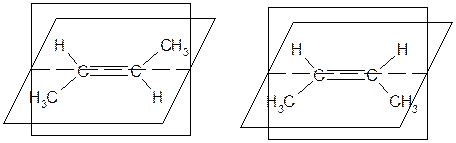
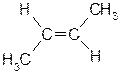 транс-бутен-2,
транс-бутен-2, 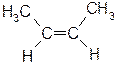 цис-бутен-2
цис-бутен-2
Изомеры этилендикарбоновой кислоты:
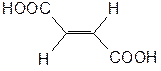 транс – бутендиовая-1,4 кислота (фумаровая кислота),
транс – бутендиовая-1,4 кислота (фумаровая кислота),
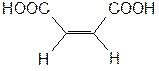 цис – бутендиовая-1,4 кмслота (малеиновая кислота)
цис – бутендиовая-1,4 кмслота (малеиновая кислота)
Цис- и транс- изомерия используется , как правило, в тех случаях, когда при двойной связи имеются два атома водорода и два заместителя, причем у каждого атома углерода при двойной связи должны быть различные заместители. Так, метиленмалоновая кислота:
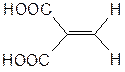 не является объектом рассмотрения геометрической (цис-транс) изомерии. Геометрические изомеры существуют в дизамещенных циклоалканах. Для хлорциклопентанола:
не является объектом рассмотрения геометрической (цис-транс) изомерии. Геометрические изомеры существуют в дизамещенных циклоалканах. Для хлорциклопентанола:
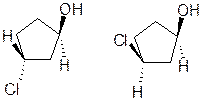
транс (OH, Cl) цис (OH, Cl)
Цис-транс изомерия является частным случаем Z, E и ε, τ изомерии. Они отличаются только системой определения старшинства заместителей. Формально - Z (цис), E (транс); ε (цис), τ (транс). В общем случае при определенном изменении старшинства заместителей, для алкена заданной структуры существует ряд изомеров:
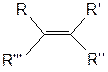
При R>R’>R’’>R’’’ соединение имеет ε (Z) конфигурацию двойной связи.
При R>R’’’>R’’>R’ соединение является t (Е)-изомером.
Система старшинства ε,τ-изомерии
Основана В.М. Потаповым и сотр. в 60-х гг. в МГУ. Суть системы - использованиеноменклатуры ИЮПАК. Например:
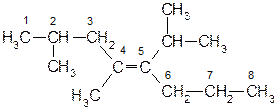
Главная цепь содержит 8 атомов углерода. Она расположена по разным сторонам плоскости p-связи, поэтому данное соединение является τ изомером (понятие цис- транс- изомерии здесь неприемлемо!)
Система старшинства Z, E-изомерии
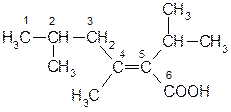
Система старшинства по Z, E типу основана на периодической системе элементов Д.И. Менделеева. (по порядковому номеру элементов)
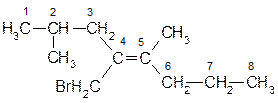
4-бромметил-2,5-диметилоктен-4 (Z)
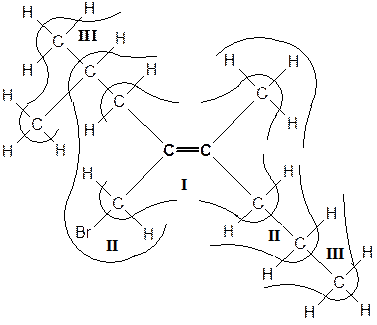
I слой. Все заместители (атомы углерода) равны между собой
II слой. CH2Br>x или y>CH3 (å порядковых номеров CH2Br равна: 6+2+35=43. Для CH3 – 6+3=9)
III слой i-Bu>н-Bu (т.к. для i-Bu, по третьему слою: 6+6+1=13, для н-Bu: 6+1+1=8). Где: i-Bu - изобутил, н-Bu - н-бутил.
Таким образом, уменьшение старшинства заместителей имеет вид: CH2Br>i-Bu>н-Bu>CH3. Следовательно, рассматриваемое соединение является Z - изомером.
Оптическая изомерия
Проявляется в тех случаях, когда изомеры одного и того же соединения, в свзи с различным расположением заместителей у определенного центра, не совместимы в пространстве. Для производных алифатического ряда изомерия связана со стереохимическими особенностями sp3 гибридного атома углерода.
Еще Ле-Бель в конце 18 века предположил тетраэдрическую структуру атома углерода. В том случае, если атом углерода соединен с четырьмя различными заместителями, появляется возможность существования 2-х изомеров, являющихся зеркальным отражением друг друга.
Атом углерода, имеющий все различные заместители называют асимметрическимили хиральным центром («хирос» - рука).
Рассмотрим на примере перспективных формул:
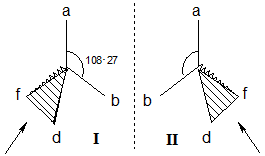
Стереоизомеры I и II не совместимы в пространстве, являются антиподами или оптическими изомерами (энантиомерами, стереомерами).
Проекционные формулы Фишера
Рассмотрим перспективные формулы в другой плоскости.
Расположим асимметрический центр (атом углерода) в плоскости листа; заместители a и b за плоскостью листа (от наблюдателя); заместители f и d над плоскостью листа (ближе к наблюдателю) – в соответствии со стрелками, указывающими направление взгляда наблюдателя. Получим взаимно перпендикулярное направление связей с хиральным центром. Такое построение изомеров называют проекционными формулами Фишера.
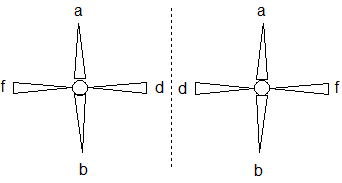
Таким образом, в проекционных формулах Фишера заместители, расположенные по горизонтали, направлены к наблюдателю, по вертикали - за плоскость листа.
При построении проекционных формул наиболее объемные заместители располагают по вертикали. Если заместителями являются атомы или малые группы, не имеющие отношения к главной цепи, то их располагают по горизонтали. Для 2-бромбутана
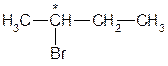
существуют два антипода:
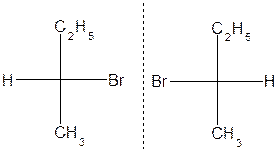
Энантиомеры, антиподы, стереомеры практически неразличимы по свойствам (t кипения, t плавления и т.д.), а также имеют сходные термодинамические константы. В то же время у них есть различия:
4) - твердые антиподы кристаллизуются с образованием зеркально похожих друг на друга кристаллов, но не совместимых в пространстве.
5) - антиподы вращают плоскость поляризованного света на одинаковый угол, но в различные стороны. Если угол вращения света положителен (по часовой стрелке), то антипод называют правовращающим, если отрицателен (против часовой стрелки), то - левовращающим.
Угол оптического вращения плоскополяризованного света обозначают [αD]. Если [αD]= -31.2°, то исследовался левовращающий антипод.
Устройство поляриметра
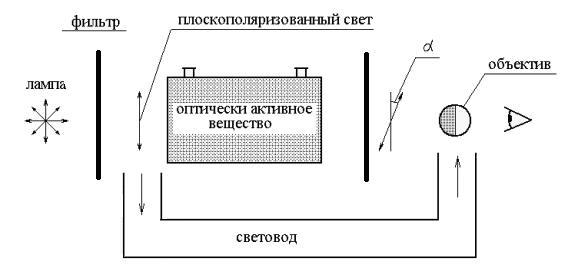
Вещества, способные вращать плоскость поляризованного света, называются оптически активными или оптически деятельными.
Смесь двух энантиомеров в соотношении 1:1 не вращает плоскость поляризованного света и называется рацемической смесью, рацематом.
Если один антипод преобладает в смеси над другим, то говорят об его оптической чистоте (ee). Она вычисляется по разности содержания энантиомеров в смеси.
I - 70 %
II - 30 %, ee=70 – 30 = 40 (%)
Вторичные и третичные амины также могут обладать оптической активностью. Четвертым заместителем является неподеленная пара электронов на атоме азота.
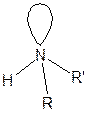
5.4.1 Диастереомеры
Диастереометрия - явление более существенно сказывающееся на свойствах веществ и наблюдается в тех случаях, когда в соединении имеется два или более асимметрических центра. Например:
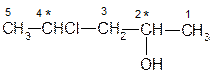 4-хлорпентанол-2
4-хлорпентанол-2
Изобразим все возможные для соединения антиподы (I-IV):

Оптические изомеры (стереоизомеры) одного и того же соединения, не являющиеся антиподами, называются диастереомерами. То есть пары изомеров I и III, I и IV, II и III, II и IV являются диастереомерными парами. Количество изомеров рассчитывают по формуле: q = 2n, где
q - общее количество стереоизомеров,
n - количество асимметрических центров (C*).
Например, глюкоза имеет 4 хиральных центра, тогда q = 24 = 16 (D-глюкоза – 8 изомеров, L- глюкоза – 8 изомеров).
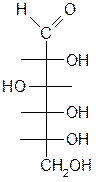
D-глюкоза
В природе встречаются случаи, когда асимметрические атомы в соединении имеют одинаковое окружение. Это приводит к тому, что половина антиподов не является оптически деятельными.
Пример:
винная кислота
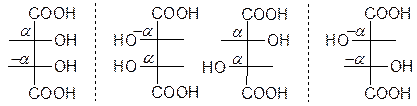
åα=0 åα=0 åα=2α åα=-2α
мезоформа
Мезоформа оптически неактивная форма, возникающая вследствие внутренней симметрии в оптически деятельном веществе.
В отличие от антиподов, диастереомеры различаются по температуре кипения, плотности (d420), показателю преломления (n420) и т.д.
Номенклатура стереоизомеров
Особенности строения стереоизомеров (конфигурацию асимметрического центра) в начале пытались изобразить через угол вращения плоскости поляризованного света [αD], но оказалось, что эта величина непостоянна и на направление вращения влияют:
природа растворителя,
концентрация оптически активного вещества в растворителе,
температура растворителя,
длина волны плоскополяризованного света.
Таким образом, [αD] лишь косвенно характеризует строение стереоизомеров. Ученые пытались определить конфигурацию стереоизомеров, сводя их к эталонным веществам (относительная система номенклатуры). Для каждого класса соединений существует свой эталон. Так, для углеводородов эталоном выбран глицериновый альдегид. По предложению академика Розанова правовращающий антипод глицеринового альдегида отнесли к D-глицериновому альдегиду, левовращающий - к L-глицериновому альдегиду.

Розанов «угадал» строение правовращающего глицеринового альдегида, отнеся его к D-ряду. Как следует из проекционных формул, D-форме соответствует правостороннее расположение гидроксильной группы (выделено пуктиром)
Для отнесения неизвестного изомера углевода к какой-либо конфигурации (D или L) сравнивают нижнюю его часть с соответствующим изомером глицеринового альдегида.
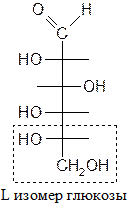
Для a-оксикислот в качестве эталона выбрана молочная кислота
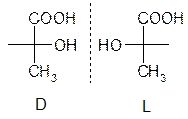
D, L номенклатура также является относительной номенклатурой стереоизомеров (как и (+), (-)).
В 1951 г. впервые две группы ученых в Англии и России предложили номенклатуру, определяющую абсолютную конфигурацию стереоизомеров.
Номенклатура Кана, Ингольда, Прелога (КИП)
Стереоизомер располагают в тетраэдре таким образом, чтобы младший заместитель находился в наиболее удаленной от наблюдателя вершине.
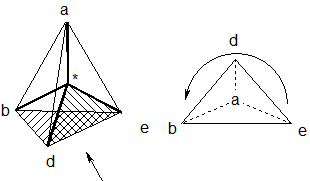
Для оставшихся трех заместителей (d, b, e) рассматривают изменение (в порядке уменьшения) их старшинства. При уменьшении старшинства по часовой стрелке, конфигурация асимметрического центра обозначается буквой R, против - S. Если в приведенном примере старшинство убывает в ряду e>d>b>a, то изомер будет иметь S - конфигурацию асимметрического центра.
При использовании проекционных формул Фишера для отнесения конфигурации по RS-номенклатуре меньший заместитель располагают внизу, а старший - слева от асимметрического центра.
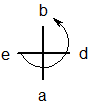
Старшинство заместителей определяют по предложенной авторами системе, в основе которой лежит периодическая таблица Менделеева (по порядковому номеру элемента).
В том случае, если элементы связаны двойной или тройной связью, то соответствующий атомный номер удваивается или утраивается.
Примечание:
В геометрической изомерии эта система используется для определения Z, E изомеров.
Пример 1:
Определим абсолютную конфигурацию D-глицеринового альдегида по номенклатуре КИП.
Примечание: заместители, расположенные в проекциях Фишера по горизонтали, направлены к наблюдателю, по вертикали - от наблюдателя.
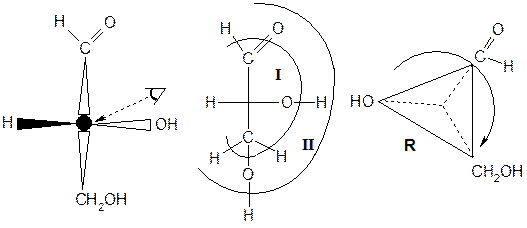
I слой: OH>X и Y>H. Где X=COH, Y=CH2OH.
II слой: X=8´2+1=17; Y=6+1+1=8. Таким образом, COH>CH2OH.
Направление уменьшения старшинства заместителей – по часовой стрелке, поэтому, D-глицериновый альдегид имеет R-конфигурацию асимметрического центра.
Пример 2:
Определим конфигурацию хирального центра для (+)-D-яблочной кислоты (двухосновная кислота)
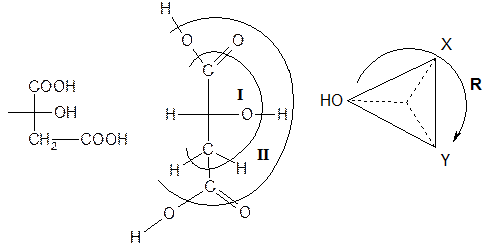
I слой: OH>X и Y>H. Где X=COOH, Y=CH2COOH.
II слой: X=8´2+8=24; Y=6+1+1=8. Таким образом, OH>X>Y>H.
Следовательно, асимметрический центр (+)-D-яблочной кислоты имеет R-конфигурацию.
Недостатки номенклатуры КИП:
Если автор ошибся в названии соединения по номенклатуре ИЮПАК, то читатель определяет конфигурацию хирального центра антипода.
При замене группы R, например, на Br конфигурация асимметрического центра не меняется, а абсолютная конфигурация (по номенклатуре КИП) измениться, так как Br и R имеют разные порядковые номера.
Значительные расхождения с номенклатурой ИЮПАК.
5.5 Номенклатура стереоизомеров Потапова В.М.,
Терентьева А.П. и сотрудников
Молекулу располагают таким образом, чтобы младший заместитель при асимметрическом центре был удален от наблюдателя, тогда при уменьшении старшинства остальных заместителей по часовой стрелке, конфигурацию асимметрического центра обозначают σ, против часовой стрелки - ρ (σ,ρ-номенклатура).
Старшинство заместителей определяют с использованием номенклатуры ИЮПАК!
Начало цепи младше, чем конец цепи (т.е. чем старше номер, тем старше заместитель).
В проекционных формулах Фишера углеродную цепь располагают таким образом, чтобы нумерация цепи: шла сверху вниз.
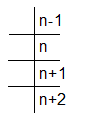
Для того, чтобы определить конфигурацию асимметрического центра, достаточно при обходе цепи сверху фиксировать положение заместителя. Если заместитель находится справа от основной цепи, то конфигурацию обозначают через ρ, если слева - то через σ. Например, определим конфигурацию 2-бром-2-метилбутановой кислоты следующего строения:
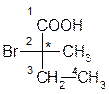
Обходим цепь слева: 2-(σ)-бром-2-метилбутановая кислота; справа - 2-бром-2-(ρ)-метилбутановая кислота. Оба названия правильны. С другой стороны, рассмотрим хиральный центр обычным способом:
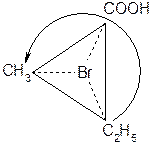
Углеводородные заместители превалируют над другими, кроме функциональных групп, то есть Br – младший заместитель. Таким образом определяем конфигурацию соединения как 2-бром-2-(ρ)-метилбутановая кислота.
При наличии в молекуле двух асимметрических центров пользуются правилом старшинства по порядковым номерам. Например:
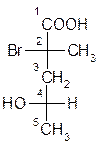
2-(σ)-бром-4-(σ)-гидрокси-2-метилпентановая кислота
Если цепь состоит из одного асимметрического атома углерода, заместители располагают таким образом, чтобы самый старший заместитель находился внизу, а атом водорода, если он есть, располагают слева или справа.
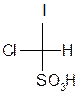
(σ)-хлориодметансульфокислота
Если цепь состоит из двух атомов углерода, то за начало цепи выбирается асимметрический центр.
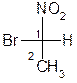
1-(σ)-бром-1-нитроэтан
Преимущества номенклатуры Потапова В.М. и др.:
1. Используется та же система определения старшинства, как и в номенклатуре ИЮПАК.
2. Если автор ошибся в нумерации цепи, то читатель по данному названию сможет определить формулу вещества и конфигурацию асимметрических центров.
Определим конфигурацию асимметрического центра D-глицеринового альдегида:
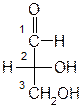
2(ρ),3-диоксипропаналь
При замене одного заместителя на другой конфигурация асимметрического центра не меняется. Напрмер:
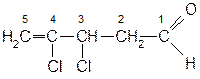
3,4-дихлорпентен-4-аль
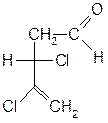
3(ρ),4-дихлорпентен-4-аль
По номенклатуре КИП:
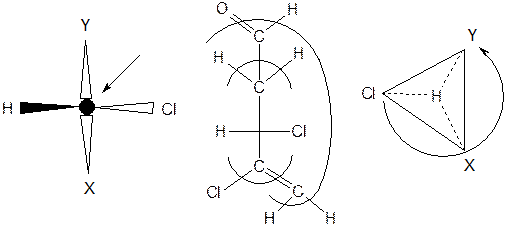
По горизонтали - над плоскостью, по вертикали - за плоскостью
I слой: Cl>X и Y>H. Где X: CCl=CH2, Y: CH2CHO.
II слой: X>Y. Третий атом углерода имеет S-конфигурацию: 3(S)-3,4-дихлорпентен-4-аль.
