Окислительно-восстановительные процессы
1. Как называется скачок потенциала, возникающий на границе раздела фаз раствор – раствор?
1) потенциал покоя
2) мембранный потенциал
3) электродный потенциал
4) диффузионный потенциал
5) электродвижущая сила
2. Какая система обладает самыми высокими окислительными свойствами?
1) φ (Au3+/Au+) = 1,40 B
2) φ (Fe3+/Fe2+) = 0,77 B
3) φ (Co3+/Co2+) = 1,81 B
4) φ (Mn3+/Mn2+) = 1,51 B
5) φ (Pb4+/Pb2+) = 1,70 B
3. Как рассчитывают электродвижущую силу гальванического элемента?
1) Е = φ1 + φ2
2) Е = φ1 – φ2
3) Е = φ1 × φ2
4) Е = φ1 / φ2
5) Е = φ2 / φ1
4. Какой электрод является электродом первого рода?
1) Ag, AgCl│KCl
2) Ag│AgNO3
3) Hg, Hg2Cl2│KCl
4) Pt│Sn4+, Sn2+
5) Pt│Fe2+, Fe3+
5. Какой электрод является электродом второго рода?
1) Ag, AgCl│KCl
2) Ag│AgNO3
3) Pt│Sn4+, Sn2+
4) Cu│CuSO4
5) Pt│Fe2+, Fe3+
6. Какой из нижеперечисленных электродов является окислительно-восстановительным?
1) Ag, AgCl│KCl
2) Ag│AgNO3
3) Hg, Hg2Cl2│KCl
4) Cu│CuSO4
5) Pt│Fe3+, Fe2+
7. Система (+) Ag│AgNO3(0,1н)║AgNO3(0.01н)│Ag(-)
1) электрод определения
2) электрод сравнения
3) электрод второго рода
4) концентрационный элемент
5) окислительно-восстановительный элемент
8. Чему равен потенциал водородного электрода (В) при [H +]=10-2 ?
1) -0,059 В
2) +0,059 В
3) -0,118 В
4) +0,118 В
5) 0 В
9. Чему равен потенциал водородного электрода (В) при рН=10?
1) 0,59
2) -0,59
3) 0,30
4) -0,30
5) 0
10. Какие электроды используют при потенциометрическом определении рН биологических жидкостей?
1) цинковый-медный
2) хлорсеребряный-стеклянный
3) медный-водородный
4) цинково-водородный
5) каломельный-хлорсеребряный
11. Какой электрод используется как электрод определения при установлении рН желудочного сока потенциометрическим титрованием?
1) стеклянный
2) цинковый
3) медный
4) хлорсеребряный
5) каломельный
12. Какая реакция протекает в гальваническом элементе ( -) Fe / FeSО4 // CuSО4 / Сu (+ ), (φ0 Fe / Fe2+ = - 0,44 В ; φ0 Сu / Сu2+ = +0,34 В)?
1) Fe0 + Cu2+ ® Fe2+ + Cu0
2) Cu0 + Fe2+ ® Fe0 + Cu2+
3) Fe2+ + 2e ®Fe0
4) Cu0 - 2e ® Cu2+
5) реакция не идет
13. Какая реакция протекает в гальваническом элементе (-) Zn/ZnS04 //CuS04 /Сu (+) (φ0Zn/Zn2+ = -0,76 B ; φ0Cu/Cu2+ = +0,34 B)?
1) Cu0 + Zn2+ ® Zn0 + Cu2+
2) Сu2+ + Zn0 ® Сu0 + Zn2+
3) Сu0 - 2е ® Сu2+;
4) Zn2+ + 2e ® Zn0
5) реакция не идет
14. Какая реакция протекает в гальваническом элементе (-)Zn /ZnS04 // NiS04 /Ni (+) (φ0 Zn/Zn2+ = -0,76 B ; φ0 Ni/Ni2+ = -0,25 B)?
1) Ni0 + Zn2+ ® Zn0 + Ni2+
2) Ni2+ + Zn0 ® Ni0 + Zn2+
3) Ni0 - 2е ® Ni2+
4) Zn2+ + 2e ® Zn0
5) реакция не идет
15. Как называется скачок потенциала, возникающий на границе раздела фаз металл - раствор его соли?
1) потенциал стандартного водородного электрода
2) мембранный потенциал
3) электродный потенциал
4) диффузионный потенциал
5) электродвижущую силу
16. Как называется скачок потенциала, возникающий на границе раздела фаз раствор – раствор?
1) потенциал стандартного водородного электрода
2) мембранный потенциал
3) электродный потенциал
4) диффузионный потенциал
5) электродвижущую силу
17. Как называется скачок потенциала, возникающий на границе раздела фаз мембрана - раствор вследствие избирательной проницаемости мембраны?
1) потенциал стандартного водородного электрода
2) мембранный потенциал
3) электродный потенциал
4) диффузионный потенциал
5) электродвижущую силу
18. Что такое электродвижущая сила гальванического элемента?
1) отношение потенциалов электродов, составляющих гальванический элемент
2) произведение потенциалов электродов, составляющих гальванический элемент
3) потенциал положительно заряженного электрода
4) сумму потенциалов электродов, составляющих гальванический элемент
5) разность потенциалов электродов, составляющих гальванический элемент
19. Как называются электроды, представляющие собой металлическую пластинку, опущенную в раствор соли этого металла?
1) электродами сравнения
2) электродами определения
3) электродами I рода
4) электродами II рода
5) мембранными электродами
20. Как называется электрод, представляющий собой металл, погруженный в насыщенный раствор трудно растворимой соли этого металла и хорошо растворимой соли, имеющий общий анион с анионом трудно растворимой соли?
1) электродом сравнения
2) электродом определения
3) электродом I рода
4) II рода
5) мембранным электродом
21. Два электрода, состоящие из одного и того же металла, опущенные в раствор соли этого же металла с разными активностями, называются:
1) окислительно-восстановительным элементом
2) полуэлементом
3) элементом Якоби-Даниэля
4) концентрационным элементом
5) элементом Вестона
22. Как называется гальваническая цепь (-) Zn/ZnS04 // CuS04 / Сu ( + ) ?
1) элемент Вольта
2) элемент Вестона
3) элемент Якоби-Даниэля
4) стандартный электрод
5) электрод сравнения
23. У какой системы наиболее высокие окислительные свойства?
1) φ (Fe3+/Fe2+) = 0,77 B
2) φ (2Hg2+/Нg22+) = 0,92 В
3) φ (Sn4+/Sn2+) = 0,15 B
4) φ (Ti4+/Ti3+) = 0,06 B
5) φ (Сu2+/Сu+) = 0,16 В
Поверхностные явления
1. По какой формуле рассчитывают величину поверхностной активности?
1) 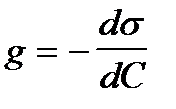 ++++
++++
2) 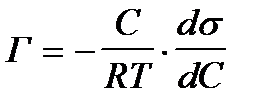
3) 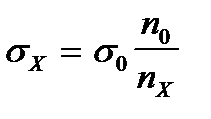
4) Г = Г¥ . C /(K + C)
5) 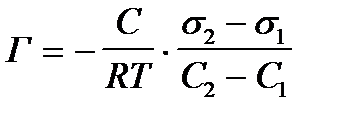
2. По какой формуле рассчитывают величину адсорбции растворенного вещества на подвижной границе раздела фаз?
1) 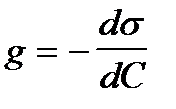
2) 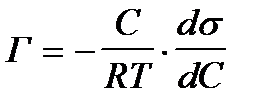 +++++++++
+++++++++
3) 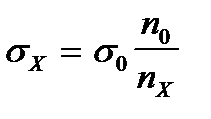
4) 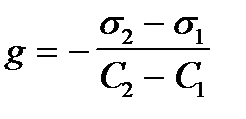
5) Г = Г¥ . C /(K + C)
3. Как можно охарактеризовать состояние адсорбционного равновесия?
1) происходит только процесс адсорбции
2) происходит только процесс десорбции
3) скорость адсорбции больше, чем скорость десорбции
4) скорость адсорбции меньше, чем скорость десорбции
5) скорость адсорбции равна скорости десорбции
4. Как называется состояние системы, при котором скорость адсорбции равна скорости десорбции?
1) положительная адсорбция
2) отрицательная адсорбция
3) удельная адсорбция
4) капиллярная конденсация
5) адсорбционное равновесие
5. Что может быть использовано для регенерации катионитов?
1) нагревание
2) замораживание
3) обработка раствором щелочи
4) обработка раствором хлорида натрия (Na)
5) обработка раствором сильной кислоты (H)
6. Какой метод может быть использован с целью предотвращения свертываемости крови при ее консервировании для удаления ионов Са2+?
1) диализ
2) электрофорез
3) хроматография
4) молекулярная адсорбция
5) ионообменная адсорбция
7. Какое вещество обладает поверхностной активностью?
1) С12Н22О11
2) HCl
3) Н2SO4
4) NH2CH2COOH
5) C6H13COOH
8.У какого иона способность к адсорбции самая высокая?
1) Na+
2) Ca2+
3) Al3+
4) Th4+
5) K+
9. Какое вещество будет адсорбироваться в виде молекулы на поверхности активированного угля?
1) CH3COONa
2) CH3COOH
3) KOH
4) CaCl2
5) H2SO4
10. Какое уравнение описывает адсорбцию на границе раздела твердое тело – жидкость?
1) 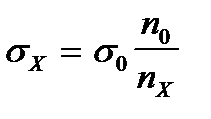
2) Г = Г¥ . C /(K + C)
3) 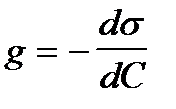
4) 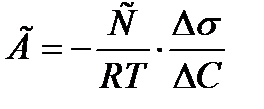
5) sх = nx / n(H2O)
11. Как изменяется поверхностная активность водных растворов веществ одного гомологического ряда при удлинении углеводородной цепи на одну –СН2- группу согласно правилу Дюкло-Траубе?
Увеличивается в 3-3,5 раза
2) увеличивается в 2-4 раза
3) не изменяется
4) уменьшается в 2-4 раза
5) уменьшается в 3-3,5 раза
12. Какая группа обладает гидрофильными свойствами?
1) – C2H5
2) – C6H5
COOH
4) – CH2–C6H5
5) –С4Н9
13. Какая группа обладает гидрофобными свойствами?
1) – OH
2) – C5H11
3) – NH2
4) –SO3H
5) – COOH
14. Какой ион согласно правилу Панета-Фаянса адсорбируется на поверхности бромида серебра?
1) NO3-
2) SO42-
3) Ca2+
4) Al3+
5) Br-
15. Какое вещество является поверхностно-активным?
1) серная кислота
2) карбонат натрия
Изоамиловый спирт
4) пероксид водорода
5) сахароза
16. Изотерма поверхностного натяжения показывает зависимость величины поверхностного натяжения σ
1) от полярности растворенного вещества
2) от полярности растворителя
3) от температуры
