Электрическая проводимость. Абсолютная скорость и подвижность ионов
Способность растворов электролитов проводить электрический ток зависит от природы электролита и растворителя, концентрации и температуры. В растворе электролита сольватированные ионы находятся в беспорядочном тепловом движении. При наложении электрического поля возникает упорядоченное движение ионов к противоположно заряженным электродам - миграция (перенос). Движение ионов происходит под действием силы, сообщающей им ускорение, однако одновременно с возрастанием скорости их движения увеличивается сопротивление среды. В результате скорость движения ионов через малый промежуток времени становится постоянной.
Сравнение скоростей движения различных видов ионов производится при одинаковом градиенте потенциала поля, равном 1 В/м. Скорость движения ионов в этих условиях называют абсолютной скоростью ионов (электрической подвижностью или абсолютной подвижностью) (u) (она измеряется в 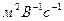 )
)
Движение гидратированного иона может быть уподоблено движению микроскопического шарика в вязкой среде. Данный факт позволяет оценить абсолютную скорость ионов i-го вида формулой Стокса:
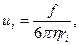 (32.41)
(32.41)
где 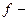 сила, действующая на ион;
сила, действующая на ион; 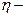 коэффициент вязкости среды;
коэффициент вязкости среды; 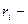 эффективный радиус частицы, который зависит от размера иона и его гидратации.
эффективный радиус частицы, который зависит от размера иона и его гидратации.
Из уравнения (32.41) следует, что чем больше эффективный радиус иона, тем меньше скорость его движения. Например, размеры ионов щелочных металлов увеличиваются в ряду
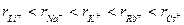 ,
,
в то время как способность к гидратации уменьшается в этой же последовательности (ион 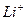 гидратирован сильнее остальных ионов). В результате эффективные радиусы уменьшаются, а абсолютные скорости при переходе от
гидратирован сильнее остальных ионов). В результате эффективные радиусы уменьшаются, а абсолютные скорости при переходе от 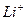 к
к 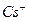 возрастают:
возрастают:
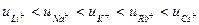 .
.
Наряду с абсолютной скоростью ионов часто пользуются понятием подвижности ионов. Произведение абсолютной скорости ионов на постоянную Фарадея F 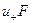
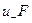 называется подвижностью иона (молярной электрической проводимостью). Постоянная Фарадея равно
называется подвижностью иона (молярной электрической проводимостью). Постоянная Фарадея равно 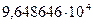 Кл/моль.
Кл/моль.
Это заряд одного моля электронов 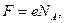 т. е. то количество электричества при электролизе, которое необходимо затратить для изменения степени окисления 1 моль вещества на единицу. Единица измерения подвижности ионов
т. е. то количество электричества при электролизе, которое необходимо затратить для изменения степени окисления 1 моль вещества на единицу. Единица измерения подвижности ионов 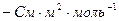 , где Cм – (сименс[5]) единица измерения электрической проводимости, обратная единице измерения сопротивления (Ом) т.е.
, где Cм – (сименс[5]) единица измерения электрической проводимости, обратная единице измерения сопротивления (Ом) т.е. 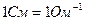 .
.
Подвижность многозарядных ионов относят к единице заряда, т. е. говорят, например, о подвижности катионов 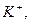
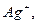 но
но 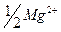 и анионов
и анионов 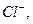
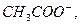 но
но 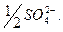
Числа переноса
Каждый вид ионов переносит определенное количество электричества, зависящее от заряда и концентрации ионов, а также скорости их движения в электрическом поле. Отношение количества электричества 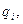 перенесенного ионами
перенесенного ионами 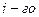 вида, к общему количеству электричества
вида, к общему количеству электричества 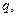 перенесенному всеми ионами, находящимися в растворе, называют числом переноса ионов:
перенесенному всеми ионами, находящимися в растворе, называют числом переноса ионов:
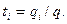 (32.42)
(32.42)
В соответствии с этим определением сумма чисел переноса всех видов ионов в растворе равна единице.
Для симметричного электролита KA, диссоциирующего на два вида ионов 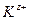 и
и 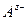 , количество электричества, перенесенное катионами и анионами, составит соответственно:
, количество электричества, перенесенное катионами и анионами, составит соответственно:
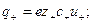
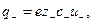 (32.43)
(32.43)
где 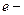 элементарный заряд;
элементарный заряд; 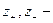 заряд катиона и аниона;
заряд катиона и аниона; 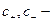 молярная концентрация катионов и анионов
молярная концентрация катионов и анионов 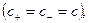
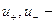 абсолютные скорости ионов. Отношение чисел переноса катионов
абсолютные скорости ионов. Отношение чисел переноса катионов 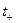 и анионов
и анионов 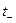 равно отношению их абсолютных скоростей или подвижностей:
равно отношению их абсолютных скоростей или подвижностей:
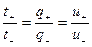 ,
,
а поскольку 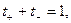 то
то
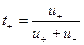 и
и 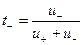 (32.44)
(32.44)
Из уравнений видно, что число переноса данного вида иона зависит от абсолютной скорости и подвижности обоих видов ионов, т. е. в растворах разных электролитах числа переноса одного и того же иона различны.
На степень гидратации ионов, величины их абсолютной скорости и числа переноса влияют концентрация раствора и температура. С ростом концентрации примерно до 0,1 моль/л для большинства электролитов числа переноса ионов изменяются незначительно; в области более высоких концентраций это изменение заметнее. При повышении температуры размеры гидратных оболочек слабо гидратированных ионов уменьшаются менее резко, чем сильно гидрати-рованных (а иногда даже увеличиваются). В результате величины абсолютной подвижности катионов и анионов сближаются, и их числа переноса стремятся к 0,5.
[1] Диэлектрическая проницаемость - величина, показывающая, во сколько раз сила взаимодействия двух зарядов в изучаемой среде меньше, чем в вакууме.
[2] Зарядом иона z называют отношение заряда иона, выраженного в кулонах, к заряду электрона Кл; заряд иона, в кулонах, соответственно, равен произведению ez.
[3] Далее во всех случаях, где это особо не оговаривается, с целью упрощения мы будем говорить о коэффициенте активности и активности электролитов, понимая, что речь идет о среднем коэффициенте активности и средней активности. В дальнейшем пренебрегается и различием между тремя способами выражения активности (коэффициента активности), что вполне допустимо для разбавленных растворов.
[4] Используют также определение – радиус (толщина) ионной атмосферы, дебаевский радиус.
[5] Обозначение единицы электрической проводимости сименс, как и всех других единиц, происходящих от имен собственных, пишется с прописной буквы (См). Это обозначение нельзя путать с обозначением единицы измерения длины – сантиметр (см).
