Суточная потребность организма человека в аминокислотах
План
- Главная проблема человечества – обеспечение продуктами питания.
Государственная политика в области здорового питания.
- Организация здорового питания населения.
- Классификация пищевых продуктов.
1. Среди основных проблем, стоящих перед человеческим обществом в наше время, можно выделить несколько главных, превалирующих над всеми другими:
- обеспечение населения земного шара продуктами питания;
- обеспечение энергией;
- обеспечение сырьем, в том числе водой;
- охрана окружающей среды, экологическая и радиационная безопасность жителей планеты, замедление негативных последствий интенсивной производственной деятельности и защита человека от результатов этой негативной деятельности.
Среди них одной из самых важных и сложных является обеспечение населения земного шара продуктами питания. Являясь одним из важнейших факторов окружающей среды, питание с момента рождения до самого последнего дня жизни человека влияет на его организм. Ингредиенты пищевых веществ, поступая в организм человека с пищей и преобразуясь в ходе метаболизма в результате сложных биохимических превращений в структурные элементы клеток, обеспечивают наш организм пластическим материалом и энергией, создают необходимую физиологическую и умственную работоспособность, определяют здоровье, активность и продолжительность жизни человека, его способность к воспроизводству. Состояние питания, поэтому, является одним из важнейших факторов, определяющих здоровье нации.
Продукты питания должны не только удовлетворять потребности человека в основных питательных веществах и энергии, но и выполнять профилактические и лечебные функции.
На решение этих задач и направлена концепция государственной политики в области здорового питания населения Российской Федерации на период до 2005 г., одобренная постановлением Правительства РФ от 10 августа 1998 г. №917.
Под государственной политикой в области здорового питания понимается комплекс мероприятий, направленный на создание условий, обеспечивающих удовлетворение потребностей населения в рациональном здоровом питании с учетом его традиций, привычек, экономического положения, в соответствии с требованиями медицинской науки.
2. Последние десятилетия характеризуются стойким ухудшением показателей здоровья населения России: продолжает снижаться средняя продолжительность жизни (она составила 58 лет у мужчин и 73 года у женщин, в среднем 65,5 года — это значительно ниже, чем в большинстве развитых стран); увеличивается общая заболеваемость. Смертность на 1000 человек увеличилась с 11,2 в 1990 г. до 15,4 в 2000 г. Среди причин заболеваемости и смертности ведущее место занимают сердечно-сосудистые и онкологические заболевания, развитие которых в определенной степени связано с питанием. Снижается уровень грудного вскармливания, ухудшаются показатель здоровья и антропометрические характеристики детей, подростков, а также состояние здоровья лиц пожилого возраста. Одной из важнейших причин этого является неудовлетворительное питание.
У большинства населения России, поданным Института питания РАМН, выявлены нарушения полноценного питания, обусловленные как недостаточным потреблением пищевых веществ (табл. 1.2), так и нарушением пищевого статуса населения России, в первую очередь недостатком витаминов, макро- и микроэлементов, полноценных белков, и нерациональным их соотношением. Важнейшие нарушения пищевого статуса населения России (по данным Института питания РАМН):
- избыточное потребление животных жиров;
- дефицит полиненасыщенных жирных кислот;
- дефицит полноценных (животных) белков;
- дефицит витаминов (аскорбиновой кислоты, рибофлавина (В2), тиамина (В,), фолиевой кислоты, ретинола (А) и |3-каротина, токоферола и других);
- дефицит минеральных веществ (кальция, железа);
- дефицит микроэлементов (селена, цинка, йода, фтора);
- дефицит пищевых волокон.
Негативное влияние оказывает потребление некачественных, фальсифицированных и опасных для здоровья человека продуктов. На устранение этих недостатков и направлен закон РФ № 29-ФЗ «О качестве и безопасности пищевых продуктов» (2 января 2000 г.).
Организация здорового питания населения — сложный и многофакторный процесс, который можно реализовать, только опираясь на глубокие знания, стройную научную концепцию и продуманную научно-техническую политику.
Технический прогресс в пищевой промышленности во многом определяется демографическими изменениями (численность населения, увеличение доли пожилых и больных людей), социальными изменениями, изменениями в условиях жизни и труда (рост численности городского населения, изменение характера труда, социальное расслоение общества). Он связан с достижениями медицины, фундаментальных наук (физика, химия, микробиология), новыми технологическими возможностями, которые появились у производителей продуктов питания в результате развития науки, технологии, техники; ухудшением экологической обстановки; жесткой конкуренцией на рынке продуктов питания. Все это требует не только коренного совершенствования технологии получения традиционных продуктов, но и создания нового поколения пищевых продуктов, отвечающих возможностям и реалиям сегодняшнего дня. Это продукты со сбалансированным составом, низкой калорийностью, с пониженным содержанием сахара и жира и повышенным — полезных для здоровья ингредиентов, функционального и лечебного назначения, с увеличенным сроком хранения, быстрого приготовления и, конечно, совершенно безопасных для человека.
Таблица 1.2. Потребление основных продуктов питания в России, кг/год на 1 человека (баланс продовольствия, по данным Госкомстата)
| Пищевые продукты | Рекомендуемая норма | 1999, % от рекомендуемой нормы | ||||||||||
| Хлебопродукты, в том числе | ||||||||||||
| импортные | ||||||||||||
| Мясо и мясопродукты | ||||||||||||
| (в том числе импортные) | (6) | (Ю) | (9) | (9) | (10) | (13) | (14) | (17) | (16) | (П) | ||
| Рыба и рыбопродукты | 23,7 | 9,4 | 8,4 | |||||||||
| Молоко и молочные продукты | ||||||||||||
| (в том числе импортные) | (38) | (47) | (21) | (39) | (37) | (38) | (32) | (36) | (33) | (25) | ||
| Яйца, шт | ||||||||||||
| Сахар | ||||||||||||
| (в том числе импортный) | (28) | (24) | (23) | (21) | т | (18) | (20) | (24) | (24) | (24) | ||
| Картофель | ||||||||||||
| Овощи и бахчевые культуры | ||||||||||||
| (в том числе импортные) | (12) | (12) | (10) | (Н) | (4) | (6) | (6) | (13) | (12) | (Н) | ||
| Фрукты и ягоды | ||||||||||||
| (в том числе импортные) | (15) | (17) | (10) | (7) | (Ю) | (9) | (П) | (12) | (15) | (14) | ||
| Масло растительное | 13,0 | 10,2 | 7,8 | 6,7 | 7,0 | 6,6 | 7,4 | 7,9 | 8,4 | 8,8 | 8,9 | |
| (в том числе импортное) | (2,0) | (1,7) | (1,3) | (1,2) | (1,1) | (1,1) | (2,2) | (4,7) | (3,8) | (3,9) |
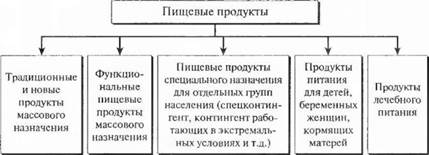
3. Рис. 1.1. Классификация современных продуктов питания
Создание новых и совершенствование технологии получения традиционных продуктов питания требует изучения структуры питания населения России, анализа состояния пищевых и перерабатывающих отраслей АПК, правильной и продуманной научно-технической политики в области здорового питания с учетом демографических изменений, развития науки в области здорового питания. Важным также является решение вопросов производства растительного белка, биологически активных добавок (БАД), пищевых добавок (ПД), организация индустрии продуктов детского питания. Решающая роль в реализации этих вопросов принадлежит развитию исследований по пищевой химии, пищевой биотехнологии, разработке новых технологических решений и оборудования, методов анализа и системы управления качеством.
Большое место в реализации этих вопросов, как уже указывалось, принадлежит пищевой химии. Пищевая химия — один из разделов химической науки, значение которой, учитывая роль питания в жизни общества, крайне велико. Это наука о химическом составе пищевых систем (сырье, полупродукты, готовые пищевые продукты), его изменениях в ходе технологического потока под влиянием различных факторов (физических, химических, биохимических и т. д.), включающих липид-белковое, липид-углеводное, белок-белковое, белок-углеводное взаимодействия, общих закономерностях этих превращений. Она включаетизуче
Пищевая химия — дисциплина, значение которой все возрастает. Знание основ пищевой химии даст возможность технологам решить один из важнейших вопросов современности — обеспечение населения планеты качественными продуктами питания. В связи с этим ничуть не потеряла своей актуальности мысль И. П. Павлова, сформулированная им в 1904 г. при вручении ему Нобелевской премии: «...над всеми явлениями человеческой жизни господствует забота о насущном хлебе».
Контрольные вопросы
1. Расскажите об основных положениях государственной политики в области здорового питания. 2. Приведите классификацию современных продуктов питания.
3. Дайте определение дисциплины «Пищевая химия».
4. Какие вопросы она изучает? Определите ее место и роль в создании современных продуктов питания.
Тема 2. «Белки»
План
1. Аминокислоты: понятие, получение, свойства, изомерия и номенклатура.
2. Белки: понятие, строение, классификация, свойства, гидратация, денатурация, пенообразование, гидролиз, горение, цветные реакции.
3. Пищевая ценность белков.
4. Нуклеиновые кислоты.
1. Аминокислоты – гетерофункциональные соединения, которые содержат две функциональные группы: аминогруппу – NH2 и карбоксильную группу - COOH , связанные с углеводородным радикалом. Общую формулу простейших аминокислот можно записать так: H2N – CH2 - COOH
Так как аминокислоты содержат две различные функциональные группы, которые оказывают влияние друг на друга, их реакции отличаются от характерных свойств карбоновых кислот и аминов.
Получение.
Аминокислоты можно получить из карбоновых кислот, заместив их в радикале атом водорода на галоген, а затем на аминогруппу при взаимодействии с амином, например:
P(кр.)
CH3COOH + Cl2 → ClCH2COOH + HCl
уксусная к-та хлоруксусная к-та
ClCH2COOH + 2NH3 → H2NCH2COOH + NH4Cl
аминоуксусная к-та
Смесь аминокислот обычно получают кислотным гидролизом белков.
Свойства.
Аминогруппа определяет основные свойства аминокислот, так как способна присоединять к себе катион водорода по донорно-акцепторному механизму за счёт наличия свободной электронной пары у атома азота.
Карбоксильная группа определяет кислотные свойства этих соединений. Следовательно, аминокислоты – это амфотерные органические соединения.
Со щелочами они реагируют как кислоты:
H2NCH2COOH + NaOH → H2NCH2COONa + H2O
С сильными кислотами – как основания-амины:
H2NCH2COOH + HCl → [H3NCH2COOH]+Cl-
Так как аминокислоты в водных растворах ведут себя как амфотерные соединения, то в живых организмах они играют роль буферных веществ, поддерживающих определённую концентрацию ионов водорода.
Аминокислоты представляют собой бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше 2000С. Они растворимы в воде и нерастворимы в эфире. В зависимости от состава радикала они могут быть сладкими, горькими или безвкусными.
Аминокислоты подразделяются на природные и синтетические. Среди природных аминокислот (около 150) выделяют протеиногенные аминокислоты (около 20), которые входят в состав белков. Они представляют собой L- формы. Примерно половина из этих аминокислот относится к незаменимым, так как они не синтезируются в организме человека (валин, лейцин, изолейцин, фенилалалин, лизин, треонин, цистеин, метионин, гистидин, триптофан). В организм человека данные вещества поступают с пищей. Если их количество в пище будет недостаточным, нормальное развитие и функционирование организма человека нарушаются. При отдельных заболеваниях организм не в состоянии синтезировать и некоторые другие аминокислоты.
Изомерия и номенклатура.
Изомерия аминокислот определяется различным строением углеродной цепи и положением аминогруппы, например:
4 3 2 1
CH3 – CH2 – CH – COOH CH3
I I
NH2 CH3 – C – COOH
2-аминобутановая кислота I
NH2 2-амино-2-метилпропановая кислота
Широко распространены также названия аминокислот, в которых положения аминогрупп обозначаются буквами греческого алфавита: ᾴ, β,γ и т.д.
γ β ᾴ
CH3 – CH2 – CH – COOH
I
NH2
ᾴ-аминомасляная кислота
2.Белки.
Белками называют высокомолекулярные (молекулярная масса от 5-10 тыс. до 1 млн и более) природные полимеры. молекулы которых построены из остатков аминокислот, соединённых амидной (пептидной) связью.
Белки также называют протеинами (от греч. «протос» - первый, важный). Число остатков аминокислот в молекуле белка очень сильно колеблется и иногда достигает нескольких тысяч. Каждый белок обладает своей, присущей ему последовательностью расположения аминокислотных остатков.
Белки выполняют разнообразные биологические функции: каталитические (ферменты), регуляторные (гормоны), структурные (коллаген, фиброин), двигательные (миозин), транспортные (гемоглобин, миоглобин), защитные (иммуноглобулины, интерферон), запасные (казеин, альбумин, глиадин) и другие. Среди белков встречаются антибиотики и вещества, оказывающие токсическое действие.
Белки – основа биомембран, важнейшей составной части клетки и клеточных компонентов. Они играют ключевую роль в жизни клетки, составляя как бы материальную основу её химической деятельности.
Исключительное свойство белка – самоорганизация структуры, т. е. его способность самопроизвольно создавать определённую, свойственную только данному белку пространственную структуру. По существу, вся деятельность организма (развитие, движение, выполнение им различных функций и многое другое) связана с белковыми веществами. Без белков невозможно представить себе жизнь.

Химический состав организма человека
Белки – важнейшая составная часть пищи человека и животных, поставщик необходимых им аминокислот.
Строение.
В пространственном строении белков большое значение имеет характер радикалов в молекулах аминокислот. Неполярные радикалы аминокислот обычно располагаются внутри макромолекулы белка и обусловливают гидрофобные взаимодействия; полярные молекулы, содержащие ионогенные (образующие ионы) группы, обычно находятся на поверхности макромолекулы белка и характеризуют электростатические (ионные) взаимодействия. Полярные неионогенные радикалы могу располагаться как на поверхности, так и внутри белковой молекулы. Они участвуют в образовании водородных связей.
Полипептидные цепи или отдельные участки внутри полипептидной цепи могут быть дополнительно связаны между собой связями. Большую роль в создании структуры белков играют ионные и водородные связи, а также гидрофобное взаимодействие – особый вид контактов между гидрофобными компонентами молекул белков в водной среде. Все эти связи имеют различную прочность и обеспечивают образование сложной, большой молекулы белка.
Несмотря на различие в строении и функциях белковых веществ, их элементный состав колеблется незначительно ( в % на сухую массу): углерода – 51-53; кислорода – 21,5-23,5; азота – 16,8-18,4; водорода – 6,5-7,3; серы – 0,3-2,5. Некоторые белки содержат в небольших количествах фосфор, селен и другие элементы.
Последовательность соединения аминокислотных остатков в полипептидной цепи получила название первичной структуры белка.
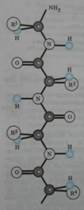
Первичная структура белков
Белковая молекула может состоять из одной или нескольких полипептидных цепей, каждая из которых содержит различное число аминокислотных остатков. Учитывая число их возможных комбинаций, можно сказать, что разнообразие белков почти безгранично, но не все из них существуют в природе. Общее число различных типов белков у всех видов живых организмов составляет 1010 – 1012. Для белков, строение которых отличается исключительной сложностью, кроме первичной, различают и более высокие уровни структурной организации: вторичную, третичную, а иногда и четвертичную структуры.
Классификация
Существует несколько классификаций белков. В их основе лежат разные признаки:
Ø степень сложности (простые и сложные0;
Ø форма молекул 9глобулярные и фибриллярные белки);
Ø растворимость в отдельных растворителях (водорастворимые, растворимые в отдельных солевых растворах – альбумины, спирторастворимые – проламины, растворимые в разбавленных щелочах и кислотах – глутелины);
Ø выполняемая функция (например, запасные белки, скелетные и т.п.).
Свойства.
Белки – амфотерные электролиты. При определённом значении рН среды (она называется изоэлектрической точкой) число положительных и отрицательных зарядов в молекуле белка одинаково. Это одно из основных свойств белка. Белки в этой точке электронейтральны, а их растворимость в воде наименьшая. Способность белков снижать растворимость при достижении электронейтральности их молекул используется для выделения их из растворов, например, в технологии получения белковых продуктов.
Гидратация.
Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объём увеличиваются. Набухание белка сопровождается его частичным растворением. Гидрофильность отдельных белков зависит от их строения. Имеющиеся в составе и расположенные на поверхности белковой макромолекулы гидрофильные амидные, аминные и карбоксильные группы притягивают к себе молекулы воды, строго ориентируя их на поверхности молекулы. Окружающая белковые глобулы гидратная оболочка препятствует агрегации и осаждению, а следовательно, способствует устойчивости растворов белка. В изоэлектрической точке белки обладают наименьшей способностью связывать воду, происходит разрушение гидратной оболочки вокруг белковых молекул, поэтому они соединяются, образуя крупные агрегаты. Агрегация белковых молекул происходит и при их обезвоживании с помощью некоторых органических растворителей, например этилового спирта. Это приводит к выпадению белков в осадок. При изменении рН среды макромолекула белка становится заряженной, и его гидратационная способность меняется.
При ограниченном набухании концентрированные белковые растворы образуют сложные системы, называемые студнями. Студни не текучи, упруги, обладают пластичностью, определённой механической прочностью, способны сохранять свою форму. Глобулярные белки могут полностью гидратироваться, растворяясь в воде (например, белки молока), образуя растворы с невысокой концентрацией. Гидрофильные свойства белков, т.е. их способность набухать, образовывать студни, стабилизировать суспензии, эмульсии и пены, имеют большое значение в биологии и пищевой промышленности. Очень подвижным студнем, построенным в основном из молекул белка, является цитоплазма – полужидкое содержимое клетки. Сильно гидратированный студень – сырая клейковина, выделенная из пшеничного теста, она содержит до 65% воды. Различная гидрофильность клейковинных белков – один из признаков, характеризующих качество зерна пшеницы и получаемой из него муки. Гидрофильность белков зерна и муки играет большую роль при хранении и переработке зерна, в хлебопечении. Тесто, которое получают в хлебопекарном производстве, представляет собой набухший в воде белок, концентрированный студень, содержащий зёрна крахмала.
Денатурация белков.
При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и ряда других факторов) происходит изменение вторичной, третичной и четвертичной структур белковой макромолекулы, т.е. её пространственной структуры. Первичная структура, а следовательно, и химический состав белка не меняются. Изменяются физические свойства: снижается растворимость, способность к гидратации, теряется биологическая активность. Меняется форма белковой макромолекулы, происходит агрегирование. В тоже время увеличивается активность некоторых химических групп, облегчается воздействие на белки протеолитических ферментов, а следовательно, он легче гидролизуется.
В пищевой технологии особое практическое значение имеет тепловая денатурация белков, степень которой зависит от температуры, продолжительности нагрева и влажности. Это необходимо помнить при разработке режимов термообработки пищевого сырья, полуфабрикатов, а иногда и готовых продуктов. Особую роль процессы тепловой денатурации играют при бланшировании растительного сырья, сушке зерна, выпечке хлеба, получении макаронных изделий. Денатурация белков может вызываться и механическим воздействием (давлением, растиранием, встряхиванием, ультразвуком). Наконец, к денатурации белков приводит действие химических реагентов (кислот, щелочей, спирта, ацетона).Все эти приёмы широко используются в пищевой и биотехнологии.
Пенообразование
Под процессом пенообразования понимают способность белков образовывать высококонцентрированные системы «жидкость-газ», называемые пенами. Устойчивость пены, в которой белок является пенообразователем, зависит не только от его природы и от концентрации, но и от температуры. Белки в качестве пенообразователей широко используются в кондитерской промышленности (пастила, зефир, суфле). Структуру пены имеет хлеб, а это влияет на его вкусовые свойства.
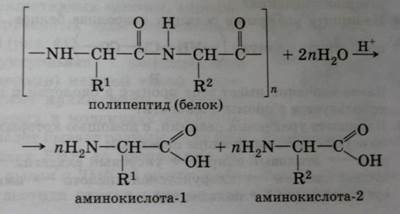
Молекулы белков под влиянием ряда факторов могут разрушаться или вступать во взаимодействие с другими веществами с образованием новых продуктов. Для пищевой промышленности можно выделить два очень важных процесса: 1) гидролиз белков под действием ферментов и 2) взаимодействие аминогрупп белков или аминокислот с карбонильными группами восстанавливающих сахаров. Под влиянием протеаз – ферментов, катализирующих гидролитическое расщепление белков, последние распадаются на более простые продукты (поли- и дипептиды) и в конечном итоге на аминокислоты. Скорость гидролиза белка зависит от его состава, молекулярной структуры, активности фермента и условий.
Гидролиз белков
Реакцию гидролиза с образованием аминокислот в общем виде можно записать так:
Горение
Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жжёных перьев.
Цветные реакции
Используют следующие реакции:
· ксантопротеиновую, при которой происходит взаимодействие ароматических гетероароматических циклов в молекуле белка с концентрированной азотной кислотой, сопровождающееся появлением желтой окраски;
· биуретовую, при которой происходит взаимодействие слабощелочных растворов белков с раствором сульфата меди (II) с образованием комплексных соединений между ионами меди и полипептидами. Реакция сопровождается появлением фиолетово-синей окраски.
Пищевая ценность белков.
Белок – наиболее важный компонент пищи человека. Основные источники пищевого белка: мясо, молоко, рыба, продукты переработки зерна, хлеб, овощи.
Потребность человека в белке зависит от его возраста, пола. Характера трудовой деятельности. В организме здорового взрослого человека должен быть баланс между количеством поступающих белков и выделяющимися продуктами распада. Для оценки белкового обмена введено понятие азотного баланса. В зрелом возрасте у здорового человека существует азотное равновесие, т.е. количество азота, полученного с белками пищи, равно количеству выделяемого азота. В молодом растущем организме идёт накопление белковой массы, образуется ряд нужных для организма соединений, поэтому азотный баланс будет положительным – количество поступающего азота с пищей превышает количество выводимого из организма. У людей пожилого возраста, а также при некоторых заболеваниях, , недостатке в рационе питания белков, незаменимых аминокислот, витаминов, минеральных веществ наблюдается отрицательный азотный баланс – количество выделенного из организма азота превышает его поступление в организм. Длительный отрицательный азотный баланс ведёт к гибели организма. На белковый обмен влияют биологическая ценность и количество поступающего с пищей белка.
Биологическая ценность белков определяется сбалансированностью аминокислотного состава и атакуемостью белков ферментами пищеварительного тракта.
В организме человека белки расщепляются до аминокислот, часть из них 9заменимые) являются строительным материалом для создания новых аминокислот, однако имеется 8 аминокислот (незаменимые), которые не образуются в организме взрослого человека, они должны поступать с пищей. Снабжение организма человека необходимым количеством аминокислот – основная функция белка в питании. В белке пищи должен быть сбалансирован не только состав незаменимых аминокислот, но и должно быть определённое соотношение незаменимых и заменимых аминокислот, в противном случае часть незаменимых будет расходоваться не по назначению.
Наиболее близки к «незаменимому» белку животные белки. Большинство растительных белков содержат недостаточное количество незаменимых аминокислот (одной или нескольких).
В то же время необходимо помнить. Что некоторые аминокислоты при тепловой обработке, длительном хранении продуктов могут образовать не усвояемые организмом соединения, т.е. становиться «недоступными». Это снижает ценность белка.
Биологическая ценность белков может быть увеличена добавлением лимитирующей аминокислоты или внесением компонента с её повышенным содержанием.
Животные и растительные белки усваиваются организмом неодинаково. На степень усвоения организмом белков оказывает влияние технология получения пищевых продуктов и их кулинарная обработка. В большинстве пищевых производств при соблюдении технологии не происходит деструкции аминокислот. При умеренном нагревании пищевых продуктов усвояемость белков несколько возрастает (частичная денатурация белков облегчает доступ протеаз к пептидным связям). При интенсивной тепловой обработке усвояемость снижается.
Суточная потребность взрослого человека в белке разного вида 1 – 1,5 г белка на 1кг массы тела (детей 4 – 1,5г). Доля животных белков должна составлять приблизительно 55% от общего его количества в рационе.
Для повышения пищевой ценности продуктов питания необходимо увеличение доли белкового компонента, сбалансированности его аминокислотного состава. Один из путей решения этой задачи – получение белковых продуктов из белоксодержащих отходов пищевых производств, например семя масличных после удаления масла, отходов мясной и молочной промышленности, и их использование для улучшения биологической ценности существующих продуктов или создание новых продуктов питания.
Нуклеиновые кислоты
Название этих веществ происходит от латинского слова nuleus – ядро и указывает, что нуклеиновые кислоты являются составной частью клеточных ядер. Нуклеиновые кислоты – высокомолекулярные соединения с молекулярными массами от 200 до нескольких миллионов. Нуклеиновые кислоты обнаружены во всех растительных и животных клетках, вирусах, бактериях и грибах.
Различают два вида нуклеиновых кислот – дезоксирибонуклеиновые (ДНК) и рибонуклеиновые (РНК). Различие в названии объясняется тем, что молекула ДНК содержит моносахарид дезоксирибозу, а РНК – рибоза. В настоящее время известно большое число разновидностей ДНК и РНК, отличающихся друг от друга по строению и значению в обмене веществ. Они являются исключительно важными элементами клетки, обеспечивающими хранение и передачу генетической (наследственной) информации в живых организмах. ДНК находится преимущественно в хромосомах клеточного ядра (99% всей ДНК клетки), а также в митохондриях и хлоропластах. РНК входит в состав ядрышек, рибосом, минохондрий, пластид, цитоплазмы. Молекула ДНК состоит из двух полинуклеотидных цепочек, спирально закрученных одна относительно другой.
Структура молекулы ДНК
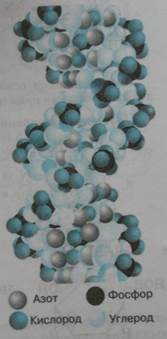
Структурными компонентами (мономерами) каждой такой цепочки служат нуклеотиды, количество которых в молекулах нуклеиновых кислот бывает разным – от 80 в молекулах РНК до нескольких десятков тысяч в ДНК. В состав любого нуклеотида входит одно из азотистых оснований – аденин, гуанин, цитозин и тимин. Нуклеиновые кислоты, как и белки, имеют первичную, вторичную и третичную структуру.
ДНК является основным строительным материалом генов, в которых хранится наследственная информация организма. РНК выполняет различные функции, так как существует в виде трёх разновидностей: рибосомальная, транспортная и информационная.
Контрольные вопросы.
1. Почему аминокислоты являются гетерофункциональными соединениями?
2. Какими особенностями строения должны обладать аминокислоты, используемые для синтеза волокон, и аминокислоты, участвующие в биосинтезе белков в клетках живых организмов?
3. Чем отличаются реакции поликонденсации от реакций полимеризации? В чём их сходство?
4. Охарактеризуйте строение белков. Какую роль играют различные виды химических связей в формировании различных структур белковых молекул?
5. Как соотносятся между собой понятия «пептид», «полипептид», «полиамид», «белок»?
6. Охарактеризуйте важнейшие физические и химические свойства белков.
7. С помощью каких реакций можно распознать белки?
8. Какую роль играют белки в жизни организмов?
9. В чём заключается пищевая ценность белков?
10. Дайте характеристику нуклеиновым кислотам.
Практические задания
1. Запишите уравнения реакций аминопропионовой кислоты с серной кислотой и гидроксидом натрия, а также с метиловым спиртом. Всем веществам дайте названия по систематической номенклатуре.
2. Как получают аминокислоты? Запишите уравнения реакций получения аминопропионовой кислоты из пропана.
3. Напишите уравнения реакций, с помощью которых можно осуществить следующие переходы: этан → этиловый спирт → уксусный альдегид → уксусная кислота → хлоруксусная кислота → аминоуксусная кислота → полипептид
Тема 3. «Углеводы»
План
1. Углеводы, их классификация и значение.
2. Моносахириды. Гексозы. Глюкоза.
3. Полисахариды. Крахмал и целлюлоза.
4. Превращения углеводов в технологических процессах.
5. Пищевая ценность углеводов.
1.Углеводы – органические вещества, молекулы которых состоят из атомов углерода, водорода и кислорода, причём водород и кислород находятся в них, как правило, в таком же соотношении, как и в молекуле воды (2/1).
Общая формула углеводов – Сn (Н2О)m, т.е. они как бы состоят из углерода и воды, отсюда и название класса, которое имеет исторические корни. В дальнейшем было установлено, что имеются углеводы, в молекулах которых не соблюдается указанное соотношение, например дезоксирибоза – С5Н10О4. Известны также органические соединения, состав которых соответствует приведённой общей формуле, но которые не принадлежат к классу углеводов. К ним относятся, например, формальдегид СН2О и уксусная кислота СН3СООН.
Углеводы по их способности гидролизоваться можно разделить на три основные группы: моно-, ди- и полисахариды.
Моносахариды – углеводы, которые не гидролизуются (не разлагаются водой). В свою очередь, в зависимости от числа атомов углерода моносахариды подразделяются на триозы (молекулы которых содержат три углеродных атома), тетрозы, пентозы, гексозы и т.д.
В природе моносахариды представлены преимущественно пентозами и гексозами.
К пентозам относятся, например рибоза – С5Н10О5 и дезоксирибоза – С5Н10О4.
К гексозам, имеющим общую молекулярную формулу С6Н12О6, относятся, например, глюкоза, фруктоза, галактоза.
Дисахариды – углеводы, которые гидролизуются с образованием двух молекул моносахаридов. Общая формула – С12Н22О11. Общее уравнение гидролиза:
С12Н22О11 + Н2О → 2С6Н12О6
дисахарид гексоза
К дисахаридам относятся:
· сахароза (обычный пищевой сахар), который при гидролизе образует одну молекулу глюкозы и молекулу фруктозы. Она содержится в большом количестве в сахарной свекле, сахарном тростнике, клёне, сахарной пальме, кукурузе и т.д.
· мальтоза (солодовый сахар), которая гидролизуется с образованием двух молекул глюкозы. Мальтозу можно получить при гидролизе крахмала под действием ферментов, содержащихся в солоде, - пророщенных, высушенных и размолотых зёрнах ячменя;
· лактоза (молочный сахар), которая гидролизуется с образованием молекулы глюкозы и галактозы. Она содержится в молоке млекопитающих животных (до 4-6%) обладает невысокой сладостью и используется как наполнитель в драже и аптечных таблетках.
Сладкий вкус разных моно- и дисахаридов различен. Так, самый сладкий моносахарид – фруктоза – в полтора раза слаще глюкозы, которую принимают за эталон. Сахароза в 2 раза слаще глюкозы и в 4-5 раз – лактозы, которая почти безвкусна.
Полисахариды – крахмал, гликоген, декстрины, целлю
