Изобразите принципиальную схему компрессорной станции .
Каков принцип ее работы?
Принципиальная схема КС представлена на рис. 1.6 Взаимодействие линейной части магистрального газопровода и КС осуществляется через узел подключения, обеспечивающий следующий режимы работы газопровода: подача газа по газопроводу с компримированием его на подключаемой КС — основной режим; подача газа по газопроводу без компримирования на КС — временный режим работы газопровода при вынужденной остановке (отключении) КС или сокращении подачи газа по газопроводу; подача газа по газопроводу при периодической очистке его полости очистными устройствами от механических примесей, влаги и конденсата — временный режим.
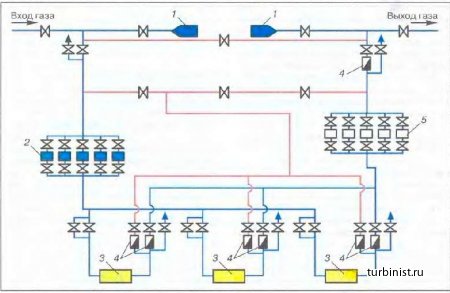
Рис.1.6 Принципиальная технологическая схема компрессорной станции: 1 - установка очистки газопровода; 2 — установка очистки газа; 3 - газоперекачивающий агрегат; 4 — обратный клапан; 5 - установка охлаждения газа.
В зависимости от типа привода, мощности и технологии, назначения состав сооружений КС и их взаимное расположение могут изменяться. По функциональному назначению и с учетом технологии. и противопожарных требований площадки КС обычно разделяются на 2 зоны: производственную и служебно-производственного комплекса.
В состав производственной зоны КС входят все производственные и вспомогательные сооружения непосредственно связанные с технологическим процессом сжатия газа: площадка газоперекачивающих агрегатов (ГПА), размещенных в индивидуальных или общем зданиях; установка очистки газа; установка охлаждения газа с трансформаторной подстанцией; установка подготовки топливного, пускового и импульсного газов; производственно энергетический блок (операторная диспетчерская, котельная, аккумуляторная, компрессорная, дизельная электростанция, помещения персонала и др.); блок маслохозяйства; склад горюче-смазочных материалов: резервуар пенного пожаротушения.
В состав служебно -производственного комплекса КС входят: водопроводные сооружения с резервуарами противопожарного запаса воды; электро-подстанция, служебно-эксплуатационный и ремонтный блок (ремонтно-механические мастерские, гараж, узел связи, мастерские и лаборатории служб КИП и автоматики, энергетические помещения персонала линейно-производств. управление магистрального газопровода и др.); столовая и ее вспомогательное здание склад материалов; открытая стоянка автомашин и тяжелой техники; очистные сооружения хозяйственно-бытовой канализации; склад метанола мойка машин с очистными сооружениями.
Основные виды коррозии трубопроводов.
Различают 4 основных вида коррозии: электрохимическая коррозия, водородная, кислородная коррозия и химическая.
Электрохимическая коррозия.
Разрушение металла под воздействием возникающих в коррозионной среде гальванических элементов называют электрохимической коррозией. Не следует путать с электрохимической коррозией коррозию однородного материала, например, ржавление железа или т. п. При электрохимической коррозии (наиболее частая форма коррозии) всегда требуется наличие электролита (Конденсат, дождевая вода и т. д.), с которым соприкасаются электроды — либо различные элементы структуры материала, либо два различных соприкасающихся материала с различающимися окислительно-восстановительными потенциалами. Если в воде растворены ионы солей, кислот, или т. п., электропроводность её повышается, и скорость процесса увеличивается.
Коррозийный элемент.
При соприкосновении двух металлов с различными окислительно-восстановительными потенциалами и погружении их в раствор электролита, например, дождевой воды с растворенным углекислым газом CO2, образуется гальванический элемент, так называемый коррозионный элемент. Он представляет собой не что иное, как замкнутую гальваническую ячейку. В ней происходит медленное растворение металлического материала с более низким окислительно-восстановительным потенциалом; второй электрод в паре, как правило, не корродирует. Этот вид коррозии особо присущ металлам с высокими отрицательными потенциалами. Так, совсем небольшого количества примеси на поверхности металла с большим редокс-потенциалом уже достаточно для возникновения коррозионного элемента. Особо подвержены риску места соприкосновения металлов с различными потенциалами, например, сварочные швы или заклёпки.
Если растворяющийся электрод коррозионно-стоек, процесс коррозии замедляется. На этом основана, например, защита железных изделий от коррозии путём оцинковки — цинк имеет более отрицательный потенциал, чем железо, поэтому в такой паре железо восстанавливается, а цинк должен корродировать. Однако в связи с образованием на поверхности цинка оксидной плёнки процесс коррозии сильно замедляется.
.
Водородная и кислородная коррозия
Если происходит восстановление ионов H3O+ или молекул воды H2O, говорят о водородной коррозии или коррозии с водородной деполяризацией. Восстановление ионов происходит по следующей схеме:
2H3O+ + 2e− → 2H2O + H2
или
2H2O + 2e− → 2OH− + H2
Если водород не выделяется, что часто происходит в нейтральной или сильно щелочной среде, происходит восстановление кислорода и здесь говорят о кислородной коррозии или коррозии с кислородной деполяризацией:
O2 + 2H2O + 4e− → 4OH−
Коррозионный элемент может образовываться не только при соприкосновении двух различных металлов. Коррозионный элемент образуется и в случае одного металла, если, например, структура поверхности неоднородна.
Химическая коррозия.
Химическая коррозия — взаимодействие поверхности металла с коррозионно-активной средой, не сопровождающееся возникновением электрохимических процессов на границе фаз. В этом случае взаимодействия окисления металла и восстановление окислительного компонента коррозионной среды протекают в одном акте. Например, образование окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом:
4Fe+3O2→2Fe2O3{\displaystyle 4Fe+3O_{2}\rightarrow 2Fe_{2}O_{3}}
При электрохимической коррозии ионизация атомов металла и восстановление окислительного компонента коррозионной среды протекают не в одном акте и их скорости зависят от электродного потенциала металла (например, ржавление стали в морской воде).
