Современные представления о биологическом окислении. Компоненты дыхательной цепи и их характеристика.
Биологическое окисление - процесс переноса электронов.
Биологическое окисление протекает:• при низкой температуре; • в присутствии воды; • без образования пламени.
В организме механизм образования СО2 – декарбоксилирование.
Если акцептором электронов является кислород, то такой процесс называется тканевым дыханием.
Если акцептором электронов является другое вещество, кроме кислорода, то такой процесс называется анаэробным окислением.
Биологическое окисление: • Процесс транспорта электронов; • Процесс многоступенчатый; • Процесс полиферментативный; • Конечный продукт тканевого дыхания – Н2О; • Энергия выделяется постепенно.
Биологическое окисление - многоступенчатый процесс транспорта электронов (на начальных этапах и протонов) осуществляемый комплексом ферментов, сопряженный с образованием энергии.
Биологическое окисление начинается с дегидрирования.
Этап осуществляется с помощью: НАД – зависимые дегидрогеназы; ФАД – зависимые дегидрогеназы. Это первичные акцепторы водорода.
В НАД рабочей частью является витамин РР - НИКОТИНАМИД.
| -2ē -2Н+ |
| +2ē +2Н+ |
| НАДН (НАДФН) + Н+ Восстановленная форма |
| НАД+ (НАДФ+) окисленная форма Окисленная форма |
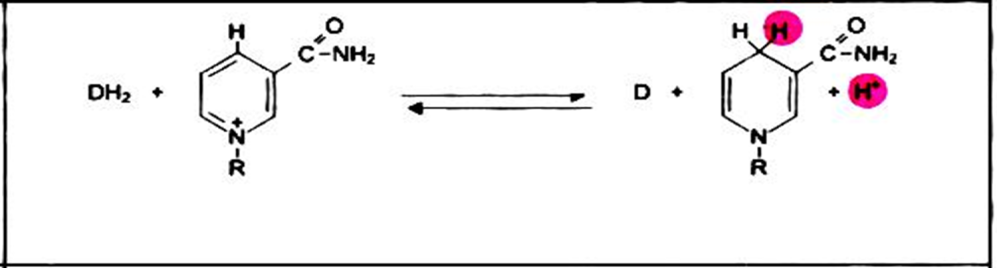
НАД+ + 2Н+ + 2е НАДН + Н+
В ФАД и ФМН рабочей частью является флавин (изоаллоксазин) – компонент В2.
| -2ē -2Н+ |
| +2ē +2Н+ |
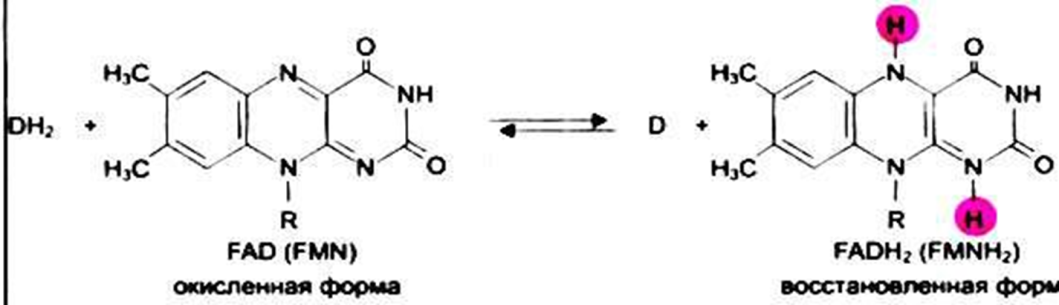
ФАД+ + 2Н + 2е ФАДН2
Компоненты дыхательной цепи: в основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы.
Комплекс ферментов переноса электронов и протонов от субстрата к кислороду называется электронтранспортная цепь (ЭТЦ), или цепь переноса электронов (ЦПЭ), или дыхательная цепь (ДЦ).
Компоненты дыхательной цепи: • в основном сложные белки, локализованные во внутренней мембране митохондрий и объединенные в комплексы; • комплекс I (НАДН-дегидрогеназа); • комплекс II (СДГ); • убихинон (кофермент Q); • комплекс III (цитохромы b, с1); • цитохром с; • комплекс IV (цитохромы а, а3 – цитохромоксидаза).
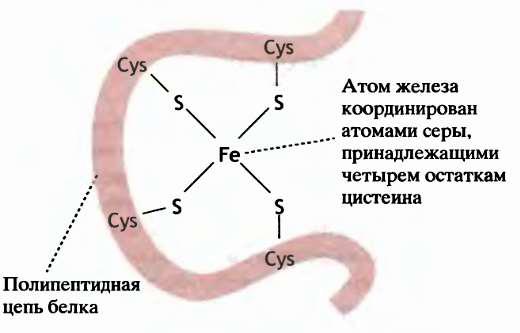 Комплекс I (НАДН-дегидрогеназа): • флавинзависимый фермент (кофермент ФМН); • субстрат – кофермент НАДН2; • содержит железо-серные белки; • донор протонов и электронов для убихинона.
Комплекс I (НАДН-дегидрогеназа): • флавинзависимый фермент (кофермент ФМН); • субстрат – кофермент НАДН2; • содержит железо-серные белки; • донор протонов и электронов для убихинона.
Комплекс II (СДГ): • флавинзависимый фермент (кофермент ФАД); • донор протонов и электронов для убихинона.
Убихинон (кофермент Q):• Quinone – хинон; • Ubiquitos – вездесущий; • производное бензохинона с боковой цепью из 10 звеньев изопрена (коэнзим Q10); • небелковый компонент ДЦ; • подвижный компонент; • акцептор протонов и электронов от флавинзависимых дегидрогеназ; • донор электронов для комплекса III; • переносит протоны в межмембранное пространство митохондрий.
| +е |
| -е |
Комплекс III (коэнзим Q – дегидрогеназа): • в составе цитохромы b, с1; • акцептор электронов от коэнзима Q; • донор электронов для цитохрома с.
Цитохром с: • не объединяется в комплекс; • акцептор электронов от комплекса III; • донор электронов для комплекса IV.
Комплекс IV (цитохромоксидаза):• содержит цитохромы а, а3,способные взаимодействовать с кислородом, ионы меди; • акцептор электронов от комплекса III; • донор электронов для кислорода.
Полная ЭТЦ - взаимодействие субстрата с НАД. Укороченная ЭТЦ - взаимодействие субстрата с ФАД. Порядок компонентов дыхательной цепи обусловлен величиной их red-ox потенциалов.
Окислительно-восстановительный потенциал: -выражается в вольтах;- чем отрицательнее E0´, тем меньше сродство к электронам;- связан с изменением свободной энергии системы *E0´ - табличная величина;- в дыхательной цепи E0´ изменяется от -0,32В до +0,81В; - -0,32 характерно для НАД+ + 2H+ + 2ē → НАДН2 (НАД+ /НАДН2); - +0,81 характерно для ½ О2 + 2H+ + 2ē → H2О (О2 /О2-).
19. Пути синтеза АТФ в клетках, клеточная локализация процессов синтеза АТФ, примеры реакций. Молекулярные механизмы окислительного фосфорилирования (теория Митчелла).
Окислительное фосфорилирование - процесс образования АТФ из АДФ и Н3РО4 за счёт энергии переноса электронов в дыхательной цепи.
Субстратное фосфорилирование - это процесс образования АТФ из АДФ и Н3РО4 за счёт энергии распада какого-либо субстрата.
В основной дыхательной цепи выделяются 3 пункта, где может образоваться АТФ:1.) НАД KоQ;•НАДН2 — 3 АТФ2.) ЦИТ.b ЦИТ.с•ФАДН2 — 2 АТФЗ.) ЦИТ.а ЦИТ.а3
Теория окислительного фосфорилирования (Питер Митчелл, 1961). Основные положения теории: 1.) Мембрана митохондрий в норме не проницаема для протонов. 2.) В процессе транспорта электронов протоны «перекачиваются» в межмембранное пространство - образуется электрохимический потенциал. 3.) Обратный транспорт протонов в матрикс митохондрий сопряжен с синтезом АТФ.
Процесс транспорта электронов происходит во внутренней мембране, где расположены ферменты ЦПЭ. Реакции окисления субстратов происходят в матриксе митохондрий. Протоны переносятся в межмембранное пространство, а электроны продвигаются по дыхательной цепи.
Тканевое дыхание.Дегидрирование без пламени и взрыва собразованием эндогенной воды при участииоксидаз(оксидазный путь окисления):• процесс транспорта электронов и протонов;• происходит в митохондриях;• конечным акцептором является кислород;• конечный продукт тканевого дыхания – Н2О;• энергия выделяется постепенно;• процесс многоступенчатый;• процесс полиферментативный.
Тканевое дыхание многоступенчатый процесс транспорта электронов. И протонов от субстрата на кислород с образованием эндогенной воды, осуществляемый комплексом ферментов, сопряженный с постепенным выделением энергии.
Во время тканевого дыхания создаётся электрохимический потенциал:• концентрационный (протонный); • разности потенциалов (электрический). При этом наружная сторона внутренней мембраны заряжается «+», а внутренняя «-». Т.е. создается градиент концентрации протонов; • электрический и концентрационный потенциал составляют протондвижущую силу, которая перемещает протоны обратно в матрикс митохондрий; • через протонные каналы, образованные ферментом - АТФ-синтазой. АДФ + Н3РО4 → АТФПротоны проходят обратно в матрикс, при этом активность АТФ-синтазы повышается. Образуется АТФ.
АТФ-синтаза: • интегральный белок внутренней мембраны митохондрий. • гидрофобная часть F0 пронизывает мембрану и образует канал, по которому протоны переносятся обратно в матрикс. • каталитическая часть F1 выступает в матрикс, соединяется с F0 при помощи γ-субъединицы, образующей вращающийся за счет изменения конформации стержень.
• электрохимический потенциал заставляет двигаться протоны по каналу АТФ-синтазы обратно в матрикс и параллельно происходят конформационные изменения в F1. • в результате из АДФ и Фн образуется АТФ. • для синтеза 1АТФ используется электрохимический потенциал, генерируемый при перепаде напряжения в одном из пунктов сопряжения (перекачка 4H+).
Модель синтеза АТФ: - протон проваливается через полуканал с наружной стороны митохондриальной мембраны, протонирует аминокислоту ротора, на аминокислоте появляется дополнительный положительный заряд. - протонированная аминокислота на роторе перемещается к следующей половинке канала, ведущей внутрь митохондрии, протон попадает во второй полуканал и матрикс, аминокислота освобождается от положительного заряда. - заряды в роторе и статоре расположены таким образом, что протонирование – депротонирование приводит к повороту белка.
В соответствии с хемоосмотической теорией Митчелла окисление НАДH + H+ и ФАДН2 в дыхательной цепи создаёт сначала электрохимический протонный потенциал, градиент концентрации ионов на внутренней мембране, а обратный транспорт протонов через мембрану сопряжен с фосфорилированием АДФ, т.е. образованием АТФ.
Коэффициент окислительного фосфорилирования (Р/О):отношение количества фосфорной кислоты (Р),использованной на фосфорилирование АДФ, к атомукислорода (О), поглощённого в процессе дыхания.для НАДН+ + Н+ Р/О = 3,для ФАДН2 Р/О = 2.
Дыхательный контроль - зависимость интенсивности дыхания митохондрий от концентрации АДФ. АТФ/(АДФ+АМФ)
Условия образования АТФ:1.) Целостность мембраны - непроницаемость её для протонов. 2.) Наличие специальных каналов. 3.) Движение протонов в матрикс сопровождается выделением энергии, используемой для синтеза АТФ.
В обычных условиях процессы окисления и фосфорилирования сопряжены и сопровождаются синтезом АТФ. Разобщение окислительного фосфорилирования (свободное окисление) - окисление идёт, а фосфорилирования нет, вся энергия выделяется в виде тепла.
Причиной разобщения окислительного фосфорилирования могут стать:- нарушение целостности /функции мембран митохондрий;- протонофоры, ионофоры (липофильныевещества): 2,4–динитрофенол, билирубин, тироксин, высшие жирные кислоты.
Пути использования кислорода в организме (альтернативный путь окисления):
| Оксидазный 90% О2 О2 + 4ē + 4Н+→2Н2О в митохондриях сопровождается синтезом АТФ синезом АТФ |
| Оксигеназный 9% О2 Не сопровождается синтезом АТФ |
| Свободнорадикальный 1% О2 Неферментативно Не сопровождается синтезом АТФ синтезом АТФ |
| Оксигеназный путь |
| Монооксигеназный |
| Диоксигеназный |
| +Н |
| S-Н +O2 S-OOH |
| S-Н + O2 + Н S-OH + H2O |
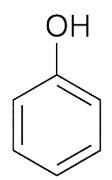 |
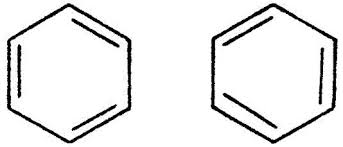 |
| бензол |
| (цит.Р450) |
| гидроксилаза |
| + НАДФ+ + Н2О |
| фенол |
| + О2 + НАДФН2 |
