Классификация каталитических реакций с водородом
Огромное разнообразие каталитических реакций с водородом можно классифицировать следующим образом:
1. Каталитическое гидрирование или присоединение водорода по месту кратных связей (С = С, С º С, С—С ароматических, N = N, N = C и т. д.).
2. Деструктивное гидрирование (гидрогенолиз, или гидрокрекинг) — крекинг в присутствии водорода. К этому типу относятся также реакции гидродеалкилирования.
3. Каталитическое восстановление — взаимодействие водорода с кислородсодержащими соединениями.
Основное значение в нефтеперерабатывающей промышленности имеют первые два типа реакций. Каталитическое восстановление используется в процессах гидроочистки нефтяных фракций от кислородсодержащих соединений.
Наиболее благоприятные условия проведения гидрогенизационных процессов выбираются на основе химико-термодинамических исследований.
Термодинамика и катализаторы гидрирования
Реакции гидрирования по физико-химическим закономерностям имеют много общего с реакциями дегидрирования. Они являются системой обратимых превращений.
Все реакции гидрирования экзотермичны. Тепловые эффекты основных реакций гидрирования имеют те же значения, что и реакции дегидрирования, но противоположны по знаку. Ниже даны значения ΔН0298 для некоторых реакций, кДж/моль:
Н2
RCH=CH2 ® RCH2CH3 : 113—134
2 Н2
CH≡CH ® CH3 CH3 : 310
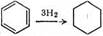 : 206
: 206
Н2
RCHO ® RCH2OH : 67—84
2 Н2
RCN ® RСH2NH2 : 134—159
По способности к гидрированию классы соединений располагаются в следующие ряды: алкены > алкины > арены
альдегиды > кетоны > нитрилы > карбоновые кислоты.
Вследствие экзотермичности основных реакций гидрирования очевидно, что с повышением температуры равновесие будет смещаться в сторону эндотермических реакций дегидрирования. Поэтому процессы гидрирования следует проводить при возможно более низкой температуре. Однако для достижения приемлемой скорости реакций в промышленности процесс ведут при 100–400 °С (в зависимости от активности катализатора и реакционной способности сырья) и давлении от 0,15–0,5 до 30–40 МПа.
Ввиду способности катализаторов одинаково ускорять как прямой, так и обратный синтез реакции гидрирования и дегидрирования должны катализироваться одними и теми же веществами. Это, главным образом, металлы I и VIII групп (Сu, Ag, Fe, Co, Ni, Pt, Pd), некоторые окислы (MgO, Fe2O3, Cr2O3, MoO3, WO3), сульфиды (MoS3, WS3) и многофункциональные катализаторы.
Список литературы
1. Эрих В.Н., Расина М.Г., Рудин М.Г. Химия и технология нефти и газа. – Л.: Химия, 1985.
2. Химия нефти и газа / под ред. В.А.Проскурякова и А.Е.Драбкина. – Л.: Химия, 1981.
3. Эрих В.Н. Химия нефти и газа. – Л.: Химия, 1969.
4. Сафиева Р.З. Физикохимия нефти. – М.: Химия, 1998.
5. Рябов В.Д. Химия нефти. – М.: Нефть и газ, 1998.
6. Добрянский А.Ф Химия нефти. – Л.: Техиздат, 1961.
7. Гриценко А.И., Островская Г.Д., Юшкин В. В. Углеводородные конденсаты месторождений природного газа. – М.: Недра, 1983.
8. Имашев У.Б. Промышленная органическая химия на предприятиях Республики Башкортостан. – Уфа: УГНТУ, 2000.
СОДЕРЖАНИЕ
Введение ………………………………………………………………….3
1. Происхождение нефти ………………………………………………..5
2. Элементарный состав нефти………………………………………...13
3. Фракционный состав нефти…………………………………………13
3.1. Детонационная стойкость горючего………………………………16
3.2. Переработка углеводородного сырья……………………………..18
3.2.1.Переработка каменного угля……………………………………..22
3.2.2.Перспективы развития энергетики ……………………………...25
4. Групповой углеводородный состав нефти. Классификация
нефти …………………………………………………………………...27
5. Молекулярный вес ………………………………………………….28
6. Физические свойства нефти ……………………………………….29
6.1. Плотность ………………………………………………………….29
6.2. Вязкость……………………………………………………………..31
6.3. Температурные переходы и агрегатные превращения ………….33
6.4. Тепловые свойства ………………………………………………..34
6.5. Оптические свойства ……………………………………………...36
6.6. Электрические свойства ………………………………………….37
7. Фазовое равновесие в системе «нефть-газ» ………………………..37
8. Классификация углеводородов ……………………………………..41
8.1. Предельные (насыщенные) углеводороды. Алканы
(парафины)..…………………………………………….………....42
8.1.1. Парафины и церезины …………………………………………...46
8.2. Предельные углеводороды. Циклоалканы ……………………….48
8.3. Непредельные (ненасыщенные) углеводороды. Алкены
(этиленовые углеводороды) ………………………………………...51
8.4. Непредельные углеводороды. Алкадиены ……………………….55
8.5. Непредельные углеводороды. Алкины (ацетиленовые
углеводороды)………………………………………………..........57
8.6. Ароматические углеводороды. Бензол и его гомологи………….62
9. Неуглеводородные соединения нефти ……………………………..67
9.1. Кислородные соединения …………………………………………67
9.2. Азотистые соединения …………………………………………….69
9.3. Сернистые соединения …………………………………………….70
10. Смолистые вещества ……………………………………………….72
Минеральные компоненты нефти ...……………………………74
Методы выделения компонентов ...……………………………...75
12.1. Перегонка………………………………………………………….75
12.2. Азеотропная и экстрактивная ректификация, экстракция,
абсорбция……………………………………………………………..77
12.3. Адсорбция…………………………………………………………82
12.4. Кристаллизация…………………………………………………...86
12.5. Диффузионные методы разделения углеводородов…………...89
13.Природные и попутные газы. Применение газа …………………91
13.1. Природные газы …………………………………………………92
13.2. Попутные (нефтяные) газы ……………………………………..94
13.3. Применение газа …………………………………………………94
14.Термические превращения углеводородов нефти………………...96
14.1. Термодинамика процесса………………………………………..96
14.2. Кинетика и механизм процесса………………………………….98
14.3. Термические превращения углеводородов
в газовой фазе……………………………………………….…...101
14.3.1. Превращения алканов…………………………………………101
14.3.2. Превращения циклоалканов ………………………………….102
14.3.3. Превращения алкенов…………………………………...….…104
14.3.4. Превращения алкадиенов и алкинов…………………………105
14.3.5. Превращения аренов…………………………………………..106
15. Термокаталитические превращения ……………………………..108
15.1. Механизм действия катализаторов окислительно-
восстановительного типа ……………………………………….108
15.2. Кислотный катализ………………………………………………109
15.3. Реакции карбкатионов…………………………………………..110
15.4. Каталитический крекинг………………………………………..112
15.4.1. Превращения алканов…………………………………….......112
15.4.2. Превращение циклоалканов………………………………….114
15.4.3. Превращение алкенов…………………………………………116
15.4.4. Превращение аренов…………………………………………..116
15.4.5. Катализаторы каталитического крекинга ………………….117
15.4.6. Каталитический крекинг в промышленности……………….118
15.5. Каталитический риформинг……………………………………120
15.5.1. Химические основы процесса……………………………......120
15.5.2. Катализаторы риформинга……………………………………124
15.5.3. Каталитический риформинг в промышленности ………….126
16. Гидрогенизация в нефтепереработке…………………………….127
16.1. Классификация процессов………………………………………127
16.2. Классификация каталитических реакций с водородом………128
16.3. Термодинамика и катализаторы гидрирования……………….128
Список литературы…………………………………………………….129
