Классификация катионов при кислотно-щелочной системе анализа
Методы анализа»
Химические методы анализа
Введение
Аналитическая химия- наука, разрабатывающая теоретические основы и экспериментальные методы определения состава веществ и (или) их смесей.
Анализ-в переводе с греческого αναλυση означает разложение, расчленение, разделение целого (предмета или явления) на его более простые составные части.
Различают качественный (1) и количественный (2) анализы:
(1) − это установление природы веществ и (или) их частей (элементов, атомов, молекул, ионов и т.д.);
(2) − это определение абсолютного или относительного содержания отдельных составных частей вещества или их смесей.
Методы, позволяющие определять содержание отдельных элементов, называют элементным анализом; функциональных групп – функциональным анализом; индивидуальных химических соединений с определенным молекулярным весом – молекулярным анализом; разделения и определения отдельных структурных составляющих гетерогенных систем называют фазовым анализом.
До сих пор различают органический и неорганический анализы. Аналитическая химия ‑ прикладная наука. Ее методы использовались и используются в развитии естественных наук, установлении законов природы (например, закона постоянства состава, кратных отношений; определение атомных масс элементов, химических формул веществ и т.д.). Химико-технологический контроль процессов и сред является обязательным условием современного производства. Введение стандартов качества на выпускаемую продукцию также невозможно без аналитики. Достижения аналитической химии находят применение в геохимии, геологии, минералогии, физике, биологии, металлургии, физиологии, медицине, астрономии и т.д.
Методы качественного и количественного анализов условно делят на химические (1), физико-химические (2) и физические (3).
Первые основаны на химическом превращении исследуемого вещества в другое вещество, обладающее характерными свойствами. Вторые изучают физические явления, сопровождающие химические процессы. Третьи основаны на исследовании зависимости физического параметра анализируемого объекта от состава. (2) и (3) объединяют под названием инструментальные методы. В последнее время они занимают главенствующее место в аналитической химии в связи с большей точностью, информативностью и экспрессностью. К инструментальным методам относят: спектральные (оптические), электрохимические, распределительные (хроматографические) и радиометрические.
Классификация химических реакций
1. По энергетическому признаку: эндотермические и экзотермические.
N2 + O2 → 2NO; ΔH > 0, эндотермическая, энергия в форме теплоты поглощается; в адиабатических условиях температура системы понижается; энтальпия повышается;
Cl2 + H2 → 2HCl; ΔH < 0, экзотермическая, энергия в форме теплоты выделяется; в адиабатических условиях температура системы повышается; энтальпия понижается;
2. По признаку изменения числа участников: образования и разложения.
H2 + ½ О2 → Н2О - реакция образования;
2КМnO4 → K2MnO4 + MnO2 + О2) - реакция разложения.
3. По признаку изменения состава: реакции обмена и замещения.
AgNO3 + КСl → AgCl↓ + КNO3 - обмена;
Hg(NO3)2 + Cu → Нg↓ + Cu(NO3)2 - замещения.
4. По признаку обратимости: обратимые и необратимые.
N2 + 3H2 ↔ 2NH3 - обратимая;
HCl + NaOH → NaCl + H2O - необратимая.
5. По признаку изменения степени окисления
6. : без изменения и окислительно-восстановительные (Redox).
BaCl2 + H2SO = BaSO4↓ + 2HCl, без изменения;
Redox:
- межмолекулярные: SO2 + 2H2S = 3S↓ + 2H2O;
- внутримолекулярные: KClO3 = KCl + 3/2O2↑;
- диспропорционирования: Cl2 + H2O ↔ HClO + HCl.
Степень окисления (окислительное число) – условный заряд, приписываемый атому элемента, из предположения полного смещения электронов. Степень окисления (С.О.)определяется по следующим правилам:
- для простого вещества С.О.=0;
- для одноатомного иона С.О.= зарядовому числу (заряду) иона;
- сумма С.О. атомов в молекуле = 0;
- сумма С.О. атомов в многоатомном ионе = заряду иона;
- для элементов 1А группы Периодической таблицы С.О.=+1 везде;
- для элементов 2А группы Периодической таблицы С.О.=+2 везде;
- для фтора С.О.=−1 во всех соединениях;
- для водорода С.О.=+1 в соединениях с неметаллами,
С.О.=−1 в соединениях с металлами и бором;
- для кислорода С.О.=−1 в пероксидах,
С.О.=−2 во всех соединениях, кроме OF2;
- для галогенов С.О.=−1 в соединениях с металлами, неметаллами (кроме кислорода) и галогенами ниже в группе.
Аналитические реакции
Реакцию, используемую для аналитических целей, принято называть аналитической реакцией, а вещество, ее вызывающую – реагентом. В аналитике используют реакции, сопровождающиеся явными (или хорошо заметными) внешними эффектами. Это могут быть изменение цвета или интенсивности окраски раствора, образование или растворение осадка, выделение газа с определенным запахом или цветом и т.д.
Аналитический сигнал или аналитический признак – любое свойство системы отличающее ее от остальных.
В качественном анализе различают три вида реакций: реакции открытия (обнаружения) тех или иных веществ, групп, ионов и т.д.; реакции идентификации (подтверждения) или проверки правильности открытия; реакции осаждения (отделения), используемые в систематическом анализе для разделения групп ионов.
Аналитические реакции по способу их выполнения делятся на «мокрые», которые проводятся в (водных) растворах, и «сухие», к которым относят:
- окрашивание пламени газовой горелки солями (обычно летучими хлоридами, карбонатами, нитратами) некоторых металлов в определенный цвет, например, Na − желтый, K − фиолетовый, Sr − карминово-красный, Ba − зеленый, Ca − кирпично-красный;
- образование окрашенных перлов (стекол) при сплавлении, например, Na2B4O7·10H2O, NaNH4HPO4·4H2O с солями металлов: Cr − изумрудно-зеленые, Mn − аметистово-фиолетовые;
- метод растирания, образования окрашенных соединений на фарфоровой пластинке, например, синего (NH4)2[Co(SCN)4] при совместном растирании CoSO4 и NH4SCN.
В зависимости от массы анализируемого вещества различают макроанализ (>1 г), микроанализ (1 мг ÷ 1 мкг), ультрамикроанализ (<1 мкг). На практике чаще имеют дело с полумикроанализом, занимающим промежуточное положение.
Условия выполнения реакции
Среда (кислая, нейтральная или щелочная) создается прибавлением к раствору кислоты, щелочи или буферного раствора; например, осадки, растворимые в кислотах, не образуются в кислой среде.
Температура должна быть соответствующей, так как осадки (например, PbCl2) могут растворяться в горячем растворе; некоторые реакции идут на холоде, некоторые – при нагревании.
Концентрация должна быть достаточной, так как осадок образуется только из пересыщенного раствора, то есть когда его концентрация больше растворимости.
Характеристика реакций
Чувствительность реакции характеризуется взаимосвязанными показателями:
- открываемый минимум (m) – наименьшая масса вещества (в мкг), которая может быть обнаружена посредством данной реакции. Аналитическим целям удовлетворяют реакции, для которых m < 50 мкг;
- минимальная (предельная) концентрация (1:q) – характеризует минимальную концентрацию Cmin, при которой обнаружение вещества возможно в небольшом (одной капле) объеме раствора; q – объем раствора (мл), в котором содержится 1 грамм вещества;
- предельное разбавление (q) − величина, обратная концентрации; аналитическим целям удовлетворяют реакции, эффективные при разбавлении более 1000.
Если минимальный объем, требуемый для обнаружения ионов Vmin (мл), то
 .
.
Аналитическая реакция тем чувствительнее, чем меньше открываемый минимум и предельная концентрация и чем больше предельное разбавление.
Специфичность. Специфической реакцией на данный ион называется такая реакция, которая позволяет обнаружить его в условиях опыта в смеси с другими ионами. Например, реакция со щелочью является специфической для обнаружения NH4+ в виде NH3 по запаху.
Ионные уравнения
При анализе неорганических веществ в большинстве случаев имеют дело с водными растворами кислот, оснований, солей, являющихся электролитами. Поэтому «мокрыми» реакциями открывают ионы, а не элементы или вещества.
Все реакции в (водных) растворах электролитов являются реакциями между ионами. Они называются ионными реакциями, а уравнения этих реакций − ионными уравнениями.
В этих уравнениях в молекулярной форме записываются вещества, которые:
- мало ионизируют (НОН),
- малорастворимы (выпадают в осадок, BaSO4↓),
- являются газами (CO2↑),
- являются простыми веществами (О2).
Например:
1. NaOH + HCl → NaCl + HOH – уравнение в молекулярной форме;
Na+ + OH‾ + H+ + Cl‾ → Na+ + Cl‾ + HOH – уравнение в ионной форме, полное ионное уравнение;
OH ‾ + H+ → HOH – сокращенное ионное уравнение.
2. BaCl2 + K2SO4 → 2KCl + BaSO4↓;
Ba2+ + 2Cl‾ + 2K+ + SO42‾ → 2K+ + 2Cl‾ + BaSO4↓;
Ba2+ + SO42‾ → BaSO4↓ – сокращенное ионное уравнение.
Для обнаружения Cl‾ используют раствор AgNO3:
HCl + AgNO3 → AgCl↓ + HNO3
− образуется белый творожистый осадок. Данной реакцией открывают не элемент хлор вообще, а именно хлорид ион Cl‾. Она неэффективна, если хлор присутствует в ином виде, например, NaClO3 или CHCl3. Также можно отметить, что реагентом является не AgNO3, а именно Ag+, а суть реакции выражается сокращенным ионным уравнением:
Ag+ + Cl− → AgCl.
Глава1.Качественный дробный и систематический анализы
Применяя специфические реакции можно обнаружить соответствующие ионы так называемым дробным методом, то есть непосредственно в отдельных порциях («раздробленного») исследуемого раствора, не учитывая возможное присутствие других ионов. При этом не имеет значения и порядок открытия ионов.
Если нет специфических реакций, то используют определенную последовательность реакций обнаружения отдельных ионов, представляющую систематический ход анализа. Он состоит в том, что к обнаружению каждого данного иона приступают лишь после того, как все другие ионы, мешающие его обнаружению, будут предварительно обнаружены и удалены из раствора.
Например, анализируемая смесь предположительно содержит Ca2+ и Ba2+, а нужно определить, есть ли Ca2+. Оба катиона образуют белые осадки с оксалат анионом (наиболее чувствительная реакция на кальций). Поэтому сначала выясняют, есть ли в растворе Ba2+, действуя хроматом калия, зная, что хромат кальция растворим:
Ba2+ + CrO42− → BaCrO4↓.
Если в отдельной порции раствора присутствие Ba2+ не подтвердилось, то открывают в другой порции Ca2+. Если Ba2+ присутствует, то его отделяют осаждением в виде желтого BaCrO4 центрифугированием или фильтрованием, проверяя полноту осаждения добавлением к фильтрату капли реагента. Затем в фильтрате открывают Сa2+ добавлением (NH4)2C2O4. Образование белого осадка доказывает присутствие Ca2+.
Кроме осаждения для отделения используют выпаривание и экстракцию органическими растворителями.
При систематическом ходе анализа ионы выделяют из сложной смеси не по одиночке, а целыми группами, пользуясь одинаковым отношением их к действию некоторых реагентов, называемых групповыми реагентами. Выделяемые группы ионов называют аналитическими группами. Групповой реагент должен удовлетворять следующим требованиям:
- практически полное осаждение (10-6 М);
- осадок должен легко растворяться в кислотах;
- избыток реагента не должен мешать открытию оставшихся ионов.
Существуют различные системы анализа: сульфидная, кислотно-щелочная, фосфатная и т.д.
Систематический ход анализа смеси катионов I÷VI групп
Анализ смеси катионов I÷VI групп начинают с открытия дробным методом катионов: NH4+, Na+, Fe2+, Fe3+, Сr3+, Sn2+, Mn2+, Bi3+, Sb3+, Co2+, Ni2+, Cu2+:
NH4+ - нагреванием со щелочами,
Na+ - методом фотометрии пламени,
Fe2+ - в солянокислой среде реакцией с К3[Fe (CN)6],
Fe3+ - в солянокислой среде реакцией с К4[Fe (CN)6],
Cr3+ - реакцией окисления в кислой среде до Cr2O72− и пероксида хрома СrO5 + амиловый спирт,
Sn2+ - реакцией с фосфоромолибдатом аммония (NH4)3[PMo12 O40],
Mn2+ - реакцией окисления висмутатом в кислой среде до МnO4−,
Bi3+ и Sb3+ - гидролизом,
Со2+ - реакцией с роданидом аммония NH4SCN + амиловый спирт,
Ni2+ - реакцией с диметилглиоксимом в присутствии NH3+амиловый спирт,
Сu2+ - реакцией с К4[Fe (CN)6],
- реакцией с избытком концентрированного аммиака.
Таблица 1
Таблица 2
Таблица 3
| Катион | Реагент | Аналитическая реакция | Методика эксперимента | Аналитический сигнал | |
| Fe3+ | K4 [Fe(CN)6] | 4Fe(NO3)3 + 3K4[Fe(CN)6] = = Fe4[Fe(CN)6]3↓ + 12KNO3 | 0,5 мл З (задачи) +1 мл Н2О+(1к HCl) + Р(реагент) по каплям | Синий осадок (окраш-е) берлинской лазури | |
| Cu2+ | K4Fe(CN)6 | 2Cu(NO3)2 + K4[Fe(CN)6] = Cu2[Fe(CN)6]↓ + 4KNO3 | 0,5 мл З+Р по каплям | Красно-бурый осадок | |
| NH3 ·H2O(изб) | Cu(NO3)2 + NH3· H2O = Cu(OH)NO3↓ + NH4NO3 и далее Cu(OH)NO3 + 3NH3 · H2O+NH4NO3= = [Cu(NH3)4](NO3)2 + 4H2O | 0,5 мл З+Р (избыток) | Ярко-синее окраш-е за счет комплекса [Cu(NH3)4]2+ | ||
| Cr3+ | H2O2 (NaОН, pH>7) | Cr(NO3)3 + 3NaOH = Cr(OH)3↓ + 3NaNO3 Cr(OH)3 + NaOH = Na[Cr(OH)4] 2Na[Cr(OH)4]+2NaOH+3H2O2 =2Na2CrO4+8H2O | 0,5 мл З + 1 мл NaOH + +1÷2к H2O2 → нагреть до кипения | Желтое окрашивание за счет CrO42- иона | |
| H2O2 (H2SО4 , pH<7) | 2Na2CrO4+H2SO4=Na2Cr2O7+Na2SO4+H2O Na2Cr2O7+4H2O2+H2SO4=2H2CrO6+3H2O+Na2SO4 | Р-р Na2CrO4 (после опыта 1) охладить + H2SO4 по каплям до оранжевой окраски + 0,5 мл изоамилового спирта + 1÷2к Н2О2 → встряхнуть | Синее окрашивание спиртового слоя за счет надхромовой к-ты H2CrO6 | ||
| Mn2+ | NaBiO3(тв) | 2Mn(NO3)2 + 5NaBiO3 + 16HNO3= = 2HMnO4 + 5Bi(NO3)3 + 5NaNO3 + 7H2O | 5 к З+3 мл Н2О + 2÷3к HNO3 + 2÷3 кристалла тв. Р | Розово-малиновое окраш-е за счет MnО4- иона | |
| Ni2+ | Диметилглиоксим DMG | NiCl2 + 2DMG = Ni(DMG)2↓ + 2HCl | 0,5 мл З+изб.NH3 ·H2O (до голубой окр.) + 0,5 мл изоамилового спирта + 10 к DMG → встряхнуть | Розовый осадок в спиртовом слое | |
| Co2+ | NH4SCN (тв) | Co(NO3)2 + 4NH4SCN = (NH4)2 [Co(SCN)4] + + 2NH4NO3 | 0,5 мл З + 0,5 мл изоамил. спирта + 3÷5 кристаллов тв. Р → встряхнуть | Синее окрашивание спиртового слоя | |
| NH4+ | NaOH(4N) | NH4Cl + NaOH = NH3↑ + NaCl + H2O | 2 мл З + 4 мл Р → нагреть до кипения | Запах выдел. аммиака (посинение лакмусовой, покраснение фф бумажки) | |
| K+ | Na3[Co(NO2)6] | 3KNO3 + Na[Co(NO2)6] = K3 [Co(NO2)6] ↓ + 3NaNO3 | 0,5 мл З + Р по каплям | Желтый осадок | |
| Na+ | Пламя газ. горелки | Полоску фильтр. бумаги смочить р-ром З → поместить в пламя, не допуская загорания | Желтое окрашивание пламени | ||
| Al3+ | Ализарин С14Н6О2(ОН)2 | 2÷3 к З+5 к 2н NН3 ∙Н2О (рН=10÷11) + 1÷2 к ализарина | Оранжево-красный осадок не растворим в уксусной кислоте | ||
| Sn2+ | Вi(NO3)3 | SnCl2 + 3 NaOH → Na[Sn(OH)4] + 2 NaCl 3 Na[Sn(OH)4] + 2 Bi(NO3)3 + 3 NaOH → 2 Bi↓ + 3 Na2[Sn(OH)6] | 2÷3 к З+8÷10 к 2н NaOH + Р по каплям | Черный осадок металлического висмута | |
| Mg2+ | Магнезон, п – нитробензол, азорезорцин Na2HPO4 | Адсорбция красителя на поверхности Mg(OH)2 | 3 к З+2 к NН3 ∙Н2О + 2 к Р 3 к З + (NH4Cl + NH4OH) + Р по каплям | Малиновый цвет Белый кристаллический осадок |
Таблица 4
«Классификация» анионов
| № | Анион | Реагент | Примечание |
| I | SO32−, SO42−, S2O32−, CO32−, PO43−, BO2−, B4O72−, CrO42−, C2O42−, Cr2O72−, F−, SiO32−, AsO33−, AsO43− | Раствор BaCl2 , нейтральный или слабо-щелочной , pH = 7 ÷ 9 | Соли, малорастворимые в воде и разбавленных кислотах |
| II | Cl−, Br-−, I−, S2−, CN−, SCN−, [Fe(CN)6]3−, IO3−, BrO33−, ClO− | Раствор AgNO3 (+ 2N HNO3) | Соли, малорастворимые в воде и разбавленной HNO3 |
| III | NO3−, NO2−, ClO3−, CH3COO−, MnO4− | — | Соли бария и серебра растворимы в воде |
Общие реакции анионов
| Реактивы | Анионы I группа: | ||||||
| SO42– | SO32– | CO32– | PO43– | ||||
| BaCl2 в нейтральной среде | Белый осадок ВаSO4 | Белый осадок ВаSO3 | Белый осадок ВаSO3 | Белый осадок ВаHPO4 | |||
| BaCl2 в кислой среде | ВаSO4 | ― | ― | ― | |||
| AgNО3 в азотно-кислой среде | ― | ― | ― | ― | |||
| AgNО3 в нейтральной среде | Белый осадок Ag2SO4 | Белый осадок Ag2SO3 | Белый осадок Ag2CO3 | Желтый осадок Ag3PO4 | |||
| H2SO4 | ― | Выделение SO2 | Выделение СО2 | ― | |||
| Реактивы | Анионы II группа | ||||||
| Cl– | Br– | I– | |||||
| BaCl2 в нейтральной среде | ― | ― | ― | ||||
| BaCl2 в кислой среде | ― | ― | ― | ||||
| AgNО3 в азотно-кислой среде | Белый осадок AgCl | Светло-желтый осадок AgBr | Желтый осадок AgI | ||||
| AgNО3 в нейтральной среде | AgCl | AgBr | AgI | ||||
| H2SO4 | ― | ― | ― | ||||
| Реактивы | Анионы III группа | ||||||
| NO3– | CH3COOH– | ||||||
| BaCl2 в нейтральной среде | ― | ― | |||||
| BaCl2 в кислой среде | ― | ― | |||||
| AgNО3 в азотно-кислой среде | ― | XX | |||||
| AgNО3 в нейтральной среде | ― | ― | |||||
| H2SO4 | ― | Образование CH3COOH– | |||||
Вопросы
1. В чем различие дробного и систематического качественного химического анализа?
2. Какие реагенты называют групповыми?
3. Написать реакции обнаружения ионов Cu2+, Fe3+, Pb2+, Cr3+, Mn2+.
4. В чем заключается классификация анионов? Привести примеры реакций.
5. Написать реакции обнаружения анионов Cl-, SO42-, NO3.
6. Какие ионы можно обнаружить с помощью пламени?
7. Привести примеры использования комплексонообразования для открытия ионов. Написать реакции.
8. Для обнаружения каких ионов используются окислительно-восстановительные реакции. Написать уравнение реакций.
9. В чем заключаются преимущества качественного анализа методом ТСХ (тонкослойной хроматографии)?
10. В чем заключается процесс хроматографирования?
11. Как производится идентификация веществ в методе ТСХ.
12. Что такое Rf, спосою расчета.
13. Какие сорбенты используются в методе ТСХ.
14. В чем заключается сущность метода качественного хроматографического обнаружения катионов металлов (Co2+, Ni2+, Cu2+, Fe3+ и др.)?
Литература
1. Основы аналитической химии. Практическое руководство (под ред. Ю.А. Золотова). М.: Высшая школа, 2006, 460 с.
2. Коренман Я.И. Практикум по аналитической химии. М.: Колос, 2005, 237с.
3. Коренман Я.И., Суханов П.Т. Задачник по аналитической химии. Воронеж: ВГТА, 2004, 339 с.
4. Цитович И.Е. Курс аналитической химии. - М.: Высшая школа, 1994, 495 с.
5. Васильев В.П. Аналитическая химия. - М.: высшая школа, 1989, Т. 1, 384 с.
6. Логинов Н.Я., Воскресенский А.Г., Солодкин И.С. Аналитическая химия. - М.: Просвещение, 1979,479 с.
7. Крешков А.П. Основы аналитической химии. - М.: Химия, 1970, 471 с.
8. Бончев П.Р. Введение в аналитическую химию. - Л.: Химия, 1978,496 с.
Глава 2.Теоретические основы химического анализа
Закон действующих масс
В современной редакции закон, установленный Гульдбергом и Вааге (1867 г.), можно сформулировать так:
Скорость 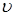 реакции
реакции
∑riRi → продукты
(где ri – стехиометрические коэффициенты, Ri – исходные вещества) пропорциональна произведению активностей исходных веществ в некоторых степенях:
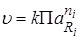 .
.
Данное выражение называется кинетическим уравнением.
k – коэффициент пропорциональности в кинетическом уравнении, называется константойскорости химической реакции;
a – активность, величина, которая будучи подставленной в уравнение для идеальных систем, позволяет рассчитать свойство для реальных систем.
Понятие активности было введено Lewis (1907), как эффективная, действующая, исправленная концентрация с:
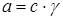 ,
,
где γ – коэффициент активности, который учитывает отклонения в свойствах реальных систем от идеальных, находят экспериментально или в справочнике. В разбавленных растворах при с→0 , γ→1, a=c. Для растворов сильных электролитов используют среднеионный коэффициент активности γ±.
В кинетическом уравнении ni – частный порядок реакции по Ri ‑ тому веществу; ni может принимать любые действительные значения; чаще ni ≠ ri ,
сумма частных порядков есть порядок реакции ∑ ni = n.
Скорость реакции по i-ому веществу υi есть число молей νi i-ого участника, претерпевающих изменение в единицу времени t в единице реакционного пространства V (объема или площади):
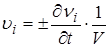 .
.
По определению υi >0, поэтому в формуле стоит + для продуктов реакции и − для исходных веществ. Скорость реакции в целом υ рассчитывают с учетом стехиометрических коэффициентов ri:
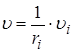 .
.
Если объем постоянный, то скорость реакции υi можно рассчитать как изменение концентрации в единицу времени:
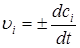 .
.
На практике имеют дело со средней скоростью 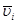 как изменением концентрации за реальное время t:
как изменением концентрации за реальное время t:
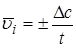 .
.
Химическое равновесие
На возможность двустороннего протекания химических превращений обратили внимание давно. Так, А.Лавуазье, установивший состав воздуха и воды, получил водород из воды (1783 г.), пропуская ее пары над раскаленным железом
3Fe + 4H2O 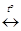 Fe3O4 + 4H2.
Fe3O4 + 4H2.
При той же температуре водород восстанавливает оксид до металла с образованием воды:
4H2 + Fe3O4 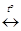 3Fe + 4H2O.
3Fe + 4H2O.
Наш соотечественник Н.Бекетов, изучая растворение мрамора в уксусной кислоте:
CaCO3 + 2CH3COOH ↔ Ca(CH3COO)2 + CO2↑ + H2O,
обнаружил, что при давлении CO2 равном 17 атмосферам растворение карбоната и выделение углекислого газа прекращается, а при Pco2 >17 атмосфер наблюдается выпадение осадка CaCO3.
Обратимые реакции используются и как аналитические, например:
KCl + NaHC4H4O6 ↔ KHC4H4O6↓ + HCl − открытие K+,
ZnCl2 + H2S ↔ ZnS↓ + 2HCl − открытие Zn2+,
2BaCl2 + K2Cr2O7 +H2O ↔ 2BaCrO4↓ + 2KCl +2HCl − открытие Ba2+,
AsO4 3− +2KJ + 2HCl ↔ AsO33− + J2 + 2KCl + H2O − восстановление As+5,
[CoCl4]2− + 6H2O ↔ [Co(H2O)6]2+ + 4Cl− − индикатор влажности.
Закон разбавления Оствальда
Рассмотрим ионизацию простейшего электролита, молекула которого состоит из одного катиона (С) и одного аниона (А). Пусть его степень ионизации αi, концентрация c:
CA ↔ C+ + A–.
При равновесии концентрации катионов и анионов равны с·αi, а недиссоциированных молекул с-с αi= с(1-αi), тогда выражение для константы ионизации Ki:
 или
или  .
.
Если в знаменателе можно пренебречь αi по сравнению с единицей, то получим:
Ki = с·αi2.
Так как по определению Ki есть величина постоянная, не зависящая от концентрации, увеличение с приводит к уменьшению αi и наоборот. В предельно разбавленном растворе (с→0) степень ионизации стремится к единице.
Понятия степень ионизации и константа ионизации применяются в основном к растворам слабых электролитов. Однако и для сильных электролитов αi как эффективная степень ионизации при концентрации с определяется в виде отношения:
α с =  ,
,
где λс – эквивалентная электропроводимость раствора при концентрации с;
λ0 − эквивалентная электропроводимость предельно разбавленного раствора, то есть при концентрации, стремящейся к нулю.
Константа ионизации (диссоциации – менее предпочтительное, устаревающее название) зависит от природы растворенного вещества и растворителя, от температуры. По значению Ki можно судить о силе слабого электролита, например, сила кислот уменьшается в ряду муравьиная > уксусная > фенол симбатно с уменьшением Ki:
HCOOH − 1,77·10-4; CH3COOH − 1,75·10-5; C6H5OH – 1,01·10-10.
Многоосновные кислоты и основания ионизируют ступенчато, причем константа ионизации следующей ступени, как правило, меньше предыдущей, например, для лимонной кислоты:
1 ступень C6H8O7 ↔ H+ + C6H7O7− , K1 = 7,45·10-4 ,
2 ступень C6H7O7 ↔ H+ + C6H6O72− , K2 = 1,73·10-5 ,
3 ступень C6H6O7 ↔ H+ + C6H5O73− , K3 = 4,02·10-6 .
Общая константа ионизации равна произведению констант отдельных ступеней
K = ∏Ki = K1·K2·K3·….
Ионное произведение воды
Вода – слабый электролит. Ее ионизация
Н2О ↔ ОН− + Н+
описывается константой
 .
.
Концентрация непроионизировавших (непродиссоциировавших) молекул воды практически не меняется при смещении равновесия, поэтому как постоянную величину ее можно объединить в виде произведения с Ki в новую константу Kw, называемую ионное произведение воды
 .
.
Kw не зависит от концентрации ионов ОН− или Н+. Их произведение при данной температуре есть величина постоянная, например, при 298 К Kw=1,008·10−14 (моль/л)2. Более удобно пользоваться величиной, полученной после логарифмирования, обозначив действие оператором pX=−lgX:

При равновесии [ОН−] = [Н+] =  = 10−7 моль/л, поэтому pOH = pH = 7 для нейтрального раствора. В кислом растворе [ОН−] < [Н+] и pH < 7 (например, pH = 3, pOH = 14–3 = 11). В щелочном растворе [ОН−] > [Н+] и pH > 7 (например, pH = 9, pOH = 14–9 = 5).
= 10−7 моль/л, поэтому pOH = pH = 7 для нейтрального раствора. В кислом растворе [ОН−] < [Н+] и pH < 7 (например, pH = 3, pOH = 14–3 = 11). В щелочном растворе [ОН−] > [Н+] и pH > 7 (например, pH = 9, pOH = 14–9 = 5).
Процесс ионизации воды сопровождается поглощением энергии в форме теплоты (∆Hi>0), поэтому при увеличении температуры Kw возрастает. Например, при 100о С pKw=12,23, то есть почти в 100 раз больше, чем при 25о С.
Гидролиз солей
Чистая вода имеет нейтральную реакцию, так как при ее ионизации:
HOH ↔ H+ + OH─
концентрации ионов H+ и OH– равны.
Опыт показывает, что водные растворы средних солей имеют кислую, щелочную или нейтральную реакции, хотя их молекулы не содержат ни ионов Н+, ни ионов ОН–. Это объясняется обратимым взаимодействием ионов соли с молекулами воды, сопровождающимся нарушением равновесия ионизации воды (изменением рН раствора), которое называется гидролизом соли. При этом образуется слабый электролит.
Гидролизу подвергаются соли, образованные при взаимодействии:
- слабой кислоты и сильного основания (CH3COONa);
- слабого основания и сильной кислоты (NH4Cl);
- слабой кислоты и слабого основания (CH3COONH4).
Рассмотрим первый случай.
Ацетат натрия CH3COONa в воде полностью диссоциирует на ионы, т.к. является сильным электролитом. Ионное уравнение гидролиза:
CH3COO–+ Na+ + HOH ↔ CH3COOH + Na+ + OH–
показывает, что образуется уксусная кислота ‑ слабый электролит, то есть ионы H+ связываются ионами CH3COO–. Ионов OH– в р-ре становится больше, чем Н+ ‑ р-р имеет щелочную реакцию (pH>7). Говорят, что имеет место гидролиз по аниону.
Во втором случае раствор NH4Cl имеет кислую реакцию (pH<7), т.к. ионы OH– связываются катионами NH4+ с образованием слабого электролита NH3·H2O. Это пример гидролиза по катиону, при котором концентрация Н+ становится больше, чем концентрация гидроксил ионов.
В третьем случае происходит гидролиз и по катиону, и по аниону. Значение pH раствора зависит от соотношения сил слабой кислоты и слабого основания.
Хлорид натрия NaCl не подвергается гидролизу, раствор имеет нейтральную реакцию (pH=7), ионы H+ и OH– не связываются, так как NaOH и HCl– сильные электролиты.
Na+ + Cl– + HOH ↔ Na+ + OH– + H+ + Cl–.
Ступенчатый гидролиз
Ступенчатому гидролизу подвергаются соли, образованные многоосновными слабыми кислотами или многоосновными слабыми основаниями.
Гидролиз по аниону (pH>7).
Na2CO3 + HOH ↔NaHCO3+ NaOH – первая ступень,
NaHCO3+ HOH ↔ H2CO3 + NaOH – вторая ступень.
Гидролиз по катиону (pH<7).
AlCl3 + HOH ↔ AlOHCl2 + HCl – первая ступень,
АlOHCl2 +H2O ↔ Al(OH)2Cl + HCl – вторая ступень,
Al(OH)2Cl + HOH ↔ Al(OH)3 + HCl – третья ступень (очень мало).
Гидролиз – как правило, обратимый процесс не идущий до конца.
Необратимый гидролиз – если продукты уходят из реакции (↓и↑).
Al2S3 + 6H2O = 2Al(OH)3↓+3H2S↑
Обратной гидролизу является реакция нейтрализации
CH3COO– + HOH ↔ CH3COOH+ OH–.
Подавление и усиление гидролиза
Для усиления гидролиза соли, гидролизующейся по катиону, необходимо добавить основание для связывали ионов Н+
Кt+ + HOH ↔ KtOH +H+
При добавлении кислоты в этом случае гидролиз подавляется. Принцип управления гидролизом соли, образованной слабой кислотой, аналогичен:
An– + HOH ↔ AnH + OH–.
Для усиления – добавляют кислоту, для уменьшения – основание. Катионы водорода можно связать в кислые анионы (HCO–3) или в нейтральные молекулы слабых кислот (H2CO3), действуя на растворы солями сильных оснований слабых кислот, например, Na2CO3 .Анионы можно связывать в комплексные ионы, например,
[Co(OH)]+ , [Al(OH)2]+ .
Применение гидролиза
1. Необратимый гидролиз Al2S3, Cr2S3, TiS2 приводит к образованию осадков соответствующих гидроксидов Al(OH)3 , Cr(OH)3, Ti(OH)4.
2. Характерные реакции открытия катионов и анионов, например, Be, Bi, Sb. Так в результате гидролиза Bi3+ образуется белый осадок хлористого висмутила
BiCl3 +2HOH ↔ Bi(OH)2Cl+2HCl и далее
Bi(OH)2Cl ↔ BiOCl↓+H2O.
Буферные системы
Buffer в буквальном переводе означает нечто, что уменьшает воздействие на систему внешней силы. В отношении растворов − это системы, способные сохранять, примерно, постоянную концентрацию ионов H+ при добавлении небольших количеств кислоты или щелочи, а также при разбавлении.
Такими буферирующими свойствами обладают смеси:
1. Cлабая кислота + ee соль сильного основания, например,
СН3СООН + СН3СООNa − ацетатный буфер (рН ~ 5);
2. Слабое основание + его соль сильной кислоты, например,
NH3 . H2O + NH4Cl − аммиачный буфер (рН ~ 9);
3. Смесь двух кислых разнозамещенных солей многоосновной кислоты, например, Na2HPO4 + KH2PO4 − фосфатный буфер (рН ~ 7);
4. Индивидуальная соль, например,
Na2B4O7 . 10H2O, рН~9;
5. Концентрированные растворы сильных кислот и щелочей.
Рассмотрим более подробно ацетатный буфер: уксусная кислота – слабый электпролит, ацетат натрия (соль) – сильный электролит.
СН3СООН ↔ СН3СОО− + Н+,
СН3СООNa → СН3СОО− + Na+.
Напишем выражение для константы ионизации слабой кислоты Kia и учтем, что в смеси концентрация ацетат аниона практически равна концентрации соли сs, а концентрация непроионизировавших молекул – концентрации кислоты ca
 .
.
Выразим [H+] и pH:
