Гидриды металлов и их свойства
Неорганическая химия
Совместный гидролиз солей
Например:
Задача 1.1. Что получится при сливании водных растворов хлорида алюминия и сульфида натрия (напишите уравнение реакции)?
Задача 1.2. Что получится при сливании водных растворов хлорида железа (III) и карбоната натрия (напишите уравнение реакции)?
Ответы внизу
Совместный гидролиз часто встречается в задачах С2, где его не так-то просто обнаружить. Вот пример:
Задача 1.3. Порошок металлического алюминия смешали с твердым иодом и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдали выпадение осадка. Напишите уравнения четырех описанных реакций.
Ответы внизу
Реакции оксидов с водой
Вопрос: Когда оксиды реагируют с водой?
Ответ: с водой реагируют только солеобразующие оксиды и только если получается растворимый гидроксид.
Например:
Задача 2.1. Запишите уравнения осуществимых реакций:
NO + H2O =
BaO + H2O =
CrO + H2O =
SO2 + H2O =
SiO2 + H2O =
Mn2O7 + H2O =
NO2 + H2O =
Ответы внизу
Гидриды металлов и их свойства
Водород способен реагировать с активными металлами (преимущественно стоящими до алюминия в ряду активности металлов, то есть это щелочные и щелочно-земельные металлы). При этом образуются гидриды, например: LiH, CaH2.
В гидридах степень окисления водорода равна -1!
Гидриды – это бинарные соединения, а потому способны гидролизоваться.
Задача 3.1 Запишите уравнения гидролиза гидрида натрия, гидрида магния.
Ответы внизу
Щелочной или кислотный гидролиз бинарных соединений
Для школьного курса – экзотическая вещь, но вот в ЕГЭ-2014 встретилось… Речь идет о таких, например, реакциях:
PCl5 + NaOH =
Ca3N2 + HCl =
Здесь можно рассуждать так. Щелочь (NaOH) или кислота (HCl) реагируют с бинарным соединением в растворе. А это значит, что фактически сначала идет реакция с водой (гидролиз бинарного соединения):
PCl5 + H2O → H3PO4 + HCl
Ca3N2 + H2O → Сa(OH)2 + NH3
А затем продукты гидролиза реагируют с щелочью (в первом случае) или с кислотой (во втором случае):
PCl5 + H2O → H3PO4 + HCl → (+NaOH) → Na3PO4 + NaCl + H2O
Ca3N2 + H2O → Сa(OH)2 + NH3 → (+HCl) → CaCl2 + NH4Cl + (H2O)
В итоге уравнения будут выглядеть так:
PCl5 + 8NaOH = Na3PO4 + 5NaCl +4 H2O
Ca3N2 + 8HCl = 3CaCl2 + 2NH4Cl
Поупражняйтесь:
Задача 3.2 Рассуждая аналогично, определите, что получится при взаимодействии:
Na3N + HCl →
PBr3 + NaOH →
Ответы внизу
Аммиак и его свойства
Аммиак реагирует с кислотами, присоединяя протон по донорно-акцепторному механизму и образуя при этом соли аммония.
Задача 4.1. Через раствор серной кислоты пропустили аммиак. Какие две соли при этом могут образоваться? От чего это зависит? Напишите уравнения реакций.
Ответы внизу
Водный раствор аммиака обладает свойствами слабой щелочи, поэтому с его помощью можно осаждать нерастворимые гидроксиды металлов.
Задача 4.2. Через водный раствор сульфата хрома (III) пропустили избыток аммиака. Запишите уравнение реакции.
Ответы внизу
3) Аммиак – восстановитель. В частности, способен восстанавливать металлы из оксидов.
Задача 4.3. Через оксид меди (II) пропустили поток аммиака при нагревании. Напишите уравнение реакции.
Ответы внизу
4) Аммиак способен быть лигандом и может образовывать комплексы – аммиакаты. Особенно вероятно упоминание в ЕГЭ аммиачного комплекса меди, так как он имеет ярко-синее окрашивание и может использоваться для обнаружения соединений двухвалентной меди.
Задача 4.4. К раствору сульфата меди (II) добавили избыток водного раствора аммиака. Запишите уравнение реакции.
Ответы внизу
Вообще с наибольшей скоростью идут те реакции, которые сопровождаются взрывами. А при обычных условиях – реакции ионного обмена в водных растворах. Почему? Потому что в них участвуют электролиты, которые уже диссоциированы, связи разрушены. Поэтому ничто не мешает ионам моментально соединиться между собой. Можно считать, что активационный барьер такой реакции приближается к нулю.
Например:
Какие вещества реагируют между собой с наибольшей скоростью при комнатной температуре:
1) HCl(p-p) и NaOH(p-p)
2) S(тв.) и H2(г)
3) CO2(г) и H2O(ж)
4) FeS2(тв.) и O2(г)
Правильный ответ – 1), так как это реакция ионного обмена.
Смешанные оксиды Fe3O4 и Pb3O4
Железо образует смешанный оксид – железную окалину Fe3O4 (FeO ∙ Fe2O3) со степенями окисления +2 и +3.
Свинец образует смешанный оксид – сурик Pb3O4 (2PbO ∙ PbO2) со степенями окисления +2 и +4.
При реакциях этих оксидов с кислотами могут получаться сразу две соли:
Fe3O4 + 8HCl = FeCl2 + 2FeCl3 + 4H2O
Pb3O4 + 4HNO3 = 2Pb(NO3)2 + PbO2 + H2O (PbO2 амфотерен, поэтому в соль не превращается).
Переходы Fe+2 ↔ Fe+3 и Cu+1 ↔ Cu+2
Вот несколько сложных ситуаций:
Fe3O4 + HNO3 = что получится?
Казалось бы, должны получиться две соли и вода: Fe(NO3)2 + Fe(NO3)3 + H2O (смотри предыдущий раздел), но HNO3 – сильный окислитель, поэтому будет окислять железо +2 в составе железной окалины до железа +3 и получится только одна соль:
Fe3O4 + 10HNO3 (конц) = 3Fe(NO3)3 + NO2 + 5H2O
Аналогично в реакции Cu2O + HNO3 может показаться, что продуктами будут CuNO3 + H2O. А на самом деле одновалентная медь (Cu+12O) может окисляться до двухвалентной, поэтому пойдет окислительно-восстановительная реакция:
Cu2O + 6HNO3 (конц) = 2Сu(NO3)2 + 2NO2 + 3H2O
Задача 7.1. Запишите уравнения реакций:
Fe3O4 + H2SO4 (разб) =
Fe3O4 + H2SO4 (конц) =
Fe2(SO4)3 + H2S =
Ответы внизу
Разложение нитратов
В целом разложение нитратов происходит согласно известной схеме, и состав продуктов зависит от расположения металла в ряду активности. Но есть сложные ситуации:
Задача 9.1 Какие продукты получатся при разложении нитрата железа (II)? Запишите уравнение реакции.
Задача 9.2 Какие продукты получатся при разложении нитрата меди (II)? Запишите уравнение реакции.
Ответы внизу
Органическая химия
Тривиальные названия
Надо знать, какие органические вещества соответствуют названиям:
изопрен, дивинил, винилацетилен, толуол, ксилол, стирол, кумол, этиленгликоль, глицерин, формальдегид, уксусный альдегид, пропионовый альдегид, ацетон, первые шесть предельных одноосновных кислот (муравьиная, уксусная, пропионовая, масляная, валериановая, капроновая), акриловая кислота, стеариновая кислота, пальмитиновая кислота, олеиновая кислота, линолевая кислота, щавелевая кислота, бензойная кислота, анилин, глицин, аланин. Не путайте пропионовую кислоту с пропеновой!! Соли важнейших кислот: муравьиной – формиаты, уксусной – ацетаты, пропионовой – пропионаты, масляной – бутираты, щавелевой – оксалаты. Радикал –CH=CH2 называется винил!!
Заодно и некоторые неорганические тривиальные названия:
Поваренная соль (NaCl), негашеная известь (CaO), гашеная известь (Ca(OH)2), известковая вода (раствор Ca(OH)2), известняк (CaCO3), кварц (он же кремнезем или диоксид кремния – SiO2), углекислый газ (CO2), угарный газ (CO), сернистый газ (SO2), бурый газ (NO2), питьевая или пищевая сода (NaHCO3), кальцинированная сода (Na2CO3), аммиак (NH3), фосфин (PH3), силан (SiH4), пирит (FeS2), олеум (раствор SO3 в концентрированной H2SO4), медный купорос (CuSO4∙5H2O).
Некоторые редкие реакции
1) Образование винилацетилена:
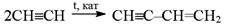
Винилацетилен далее способен вступать в реакции присоединения и, в частности. Является сырьем для получения хлоропрена, из которого делают хлоропреновый каучук:
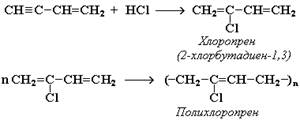
2) Реакция прямого окисления этилена в уксусный альдегид:

Эта реакция коварна тем, что мы хорошо знаем, как ацетилен превращается в альдегид (реакция Кучерова), а если в цепочке встретится превращение этилен → альдегид, то это может нас поставить в тупик. Так вот, имеется в виду эта реакция!
3) Реакция прямого окисления бутана в уксусную кислоту:
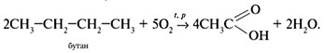
Эта реакция лежит в основе промышленного производства уксусной кислоты.
4) Реакция Лебедева:
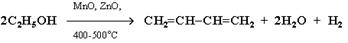
Отличия фенолов от спиртов
Огромное количество ошибок в таких заданиях!!
1) Следует помнить, что фенолы более кислотны, чем спирты (связь О-Н в них более полярна). Поэтому спирты не реагируют с щелочью, а фенолы реагируют и с щелочью, и некоторыми солями (карбонаты, гидрокарбонаты).
Например:
Задача 10.1
Какие из этих веществ реагируют с литием:
а) этиленгликоль, б) метанол, в) фенол, г) кумол, д) глицерин.
Задача 10.2
Какие из этих веществ реагируют с гидроксидом калия:
а) этиленгликоль, б) стирол, в) фенол, г) этанол, д) глицерин.
Задача 10.3
Какие из этих веществ реагируют с гидрокарбонатом цезия:
а) этиленгликоль, б) толуол, в) пропанол-1, г) фенол, д) глицерин.
2) Следует помнить, что спирты реагируют с галогеноводородами (эта реакция идет по связи С-О), а фенолы нет (в них связь С-О из-за эффекта сопряжения малоподвижна).
Дисахариды
Основные дисахариды: сахароза, лактоза и мальтоза имеют одинаковую формулу C12H22O11.
О них следует помнить:
1) что они способны гидролизоваться на те моносахариды, из которых состоят: сахароза – на глюкозу и фруктозу, лактоза – на глюкозу и галактозу, мальтоза – на две глюкозы.
2) что лактоза и мальтоза обладают альдегидной функцией, то есть являются восстанавливающими сахарами (в частности, дают реакции «серебряного» и «медного» зеркала), а сахароза – невосстанавливающий дисахарид, не имеет альдегидной функции.
Механизмы реакций
Будем надеяться, что достаточно следующих знаний:
1) для алканов (в том числе в боковых цепях аренов, если эти цепи предельные) характерны реакции свободнорадикального замещения (с галогенами), которые идут по радикальному механизму (инициирование цепи – образование свободных радикалов, развитие цепи, обрыв цепи на стенках сосуда или при соударении радикалов);
2) для алкенов, алкинов, аренов характерны реакции электрофильного присоединения, которые идут по ионному механизму (через образование пи-комплекса и карбокатиона).
Особенности бензола
1. Бензол в отличие от других аренов не окисляется перманганатом калия.
2. Бензол и его гомологи способны вступать в реакцию присоединения с водородом. Но только бензол способен также вступать в реакцию присоединения с хлором (только бензол и только с хлором!). При этом все арены способны вступать в реакцию замещения с галогенами.
Реакция Зинина
Восстановление нитробензола (или аналогичных ему соединений) в анилин (или другие ароматические амины). Эта реакция в одном из ее видов почти обязательно встретится!
Вариант 1 – восстановление молекулярным водородом:
C6H5NO2 + 3H2 → C6H5NH2 +2H2O
Вариант 2 – восстановление водородом, полученным при реакции железа (цинка) с соляной кислотой:
C6H5NO2 + 3Fe + 7HCl → C6H5NH3Cl +3FeCl2 + 2H2O
Вариант 3 – восстановление водородом, полученным при реакции алюминия с щелочью:
C6H5NO2 + 2Al + 2NaOH + 4H2O → C6H5NH2 +2Na[Al(OH)4]
Свойства аминов
Почему-то свойства аминов запоминаются хуже всего. Возможно, это связано с тем, что амины изучаются в курсе органической химии последними, и их свойства не удается повторить, изучая другие классы веществ. Поэтому рецепт такой: просто выучить все свойства аминов, аминокислот и белков.
Разложение ацетатов
Почему-то составители ЕГЭ считают, что нужно знать, как разлагаются ацетаты. Хотя в учебниках этой реакции нет. Разные ацетаты разлагаются по-разному, но давайте запомним реакцию, которая попадается в ЕГЭ:
при термическом разложении ацетата бария (кальция) получается карбонат бария (кальция) и ацетон!!!
Ba(CH3COO)2 → BaCO3 + (CH3)2CO (t0)
Ca(CH3COO)2 → CaCO3 + (CH3)2CO (t0)
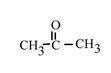
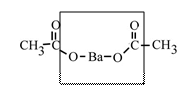 По сути, при этом происходит декарбоксилирование:
По сути, при этом происходит декарбоксилирование:
→ BaCO3 +
Ответы:
1.1. При совместном гидролизе солей, одна из которых гидролизуется по катиону, а другая – по аниону, гидролиз взаимно усиливается и идет до образования конечный продуктов гидролиза обеих солей: 2AlCl3 + 3Na2S + 6H2O = 2Al(OH)3↓ + 3H2S↑ + 6NaCl
1.2. Аналогично: 2FeCl3 + 3Na2CO3 + 3H2O = 2Fe(OH)3↓ + 3CO2↑ + 6NaCl
1.3. Последовательность реакций:
2Al + 3I2 = 2AlI3
AlI3 + 3NaOH = Al(OH)3 + 3NaI
Al(OH)3 + 3HCl = AlCl3 + 3H2O
2AlCl3 + 3Na2CO3 + 3H2O = 2Al(OH)3 +3CO2 + 6NaCl
2.1.
NO + H2O = не реагируют (так как несолеобразующий оксид)
BaO + H2O = Ba(OH)2 (реагируют, так как получается растворимый гидроксид)
CrO + H2O = (не реагируют, так как гидроксид хрома (II) нерастворим)
SO2 + H2O = H2SO3 (реагируют, так как получается растворимый гидроксид)
SiO2 + H2O = (не реагируют, так как гидроксид кремния (IV), то есть кремниевая кислота - нерастворима)
Mn2O7 + H2O = 2HMnO4 (реагируют, так как получается растворимый гидроксид – марганцевая кислота)
2NO2 + H2O = HNO2 + HNO3
3.1. При гидролизе бинарных соединений получается гидроксид первого элемента и водородное соединение второго элемента. В случае гидрида вторым продуктом будет просто водород:
NaH + H2O = NaOH + H2↑
MgH2 + 2H2O = Mg(OH)2 + 2H2↑
3.2
Na3N + 4HCl → 3NaCl + NH4Cl
PBr3 + 6NaOH → Na3PO3 + 3NaBr + 3H2O
4.1 При пропускании аммиака через растворы многоосновных кислот могут получаться средние или кислые соли, в зависимости от того, какой из реагентов в избытке:
NH3 + H2SO4 = NH4HSO4 (кислота в избытке)
2NH3 + H2SO4 = 2 (NH4)2SO4 (аммиак в избытке)
4.2
Cr2(SO4)3 + 6NH3 + 6H2O = 2Cr(OH)3↓ + 3(NH4)2SO4
(Фактически это та же реакция, что и:
Cr2(SO4)3 + 6NH4OН = 2Cr(OH)3↓ + 3(NH4)2SO4,
но формулу NH4OН сейчас писать не принято).
4.3
3CuO + 2NH3 = 3Cu + N2 + 3H2O
4.4
CuSO4 + 4NH3 = [Cu(NH3)4 ]SO4
(Хотя на самом деле сначала пойдет такая реакция:
CuSO4 + 2NH3 + 2H2O = Cu(OH)2↓ + (NH4)2SO4 (так как аммиак действует как щелочь)
А потом: Cu(OH)2↓ + 4NH3 = [Cu(NH3)4](OH)2)
В общем, в любом случае при достаточном количестве аммиака получится комплекс и ярко-синее окрашивание!
5.1
K3[Al(OH)6] + 6HBr = 3KBr + AlBr3 + 6H2O
K3[Al(OH)6] + 3HBr = 3KBr + Al(OH)3↓ + 3H2O
Na2[Zn(OH)4] + 2CO2 = 2NaHCO3 + Zn(OH)2↓
K[Al(OH)4] = KAlO2 + 2H2O↑ (t0)
[Ag(NH3)2]Cl + 2HNO3 = 2NH4NO3 + AgCl↓
6.1
2СuSO4 + 4KI = 2CuI + I2 + 2K2SO4 (двухвалентная медь восстанавливается до одновалентной)
Fe2O3 + 6HI = 2FeI2 + I2 + 3H2O
KNO2 + NH4I = KI + N2 + 2H2O
H2O2 + 2KI = I2 + 2KOH
7.1
Fe3O4 + 4H2SO4 (разб) = FeSO4 + Fe2(SO4)3 + 4H2O
так как разбавленная серная кислота не является сильным окислителем, то идет обычная обменная реакция.
2Fe3O4 + 10H2SO4 (конц) = 3Fe2(SO4)3 + SO2 + 10H2O
так как концентрированная серная кислота является сильным окислителем, то железо +2 окисляется до железа +3.
Fe2(SO4)3 + H2S = 2FeSO4 + S + H2SO4
так как сероводород является восстановителем, то железо +3 восстанавливается до железа +2.
8.1
NaHSO4 + NaOH = Na2SO4 + H2O
Na2SO4 + NaOH – не реагируют
NaHSO4 + Ba(OH)2 = BaSO4 + NaOH + H2O
Na2SO4 + Ba(OH)2 = BaSO4 + 2NaOH
8.2
Сu + 2H2SO4 (конц) = CuSO4 + SO2 + 2H2O
CuO + H2SO4 = CuSO4 + H2O
8.3
Сu + HCl – не реагируют
CuO + 2HCl = CuCl2 + H2O
8.4
ZnS + 2HCl = ZnCl2 + H2S↑
ZnO + 2HCl = ZnCl2 + H2O
8.5
Cu2O + 3H2SO4 = 2CuSO4 + SO2 + 3H2O (тут дело в том, что, поскольку кислота концентрированная, то она доокисляпет Cu+1 до Cu+2.
CuO + H2SO4 = CuSO4 + H2O
9.1
Казалось бы, при разложении нитрата железа (II) должны получиться оксид железа (II), оксид азота (IV) и кислород. Но хитрость в том, что поскольку в оксиде железа (II) железо имеет не высшую степень окисления, а в реакции выделяется кислород, то железо будет окисляться до +3 и получится оксид железа (III):
Fe(NO3)2 → Fe2O3 + NO2 + O2
В этой реакции сразу два восстановителя – железо и кислород. С коэффициентами будет так:
4Fe(NO3)2 = 2Fe2O3 + 8NO2 + O2
9.2
В этой реакции ничего особенного нет, кроме того, что часто забывают, что медь относится еще к тем металлам, при разложении которых получается оксид металла, а не сам металл:
2Cu(NO3)2 = 2CuO + 4NO2 + O2
А вот все металлы, которые за медью, при разложении своих нитратов будут давать уже просто металл.
10.1
Правильные ответы: а,б,в,д (в кумоле вообще нет гидроксильной группы, это арен).
10.2
Правильные ответы: в (в стироле вообще нет гидроксильной группы, это арен).
10.3
Правильные ответы: нет правильного ответа (в толуоле вообще нет гидроксильной группы, это арен. Фенол недостаточно кислотный. Могла бы реагировать какая-нибудь карбоновая кислота.).
Неорганическая химия
Совместный гидролиз солей
Например:
Задача 1.1. Что получится при сливании водных растворов хлорида алюминия и сульфида натрия (напишите уравнение реакции)?
Задача 1.2. Что получится при сливании водных растворов хлорида железа (III) и карбоната натрия (напишите уравнение реакции)?
Ответы внизу
Совместный гидролиз часто встречается в задачах С2, где его не так-то просто обнаружить. Вот пример:
Задача 1.3. Порошок металлического алюминия смешали с твердым иодом и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка. Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдали выпадение осадка. Напишите уравнения четырех описанных реакций.
Ответы внизу
Реакции оксидов с водой
Вопрос: Когда оксиды реагируют с водой?
Ответ: с водой реагируют только солеобразующие оксиды и только если получается растворимый гидроксид.
Например:
Задача 2.1. Запишите уравнения осуществимых реакций:
NO + H2O =
BaO + H2O =
CrO + H2O =
SO2 + H2O =
SiO2 + H2O =
Mn2O7 + H2O =
NO2 + H2O =
Ответы внизу
Гидриды металлов и их свойства
Водород способен реагировать с активными металлами (преимущественно стоящими до алюминия в ряду активности металлов, то есть это щелочные и щелочно-земельные металлы). При этом образуются гидриды, например: LiH, CaH2.
В гидридах степень окисления водорода равна -1!
Гидриды – это бинарные соединения, а потому способны гидролизоваться.
Задача 3.1 Запишите уравнения гидролиза гидрида натрия, гидрида магния.
Ответы внизу
