Масса газа, полученного взаимодействием 16 г серы с 22,4 л (н.у.) кислорода
А) 32 г
B) 30 г
C) 34 г
D) 36 г
E) 38 г
150.Пара веществ, которая реагирует с раствором серной кислоты:
A) Карбонат калия и азот
B) Магний и оксид кальция
C) Гидроксид цинка и соляная кислота
D) Цинк и оксид углерода (IV)
E) Оксид меди и серебро
151.Газ аммиак может быть обнаружен:
A) По запаху
B) По покраснению универсальной индикаторной бумаги
C) По покраснению лакмуса фиолетового
D) По обесцвечиванию кристаллов хлорида меди(II)
E) По помутнению известковой воды
152.В лабораторных условиях оксид углерода (IV) получают:
A) CH4 + O2→
B) CaCO3 + HCl→
C) CO + O2→
D) CuO + C→
E) CaO + C→
Молярная масса газа(г/моль), если его плотность по водороду равна 14
А) 28
B) 58
C) 29
D) 9
E) 14
154.Для определения ионов галогенов в водном растворе используют
A) Al3+
B) Ca2+
C) Ag+
D) Cu2+
E) K+
155.Совместно в растворе может находиться пара веществ:
A) Zn, HCl
B) ZnO, H2SO4
C) NaOH, KOH
D) Fe(OH)2, HNO3
E) Mg, HNO3
CaО не взаимодействует с
А) S
B) HCl
C) KC l
D) H2O
E) H2SO4
157.Не является физическим свойством алюминия
А) Плохо проводит тепло
B) Легкий (плотность= 2,7г/см3)
C) Серебристо-белый
D) Ковкий, пластичный
E) Электропроводный
158.Масса цинка, необходимая для вытеснения 11,2л водорода из соляной кислоты
A) 32, 5 г
B) 33, 7 г.
C) 21 г.
D) 25 г.
E) 22, 5 г.
Вещество Б в цепи превращений
Ca 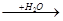 А
А  CaCO3
CaCO3 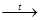 Б
Б
А) CaO
B) H2CO3
C) CaC2
D) Ca(OH)2
E) H2O
Общая формула RO характерна для оксида
А) Кальция
В) Водорода
С) Натрия
D) Серы
Е) Фосфор
Запись, обозначающая три молекулы водорода
A) 3H2.
B) 2H3.
C) 3H3.
D) 3H.
E) 2H.
Реакция разложения - это
A) 2KClO3 = 2KCl + 3O2
B) 2H2 +O2 =2 H2O C) S + O2 = SO2
D) Fe + CuSO4 = FeSO4 + Cu
E) Ca +2 HCl = CаCl2 + H2
163.Сумма коэффициентов в уравнении реакции соединения P2O5 + K2O = K3PO4
A) 6
B) 5
C) 7
D) 8
E) 9
164.В данном перечне оксидов атомы всех элементов имеют валентность, равную одному
A) K2O, H2O, N2O.
B) Fe2O3, Al2O3, P2O3.
C) N2O3, P2O5 CaO,.
D) Al2O3, N2O3, K2O.
E) CaO, N2O3, P2O3.
165.Порция 1,5 . 1023 молекул диоксида углерода соответствует количеству вещества
A) 0, 5 моль.
B) 1 моль.
C) 0, 25 моль.
D) 0, 75 моль.
E) 1, 5 моль.
Массовая доля кислорода в сульфате меди (II)
A)40%
B) 12%
C) 48%
D) 50%
E) 40%
Кислород – химический элемент в утверждении
A) Кислород поддерживает горение
B) Рыбы дышат растворенным в воде кислородом.
C) Воздух содержит 21% кислорода по объему
D) Газ кислород тяжелее воздуха.
E) В состав озона входит кислород.
Диоксид серы взаимодействует с водой и образует
A) Сернистую кислоту.
B) Триоксид серы.
C) Серную кислоту.
D) Сероводородную кислоту.
E) Серу.
Валентность кислотного остатка не равна двум
A) Сероводородной кислоты.
B) Сернистой кислоты.
C) Серной кислоты.
D) Угольной кислоты.
E) Соляной кислоты.
170.Сумма коэффициентов в уравнении реакции получения сульфата алюминия реакцией нейтрализации равна
A) 12.
B) 6.
C) 8.
D) 10.
E) 9.
Щелочь среди оснований - это
A) Гидроксид натрия
B) Гидроксид цинка
C) Гидроксид железа (II)
D) Гидроксид железа (III)
E) Гидроксид меди(II)
Атому элемента фосфора отвечает электронная формула
A) 1s22s22p63s23p3
B) 1s22s22p63s23p2
C) 1s22s22p63s23p1
D) 1s22s22p63s23p4
E) 1s22s22p63s23p5
