Вода образуется в результате реакции
A) Разложения гидроксида алюминия.
B) Взаимодействия алюминия с соляной кислотой.
C) Взаимодействия водорода с азотом в определенных условиях.
D) Окисления меди.
E) Горения серы.
Максимальное число электронов на р – подуровне равно
A) 6.
B) 2.
C) 10.
D) 14
E) 18.
113.Среди элементов первой группы наиболее ярко выражен металлический характер у:
A) Цезия.
B) Натрия.
C) Калия.
D) Лития.
E) Франция.
Электроотрицательность элементов возрастает в ряду
A) Si-P-S-Cl
B) P-As-Sb-Bi
C) O-N-C-B
D) Si-Al-Mg-Na
E) Cr-Se-Mo-Te
Восстановитель среди окислителей - это
A) S-2
B) Mn+7
C) S+6
D) N+5
E) Cr+6
116. Летучее водородное соединение RH4 характерно для
A) Углерода
B) Бария
C)Азота.
D) Фосфора
E) Хлора
Сумма всех коэффициентов в ионном сокращенном уравнении реакции
Ba(OH)2 + HNO3 =
А) 6
B) 8
C) 10
D) 9
E) 14
Относительная плотность оксида серы (IV) по водороду
А) 32
B) 10
С) 12
D) 14
E) 8
119.При сгорании 16г серы в 11,2 л кислорода образуется сернистый газ количеством вещества
A) 0,5 моль
B) 1 моль
C) 1,5 моль
D) 2 моль
E) 2,5
120.Кислые соли серной кислоты называют:
A) Гидросульфатами
B) Гидросульфитами
C) Гидроксосульфатами
D) Гидросульфидами
E) Сульфатами
К физическим свойствам аммиака не относится
A) Хорошо растворим в воде
B) С резким специфическим запахом
C) Жидкость
D) Легче воздуха
E) Бесцветный
122.Массовая доля кислорода в оксиде серы (IV) SO2
A) 50%
B) 12%
C) 48%
D) 40%
E) 60%
Молярная масса газа(г/моль), если его плотность по воздуху равна 2
А) 4
B) 58
C) 29
D) 9
E) 14
Хлор не может вступать в реакцию c
A) H2O
B) HF
C) HBr
D) HI
E) NaOH
125.Совместно в растворе может находиться пара веществ:
A) HCl, CaO
B) NaOH, Ca(OH)2
C) SO3, KOH
D) LiOH, CO2
E) BaO, SO2
126.Ca(OH)2 взаимодействует с
А) BaSO4
В) CuO
С) H2SO4
Д) Na2O
Е) Cu(OH)2
Амфотерность алюминия проявляется при взаимодействии с
А) NaOH, HCl
B) NaOH, KOH
C) HCl, H2SO4
D) NaOH, H2O
E) H2O, CaO
128.Объем водорода, необходимый для получения 5,6 л газа хлороводорода (н.у.), составляет
A) 5, 6 л.
B) 3 л.
C) 3, 4 л.
D) 2, 8 л.
E) 5, 8л.
Вещество Х в цепи превращений
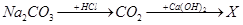
А) CaCO3
B) CO
C) СaO
D)CaC2
E) H2CO3
130. Формула летучего водородного соединения RH3 характерна для
A) Фософра
B) Серы
C) Углерода
D) Хлора
E) иод
131.Не относится к химическому явлению:
A) Таяние снега.
B) Сжигание угля.
C) Разложение воды под действием электрического тока.
D) Обесцвечивание цветных тканей в хлорной воде.
E) Образование коричневой корочки на хлебе при выпечке.
Реакция соединения - это
A) 2H2 +O2 =2H2O
B) 2H2O = 2H2 + O2
C) 2KClO3 = 2KCl + 3O2
D) Ca +2HCl = CaCl2 + H2
E) CаCO3 = CaO + CO2
133.Сумма коэффициентов в уравнении реакции разложения NaNO3 = NaNO2 + O2
A) 5
B) 6
C) 7
D) 8
E) 9
134.В данном перечне оксидов атомы всех
элементов имеют валентность, равную двум
A) CaO, NO, MgO
B) Fe2O3, Al2O3, P2O3.
C) K2O, CaO, Fe2O3.
D) Al2O3, N2O3, K2O.
E) N2O3, P2O5, H2O.
135.Число молекул в 0,1 моль углекислого газа CO2
A) 6 . 1023.
B) 6 . 1022.
C) 1, 2 . 1023.
D) 1, 2 . 1022.
E) 0, 6 . 1022.
136.Массовая доля кислорода в оксиде серы (IV) SO2
A) 50%
B) 12%
C) 48%
D) 40%
E) 60%
Химический элемент кислород имеет аллотропных видоизменений
A) 2.
B) 1.
C) 3.
D) 4.
E) 5.
Реагирует при н.у.с водой оксид
A) Кальция..
B) Меди.
C) Серебра.
D) Алюминия
E) Свинца.
Кислоты можно получить в результате взаимодействия
A) Кислотного оксида и воды.
B) Основного и кислотного оксида.
C) Основания с кислотным оксидом.
D) Соли и основания.
E) Двух солей.
140.Сумма коэффициентов в уравнении реакции образования ортофосфата калия из оксида фосфора (V) и оксида калия равна:
A) 6.
B) 3.
C) 4.
D) 7.
E) 2.
141.Раствор, в котором данное вещество при данной температуре больше не растворяется, называют
A) Очень концентрированным
B) Пересыщенным
C) Концентрированным
D) Разбавленным
E) Насыщенным
Элемент стронций относится
A) s-элементам
B) р-элементам.
C) d-элементам
D) f-элементам
E) h-элементам
143.Среди элементов шестой группы наиболее ярко выражен неметаллический характер у
A) Кислорода.
B) Серы.
C) Селена.
D) Теллура.
E) Полония.
Ионную кристаллическую решетку имеет
A) Алмаз.
B) Вода.
C) Поваренная соль.
D) Медь.
E) Аммиак.
Окислитель среди восстановителей - это
A) S-2
B) N-3
C) H-1
D) Cl-1
E) N+5
146. Формула летучего водородного соединения RH2 характерна для
A) Серы
B) Фосфора
C) Углерода
D) Хлора
E) иод
147.Сумма всех коэффициентов в ионном сокращенном уравнении реакцииNaOH + H2SO4 =
А) 10
B) 8
C) 9
D) 6
E) 12
146. Формула летучего водородного соединения RH4 характерна для
A) Углерода
B) Фосфора
C) Серы
D) Хлора
E) иод
