Вызванные потенциалы и потенциалы, связанные с событиями
Сенсорные стимулы вызывают изменения в суммарной электрической активности мозга, которые выглядят как последовательность из нескольких позитивных и негативных волн, которая длится в течение 0,5-1 с после стимула. Этот ответ получил название вызванного потенциала (evoked potential). Его нелегко выделить из фо-
новой ЭЭГ. В 1951 г. Дж. Даусон (G. Dawson) разработал технику когерентного накопления или усреднения ответов. Использовалась процедура синхронизации ЭЭГ относительно момента предъявления стимула, который поэтому многократно повторялся. Сначала использовалась суперпозиция -- наложение нескольких реакций (участков ЭЭГ, следующих за стимулом). Обычно это выполнялось на фотопленке, что позволяло выявить наиболее устойчивые части реакции на стимул. Затем процедура суперпозиции была заменена на суммацию участков ЭЭГ и получение усредненного вызванного потенциала (average evoked potential) (Шагас Ч., 1975; Рут-ман Э.М., 1975).
Эффективность этой процедуры была наглядно продемонстрирована при выявлении звуковых стволовых вызванных потенциалов (ВГТ). Из-за их очень малой амплитуды требуется просуммировать и усреднить несколько тысяч единичных ответов. На рис. 2 представлены основные группы компонентов звукового усредненного ВП. По латентному периоду компоненты делятся на три груп-ч пы: потенциалы ствола мозга (с лагенцией до 10—12 мс), средне-Л латентные (до 50 мс) и длиннолатентные (более 100 мс) потенци-д алы. Звуковые стволовые потенциалы состоят из 7 отклонений. Волна I \ зависит от реакции волокон слухового нерва улитки. Волна II с ла-N тенцисй 3,8 мс возникает в том случае, если импульсы слухового ^ нерва достигают ствола мозга. Волна III отражает реакцию верхней Ч оливы на уровне моста, Волна IV с латенцией около 4,5 мс связана с активностью латеральных лемнисков. Волна V имеет латенцию около 5,2 мс и отражает активность нижнего двухолмия. Фазы VI— VII — распространение сигналов по таламо-кортикальной радиации, они совпадают с медленной негативностью, предшествующей корковому ответу. Ранние компоненты нечувствительны к сну. наркозу. Они вызываются звуковыми топами частотой 2000-4000 Гц. Звуки на частоте ниже 2000 Гц вызывают только волну V.
Стволовые потенциалы — высокочувствительный инструмент Для тестирования слуховой функции. Они позволяют определить сохранность слухового анализатора на периферическом и стволовом уровнях. Особенно это важно при обследовании слуха у детей, в том числе у новорожденных, когда словесные реакции не могут быть использованы. Значение этого геста возрастает в связи с тем фактом, что даже незначительная потеря слуха в раннем детстве может привести к существенной задержке развития речи. Стволовые звуковые потенциалы применяют также в клинике для выявления опухолей, определения коматозного состояния, обследования пациентов с демиелинизацией волокон. Если стволовые потенциалы полностью отсутствуют, можно говорить о смерти
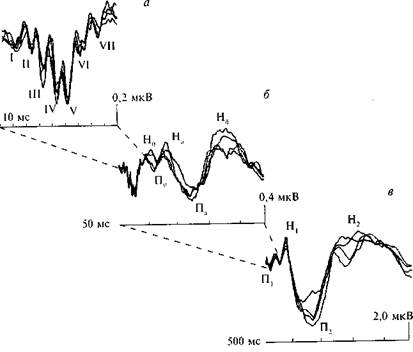
Рис. 2. Основные компоненты звукового ВП, зарегистрированного между вертексом и правым сосцевидным отростком в ответ на щелчок (60 дБ над
уровнем порога), предъявляемый на правое ухо с частотой 1 Гц. а — стволовые, б — срсднслатентпые, в — длиннолатентные компоненты; Н — негативные. П — позитивные компоненты. Для трех групп компонентов временные шкалы и калибровка различны. Начало временных шкал соответствует моменту подачи стимула. Каждая кривая получена в результате усреднения 1024 индивидуальных ответов (по R. Naatanen, 1992).
Среднелатентные и длиннолатентные компоненты отражают функционирование кортикального уровня слухового анализатора. Среднелатентные компоненты (Н(), П0, На, Па, Н6) регистрируются от первичной слуховой коры, имеют малую амплитуду, более лабильны, чем стволовые потенциалы, чувствительны к сну, наркозу. Максимальная их амплитуда вызывается звуковыми тонами речевого диапазона. Длиннолатентные ответы включают компонент Н, с латенцией пика в 100 мс. Потенциал характеризуется
полимодальностью и чувствительностью к активации. Кроме того, на него может накладываться другой потенциал — негативность рассогласования (HP), которую связывают с процессами пред-внимания (см. главу «Внимание»). Компонент П2 имеет специфические и неспецифические составляющие. Волна Н2 также включает несколько компонентов.
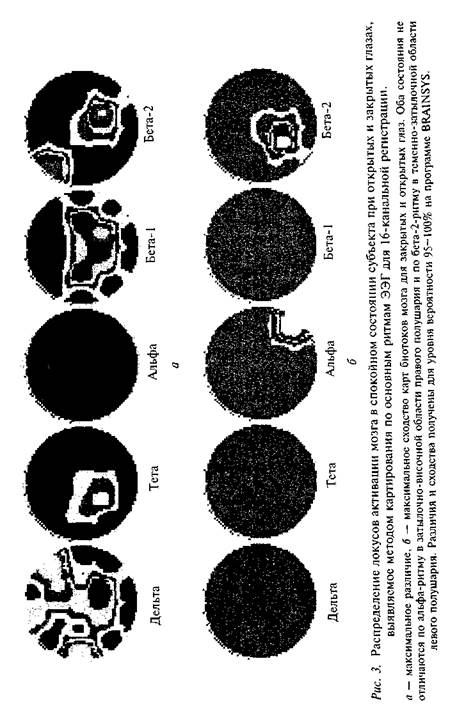
Позже техника усреднения ВП была применена для выявления потенциалов, связанных с движением. Участки ЭЭГ усреднялись относительно не стимула, а начала движения. Это дало возможность исследовать моторные потенциалы и потенциалы готовности, предшествующие движению. Для обозначения всех групп потенциалов был введен общий для них термин — «потенциалы, связанные с событиями» (ПСС), объединяющий ВП, моторный потенциал и др. На основе многоканальной регистрации ЭЭГ был разработан метод картирования биотоков мозга (brain mapping). Картирование дает представление о пространственном распределении по коре любого выбранного показателя электрической активности мозга. Это может быть ВП, один из его компонентов или альфа-ритм (или другие частотные полосы спектра ЭЭГ). Значения мощности выбранного показателя подразделяются на уровни. В одном варианте каждому уровню приписывается свой цвет и изменение локу-са активности выглядит как перемещение определенного цвета по карте. В другом варианте значения показателя, принадлежащие одному уровню, соединяются изолиниями, как на топографических картах, на которых можно видеть возвышенности и впадины. Рассматриваются карты, полученные в разное время и в разных условиях. Этот метод позволяет выявить фокусы активности мозга. Используется процедура вычитания одной карты потенциалов из другой, что позволяет связать паттерн ЭЭГ-активности с той или другой когнитивной операцией. На рис. 3 приведен пример картирования мозговой активности по основным ритмам ЭЭГ для двух состояний взрослого испытуемого (открытые и закрытые глаза). Измерялась мощность распределения для каждого ритма (дельта, тета, альфа, бета-1, бета-2) в процентах. Показаны карты максимального различия и сходства для сравниваемых двух состояний. Открытые глаза, создающие условия для перцептивной активности, вызывают усиление бета-2 с фокусом в теменно-затылочной области правого полушария, отвечающего за конкретно-образное мышление и сенсорно-пространственные преобразования. Второй фокус активности бета-2 локапизован в левой фронтальной коре, функции которой связаны с управлением выполняемой деятельности и рабочей памятью. Одновременно открытые глаза усиливают мощность оета-1 в теменно-центральных отведениях обоих полушарий.
 |
Чтобы сжать информацию, содержащуюся в карте с изолиниями, делают следующий шаг: рассчитывают некоторый источник тока — диполь, эквивалентный реальному источнику тока в мозге. Определяют его локализацию, ориентацию, длину. Таким диполем обычно можно объяснить до 80—90% потенциалов, зарегистрированных от поверхности черепа. Процедура определения диполя включает построение новой карты распределения потенциалов, исходя из характеристик первично рассчитанного диполя. Затем рассчитанную карту сравнивают с исходной картой потенциалов. При их различии включают процедуру итерации, которая вносит коррективы в локализацию и характеристики рассчитанного диполя. В результате расчетная карта потенциалов максимально при-
~> 1
ближается к исходной. При расчете диполя учитывают различия распространения тока в объемном проводнике для разных типов ткани, находящейся под электродом (кожа, кости черепа, мозговые оболочки, структуры мозга).
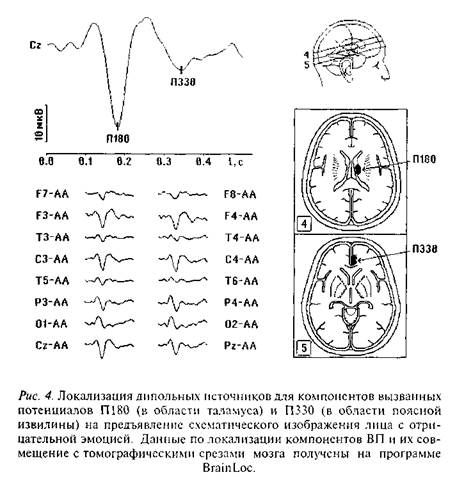
На рис. 4 представлены результаты расчетов дипольных источников для двух компонентов ВП. Наложение данных об источниках ЭЭГ-активности на структурные томограммы мозга конкретного человека, полученные методом структурной магнитно-резонансной томографии, дает наглядное представление о распределении локусов активации по структурам мозга. Соединение двух методов: структурной магнитно-резонансной томографии и дипольной трехмерной локализации источников электрической активности мозга — позволяет получать результаты, близкие тем, которые обычно выявляются только методами функциональной томографии (см. раздел «Томографические методы исследования мозга»).
МАГНИТОЭНЦЕФАЛОГРАФИЯ
Значительные успехи в локализации источников активности мозга, достигнутые в последнее десятилетие, связаны с развитием магнитоэнцефалографии (Холодов Ю.А. и др., 1987; Naatanen R., 1992). Первые электромагнитные поля (ЭМП) нервной системы были зарегистрированы у лягушки. Они были записаны с расстояния 12 мм при возбуждении седалищного нерва. Биологические поля мозга и различных органов очень малы. Магнитное поле человеческого сердца составляет около 1 миллионной доли земного магнитного поля, а человеческого тела — в 100 раз слабее. Магнитное поле сердца человека впервые было записано в 1963 г. Первые же измерения ЭМП мозга человека были сделаны Д. Косном (Koen D.) из Массачусетского технологического института в 1968 г. Магнитным методом он зарегистрировал спонтанный альфа-ритм у здоровых испытуемых и изменение активности мозга у эпилептиков. Первые вызванные потенциалы с помощью магнитометров были получены несколько лет спустя.
Сначапа для регистрации ЭМП были использованы индукционные катушки с большим количеством витков. С увеличением их числа чувствительность системы возрастает.Число витков в первых таких катушках достигало миллиона. Однако чувствительность их оставалась невысокой и они не регистрировали постоянное ЭМП.
Создание новых магнитометров связано с открытием Б. Джо-зефсона, за которое он получил Нобелевскую премию. Работая в области криогенной технологии со сверхпроводящими материалами, он обнаружил, что между двумя сверхпроводниками, разде-
ленными диэлектриком, возникает ток, если они находятся вблизи ЭМП. Эта система реагировала на переменные и постоянные ЭМП. На основе открытия Б. Джозефсона были созданы СКВИДы — сверхпроводниковые квантомеханические интерференционные датчики. Магнитометры, работающие на базе СКВИДа, очень дороги, их необходимо регулярно заполнять жидким гелием в качестве диэлектрика. Дальнейшее совершенствование магнитометров связано с разработкой квантовых магнитометров с оптической накачкой (МОИ). Созданы МОНы, в которых вместо жидкого гелия используются пары щелочного металла цезия. Это более дешевые системы, не требующие криогенной техники. В них световой сигнал поступает по световодам от общего источника и достигает фотодетекторов. Колебания ЭМП мозга человека модулируют сигнал на фотодетекторах. По его колебаниям судят об электромагнитных волнах мозга. Каждый магнитометр имеет множество датчиков, что позволяет получать пространственную картину распределения ЭМП. Современные магнитометры (СКВИДы и др.) обладают высокой временной и пространственной разрешающей способностью (до 1 мм и 1 мс). Магнитоэнцефалограмма (МЭГ) по сравнению с ЭЭГ обладает рядом преимуществ. Прежде всего это связано с бесконтактным методом регистрации. МЭГ не испытывает также искажений от кожи, подкожной жировой клетчатки, костей черепа, твердой мозговой оболочки, крови и др., так как магнитная проницаемость для воздуха и для тканей примерно одинакова. В МЭГ отражаются только источники активности, которые расположены тангенциально (параллельно черепу), так как МЭГ не реагирует на радиально ориентированные источники, т.е. расположенные перпендикулярно поверхности. Благодаря этим свойствам МЭГ позволяет определять локализацию только корковых диполей, тогда как в ЭЭГ суммируются сигналы от всех источников независимо от их ориентации, что затрудняет их разделение. МЭГ не требует индифферентного электрода и снимает проблему выбора места для реально неактивного отведения. Для МЭГ, так же как и для ЭЭГ, существует проблема увеличения соотношения «сигнал-шум», поэтому усреднение ответов также необходимо. Из-за различной чувствительности ЭЭГ и МЭГ к источникам активности особенно полезно комбинированное их использование.
