Геологическая деятельность подземных вод
ГИДРОГЕОХИМИЯ (продолжение)
– Виды выражения химического состава подземных вод.
Полезные, либо вредные свойства воды и ее пригодность для использования человеком можно определить исходя из рассмотрения растворенных в воде химических элементов и соединений.
Такое содержание в количественном выражении определяют в процессе выполнения химических анализов. Анализы подразделяют на общий анализ и специальные виды анализа.
Общий анализ , который также известен как стандартный, либо шестикомпонентный анализ, включает определение шести основных ионов: Cl-, SO42–, HCO3–, Ca2+, Mg2+, Na+, минерализации, плотности и рН воды.
Специальные виды анализа разнообразны. Их вид зависит от поставленной задачи. В поисковой нефтяной гидрогеологии, выполняют часто определение содержания J, Br, аммония, органических соединений, а также газовый состав, содержащийся в пробах воды.
Санитарный анализ выполняют чтобы определить пригодна ли вода в качестве питьевой, а также удовлетворяет ли она требованиям к воде для бытового использования. При этом определяют содержание ионов NH2+, NO2–, NO3– и окисляемость воды. В ряде случаев выполняют бактериологический анализ.
Бальнеологические анализы выполняют с тем, чтобы определить лечебные свойства воды. Как правило, такие анализы включают расширенный список дополнительных элементов, таких как определение содержания сульфидов, железа, мышьяка, лития, радиоактивности (например, содержание радона) и газовой составляющей.
Технические анализы выполняют с целью определить степень пригодности воды для технических нужд, таких как – для закачки вод в нефтяные пласты для вытеснения нефти, в котельных – для питания паровых котлов, для оценки других коррозионных (агрессивных) свойств воды.
Способы (формы) изображения химического состава воды.
На практике используют следующие формы отображения: весовая ионная, эквивалентная и процент-эквивалентная формы.
Весовая ионная форма – это выражение состава воды в виде весового количества отдельных ионов. При этом, содержание ионов (в миллиграммах, либо граммах) в единице объема, либо единице массы (обычно в 100 см3, 1000 см3, 100 г, 1 кг).
Если для пресных вод не имеет решающего значения, в каких единицах приведено это выражение, то для рассолов есть различие. Для выражения содержания растворенных газов в ряде веществ, находящихся в коллоидном состоянии, весовая ионная форма не используется.
Эквивалентная форма более точно учитывает химические свойства воды, позволяет контролировать точность результатов анализа и вычислять содержание ионов натрия и калия без прямого их аналитического определения.
Ионы, содержащиеся в растворе, реагируют между собой в количествах, определяемых весом и валентностью ионов (другими словами – в эквивалентных количествах). Как известно, эквивалентный вес (эквивалент) иона - это частное от деления ионного веса на его валентность. Так, эквивалент иона Са2+ равен 20 (40 : 2), а эквивалент иона SO42–, - 48 (96 : 2), или 20 весовых единиц иона Са2+ соответствует 48 весовым единицам иона SO42–.
Весовую ионную форму переводят в эквивалентную форму путем деления содержания ионов ( в мг, или г) на величину эквивалента иона. Можно также умножить содержание иона в весовой форме на коэффициент реакции (являющийся обратной величиной эквивалента этого иона).
Наличие перед химическим символом иона буквы r (например, rNa+, rCl– и т.д.) показывает, что содержание этого элемента выражено в эквивалентной форме.
Если же анионы и катионы даны в эквивалентной форме, то исходя из принципа электронейтральности раствора сумма анионов (Σra) должна быть всегда равна сумме катионов (Σrк)
Σra = Σrк
Тогда всегда можно определить содержание одного из шести ионов, если известны содержания других пяти. Тк, например иногда определяют содержание Na+:
rNa+ = (rCl–+ rHCO3–+ rSO42–) – (rCa2+ + rMg2+).
Чтобы определить содержание Na+в весовой ионной форме, полученную величину rNa+умножают на его эквивалент.
Процент-эквивалентная форма является модификацией эквивалентной формы и характеризует относительную долю каждого иона в общей сумме растворенных ионов, равную 100 %. Здесь сумма катионов и сумма анионов составляют по 50 %. Иногда принимают за 100 % сумму катионов (равной сумме анионов), при этом общее содержание ионов будет 200 %.
Содержание каждого иона в процентах от суммы всех ионов дает процент-эквивалентную форму отображения ионно-солевого состав воды.
Составив пропорции, где сумма всех ионов в эквивалентной форме равна (100% (или 200%), находим процентное содержание всех ионов последовательно:
Σ(а +к) – 100%,
i – x %,
Где Σ(а +к) – сумма ионов и катионов в эквивалентной форме; i – содержание искомого иона в эквивалентной форме; x – содержание искомого иона в процент-эквивалентной форме.
Заметим, что процент-эквивалентная форма не учитывает минерализацию воды. Это дает возможность сравнивать химический состав вод независимо от их степени минерализации.
В гидрогеологии используют три рассмотренные формы. Кроме того, чтобы кратко изобразить химический состав воды используют формулу М.ГЭ. Курлова. Она представляет собой сложную дробь. В числителе указывают содержание анионов, а в знаменателе – катионов в процент-эквивалентной форме. Ионы записывают по убывающим величинам. Перед дробью перечисляют основные компоненты состава растворенных газов и величину минерализации (г/дм3). За дробью приводят температуру, рН, содержание микрокомпонентов состава.
Например: 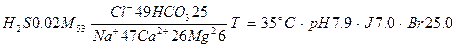
При этом, можно сказать, что состав воды следующий: сероводородная соленая вода гидрокарбонатно-хлоридного магниево-кальциево-натриевого состава имеет температуру 35 ˚С, слабощелочная, содержит йод (7.9 мг/дм3) и бром (25 мг/ дм3).
Ранее применяли характеристику Пальмера для определения характеристики воды нефтяных месторождений. Это определение воды по содержанию в ней тех или иных групп солей. Последние сочетаются из ионов по правилу Фрезениуса, утверждающей о том, что ионы соединяются между собой в порядке уменьшения химической активности. Последовательность степени активности основных ионов следующая: анионы – Cl–, SO42–, HCO3-, катионы – Na+, Mg2+, Ca2+.
Ионы Br-, J- располагаются за ионом Cl-; ионы H+, Fe3+, Al3+ - после иона Ca2+; ион HS– - после HCO3–; ион K+ - перед Na+; ион NH4+ - после Na+.
В соответствии с формулой Фрезениуса ион Cl– соединяется с ионом Na+, при избытке хлора его остаток затем соединяется с магнием, а в случае преобладания над ним – с кальцием; при избытке же натрия, его остаток соединяется с сульфат-ионом. Если натрий преобладает над сульфатом, то он (натрий) соединяется с гидрокарбонатом.
Пальмер выделил шесть солевых характеристик. Основное значение имеют: первая соленость (S1), вторая соленость (S2), первая щелочность (А1) и вторая щелочность (А2).
Графические методы изображения состава вод применяют для наглядного сравнения состава различных вод, а также – на картах и разрезах.
График Толстихина имеет круговую форму. Он используется для изображения состава отдельных проб воды в процент-эквивалентах. При этом, минерализация воды соответствует в выбранном масштабе радиусу круга. Он используется для вынесения единичных проб воды на карты. С его помощью можно изображать и состав растворенных и свободных газов.
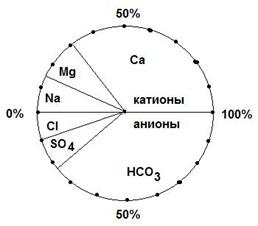
График Роджерса представляет собой 3 столбика одинаковой высоты. В крайних столбиках расположены ионы в порядке убывания их химической активности – левый столбик соответствует суммарному содержанию анионов, а правый – катионов. Вся высота столбика соответствует 50%-экв. Средний столбик отображает характеристику Пальмера. Его высота равна 100%-экв. Таким образом, график Роджерса изображает состав воды в процент-эквивалентной форме и позволяет легко графически находить характеристики Пальмера.
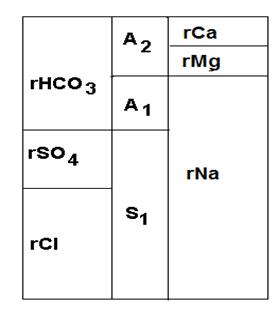
Метод «узоров» Стиффа. Он заключается в том, что содержание главных ионов (в миллиграмм-эквивалентной форме) откладывается в масштабе от общей оси. Концы отрезков, соединенных ломаной линией, образуют узор. От этого произошло его название.
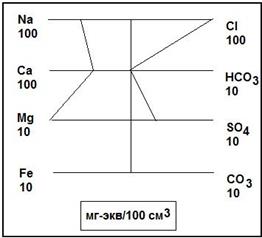
Полулогарифмическая диаграмма Шеллера – это график, по оси абсцисс которого отложены ионы, а по оси ординат – их содержание в миллиграмм-эквивалентах (в полулогарифмическом масштабе). Удобство заключается в том, что на одну диаграмму наносят ряд анализов воды, что позволяет сравнивать их между собой.
Наконец, любая гидрохимическая карта также представляет собой графическое изображение химического состава подземных вод.
ГИДРОГЕОХИМИЯ (продолжение)
– Виды выражения химического состава подземных вод.
Полезные, либо вредные свойства воды и ее пригодность для использования человеком можно определить исходя из рассмотрения растворенных в воде химических элементов и соединений.
Такое содержание в количественном выражении определяют в процессе выполнения химических анализов. Анализы подразделяют на общий анализ и специальные виды анализа.
Общий анализ , который также известен как стандартный, либо шестикомпонентный анализ, включает определение шести основных ионов: Cl-, SO42–, HCO3–, Ca2+, Mg2+, Na+, минерализации, плотности и рН воды.
Специальные виды анализа разнообразны. Их вид зависит от поставленной задачи. В поисковой нефтяной гидрогеологии, выполняют часто определение содержания J, Br, аммония, органических соединений, а также газовый состав, содержащийся в пробах воды.
Санитарный анализ выполняют чтобы определить пригодна ли вода в качестве питьевой, а также удовлетворяет ли она требованиям к воде для бытового использования. При этом определяют содержание ионов NH2+, NO2–, NO3– и окисляемость воды. В ряде случаев выполняют бактериологический анализ.
Бальнеологические анализы выполняют с тем, чтобы определить лечебные свойства воды. Как правило, такие анализы включают расширенный список дополнительных элементов, таких как определение содержания сульфидов, железа, мышьяка, лития, радиоактивности (например, содержание радона) и газовой составляющей.
Технические анализы выполняют с целью определить степень пригодности воды для технических нужд, таких как – для закачки вод в нефтяные пласты для вытеснения нефти, в котельных – для питания паровых котлов, для оценки других коррозионных (агрессивных) свойств воды.
Способы (формы) изображения химического состава воды.
На практике используют следующие формы отображения: весовая ионная, эквивалентная и процент-эквивалентная формы.
Весовая ионная форма – это выражение состава воды в виде весового количества отдельных ионов. При этом, содержание ионов (в миллиграммах, либо граммах) в единице объема, либо единице массы (обычно в 100 см3, 1000 см3, 100 г, 1 кг).
Если для пресных вод не имеет решающего значения, в каких единицах приведено это выражение, то для рассолов есть различие. Для выражения содержания растворенных газов в ряде веществ, находящихся в коллоидном состоянии, весовая ионная форма не используется.
Эквивалентная форма более точно учитывает химические свойства воды, позволяет контролировать точность результатов анализа и вычислять содержание ионов натрия и калия без прямого их аналитического определения.
Ионы, содержащиеся в растворе, реагируют между собой в количествах, определяемых весом и валентностью ионов (другими словами – в эквивалентных количествах). Как известно, эквивалентный вес (эквивалент) иона - это частное от деления ионного веса на его валентность. Так, эквивалент иона Са2+ равен 20 (40 : 2), а эквивалент иона SO42–, - 48 (96 : 2), или 20 весовых единиц иона Са2+ соответствует 48 весовым единицам иона SO42–.
Весовую ионную форму переводят в эквивалентную форму путем деления содержания ионов ( в мг, или г) на величину эквивалента иона. Можно также умножить содержание иона в весовой форме на коэффициент реакции (являющийся обратной величиной эквивалента этого иона).
Наличие перед химическим символом иона буквы r (например, rNa+, rCl– и т.д.) показывает, что содержание этого элемента выражено в эквивалентной форме.
Если же анионы и катионы даны в эквивалентной форме, то исходя из принципа электронейтральности раствора сумма анионов (Σra) должна быть всегда равна сумме катионов (Σrк)
Σra = Σrк
Тогда всегда можно определить содержание одного из шести ионов, если известны содержания других пяти. Тк, например иногда определяют содержание Na+:
rNa+ = (rCl–+ rHCO3–+ rSO42–) – (rCa2+ + rMg2+).
Чтобы определить содержание Na+в весовой ионной форме, полученную величину rNa+умножают на его эквивалент.
Процент-эквивалентная форма является модификацией эквивалентной формы и характеризует относительную долю каждого иона в общей сумме растворенных ионов, равную 100 %. Здесь сумма катионов и сумма анионов составляют по 50 %. Иногда принимают за 100 % сумму катионов (равной сумме анионов), при этом общее содержание ионов будет 200 %.
Содержание каждого иона в процентах от суммы всех ионов дает процент-эквивалентную форму отображения ионно-солевого состав воды.
Составив пропорции, где сумма всех ионов в эквивалентной форме равна (100% (или 200%), находим процентное содержание всех ионов последовательно:
Σ(а +к) – 100%,
i – x %,
Где Σ(а +к) – сумма ионов и катионов в эквивалентной форме; i – содержание искомого иона в эквивалентной форме; x – содержание искомого иона в процент-эквивалентной форме.
Заметим, что процент-эквивалентная форма не учитывает минерализацию воды. Это дает возможность сравнивать химический состав вод независимо от их степени минерализации.
В гидрогеологии используют три рассмотренные формы. Кроме того, чтобы кратко изобразить химический состав воды используют формулу М.ГЭ. Курлова. Она представляет собой сложную дробь. В числителе указывают содержание анионов, а в знаменателе – катионов в процент-эквивалентной форме. Ионы записывают по убывающим величинам. Перед дробью перечисляют основные компоненты состава растворенных газов и величину минерализации (г/дм3). За дробью приводят температуру, рН, содержание микрокомпонентов состава.
Например: 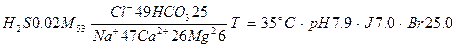
При этом, можно сказать, что состав воды следующий: сероводородная соленая вода гидрокарбонатно-хлоридного магниево-кальциево-натриевого состава имеет температуру 35 ˚С, слабощелочная, содержит йод (7.9 мг/дм3) и бром (25 мг/ дм3).
Ранее применяли характеристику Пальмера для определения характеристики воды нефтяных месторождений. Это определение воды по содержанию в ней тех или иных групп солей. Последние сочетаются из ионов по правилу Фрезениуса, утверждающей о том, что ионы соединяются между собой в порядке уменьшения химической активности. Последовательность степени активности основных ионов следующая: анионы – Cl–, SO42–, HCO3-, катионы – Na+, Mg2+, Ca2+.
Ионы Br-, J- располагаются за ионом Cl-; ионы H+, Fe3+, Al3+ - после иона Ca2+; ион HS– - после HCO3–; ион K+ - перед Na+; ион NH4+ - после Na+.
В соответствии с формулой Фрезениуса ион Cl– соединяется с ионом Na+, при избытке хлора его остаток затем соединяется с магнием, а в случае преобладания над ним – с кальцием; при избытке же натрия, его остаток соединяется с сульфат-ионом. Если натрий преобладает над сульфатом, то он (натрий) соединяется с гидрокарбонатом.
Пальмер выделил шесть солевых характеристик. Основное значение имеют: первая соленость (S1), вторая соленость (S2), первая щелочность (А1) и вторая щелочность (А2).
Графические методы изображения состава вод применяют для наглядного сравнения состава различных вод, а также – на картах и разрезах.
График Толстихина имеет круговую форму. Он используется для изображения состава отдельных проб воды в процент-эквивалентах. При этом, минерализация воды соответствует в выбранном масштабе радиусу круга. Он используется для вынесения единичных проб воды на карты. С его помощью можно изображать и состав растворенных и свободных газов.

График Роджерса представляет собой 3 столбика одинаковой высоты. В крайних столбиках расположены ионы в порядке убывания их химической активности – левый столбик соответствует суммарному содержанию анионов, а правый – катионов. Вся высота столбика соответствует 50%-экв. Средний столбик отображает характеристику Пальмера. Его высота равна 100%-экв. Таким образом, график Роджерса изображает состав воды в процент-эквивалентной форме и позволяет легко графически находить характеристики Пальмера.

Метод «узоров» Стиффа. Он заключается в том, что содержание главных ионов (в миллиграмм-эквивалентной форме) откладывается в масштабе от общей оси. Концы отрезков, соединенных ломаной линией, образуют узор. От этого произошло его название.

Полулогарифмическая диаграмма Шеллера – это график, по оси абсцисс которого отложены ионы, а по оси ординат – их содержание в миллиграмм-эквивалентах (в полулогарифмическом масштабе). Удобство заключается в том, что на одну диаграмму наносят ряд анализов воды, что позволяет сравнивать их между собой.
Наконец, любая гидрохимическая карта также представляет собой графическое изображение химического состава подземных вод.
ГЕОЛОГИЧЕСКАЯ ДЕЯТЕЛЬНОСТЬ ПОДЗЕМНЫХ ВОД
Любой геологический процесс так или иначе связан с водой, поскольку вода существует в земных недрах практически везде.
