Основные этапы истории генетики
Методы генетики
Генетика, как любая наука имеет свои методы исследований. В ходе развития и накопления знаний появляются новые способы изучения наследственности и изменчивости организмов. Многообразие методов генетики определяется разнообразием объектов и структур изучения. К классическим методам генетики можно отнести:
1.Гибридологический метод — скрещивание (гибридизация) организмов, отличающихся друг от друга по одному или нескольким признакам. Потомки от таких скрещиваний называются гибридами.
2.Генеалогический метод (метод родословных) — изучение наследования какого-либо признака у человека в ряде поколений. Позволяет прогнозировать вероятность передачи потомкам наследственных заболеваний.
3.Близнецовый метод — изучение проявления признаков у однояйцовых близнецов. Позволяет оценить роль внешней среды в формировании фенотипа.
4.Цитогенетический метод — изучение количества, формы и размеров хромосом. Позволяет обнаружить хромосомные и геномные мутации.
5.Биохимический метод — изучение наследственно обусловленных нарушений обмена веществ. Позволяет обнаружить генные мутации.
6.Популяционный метод — изучение частоты встречаемости генов и генотипов в популяциях. Дает информацию о степени гетерозиготности и полиморфизма (неоднородности) человеческих популяций.
На современном этапе развития успехи молекулярной генетики создали предпосылки для возникновения четырех новых направлений генетических исследований преимущественно прикладного характера, основная цель которых изменять геном организма в желаемую сторону. Наиболее быстро из этих направлений развивались: 1.генетическая инженерия и
2.генетика соматических клеток.
Генетическая инженерия подразделяется на генную (искусственный перенос отдельных генов) и хромосомную (искусственный перенос хромосом и их фрагментов). Методы генной инженерии, развитие которых началось в 1972 в США в лаборатории П. Берга, широко используются для промышленного производства высококачественных биопрепаратов, используемых в медицине (инсулин человека, интерферон, вакцины против гепатитов В, для диагностики СПИД и т. д.). С их помощью получены разнообразные трансгенные животные. Получены растения картофеля и подсолнечника, обогащенные запасным белком, кодируемым геном бобовых, растения подсолнечника, обогащенные белком, кодируемым геном кукурузы. Очень перспективны работы, ведущиеся во многих лабораториях мира, по переносу генов азотфиксации из почвенных бактерий в сельскохозяйственные растения. Делаются попытки излечения наследственных заболеваний путем введения в организм пациента «здорового» гена для замещения им мутантного, являющегося причиной болезни. Достижения в технологии рекомбинантных ДНК, сделавшие возможным выделение многих генов др. организмов, а также расширение знаний о регуляции их экспрессии позволяют надеяться на реализацию этой, казавшейся прежде фантастической, идеи.
Метод хромосомной инженерии позволяет пересадить в яйцеклетку млекопитающего с удаленным ядром диплоидное ядро соматической клетки и ввести такую яйцеклетку в матку самки, гормонально подготовленную к имплантации. В этом случае родится потомок, генетически идентичный особи, от которой взята соматическая клетка. Таких потомков можно получить от этой особи неограниченное число, т. е. генетически клонировать ее.
2.ГЕНЕТИКА СОМАТИЧЕСКИХ КЛЕТОК ЗАНИМАЕТСЯ исследованиями, проводимыми на соматических клетках растений, животных и человека. Селекциейклеток растений — продуцентов лекарственных алкалоидов (руты душистой, раувольфии), в сочетании с мутагенезом содержание этих алкалоидов в клеточной массе повышено в 10-20 раз. Селекцией клеток на питательных средах и последующей регенерацией целых растений из клеточного каллуса выведены сорта ряда возделываемых растений, устойчивые к различным гербицидам и засолению почвы. Гибридизацией соматических клеток разных видов и родов растений, половая гибридизация которых невозможна или очень затруднена, и последующей регенерацией из клеточного каллуса созданы разные гибридные формы (капуста — турнепс, культурный картофель — дикие его виды и т. п.).
Другое важное достижение генетики соматических клеток животных — создание гибридов, на основе которых получают моноклональные антитела, служащие для создания высокоспецифических вакцин, а также для выделения необходимого фермента из смеси ферментов.
Весьма перспективны для практики еще два молекулярно-генетических направления — 3. сайт-специфичный мутагенез и 4.создание антисмысловых РНК. Сайт-специфичный мутагенез (индукция мутаций определенного выделенного рестриктазами гена или его комплементарной ДНК, и затем включение мутировавшего гена в геном для замены им его немутантного аллеля) впервые позволил индуцировать желательные, а не случайные генные мутации, и уже успешно применяется для получения направленных генных мутаций у бактерий и дрожжей.
Антисмысловые РНК, возможность получения которых впервые была показана в 1981 работающим в США японским иммунологом Д. Томизавой, могут использоваться для целенаправленного регулирования уровня синтеза определенных белков, а также для направленного ингибирования онкогенов и вирусных геномов. Исследования, проведенные по этим новым генетическим направлениям, были нацелены преимущественно на решение прикладных задач. Вместе с тем они внесли фундаментальный вклад в представления об организации генома, структуре и функциях генов, взаимоотношениях генов ядра и клеточных органелл и др.
Генетика в России и СССР
Если не считать опытов по гибридизации растений в XVIII в., первые работы по генетике в России были начаты в начале XX в. как на опытных сельскохозяйственных станциях, так и в среде университетских биологов, преимущественно тех, кто занимался экспериментальной ботаникой и зоологией.
После революции и гражданской войны 1917—1922 гг. началось стремительное организационное развитие науки. К концу 1930-х годов в СССР была создана обширная сеть научно-исследовательских институтов и опытных станций (как в Академии наук СССР, так и во Всесоюзной академии сельскохозяйственных наук имени Ленина (ВАСХНИЛ)), а также вузовских кафедр генетики. Признанными лидерами направления были Н. И. Вавилов, Н. К. Кольцов, А. С. Серебровский, С. С. Четвериков и др. В СССР издавали переводы трудов иностранных генетиков, в том числе Т. Х. Моргана, Г. Мёллера, ряд генетиков участвовали в международных программах научного обмена. Американский генетик Г. Мёллер работал в СССР (1934—1937), советские генетики работали за границей. Н. В. Тимофеев-Ресовский — в Германии (с 1925 г.), Ф. Г. Добржанский — в США (с 1927 г.).
В 1930-е гг. в рядах генетиков и селекционеров наметился раскол, связанный с энергичной деятельностью Т. Д. Лысенко и И.И. Презента. По инициативе генетиков был проведен ряд дискуссий (наиболее крупные—в 1936 и 1939 г.), направленных на борьбу с подходом Лысенко, но их результаты были довольно неопределенными.
На рубеже 1930—1940-х гг. в ходе так называемого Большого террора большинство сотрудников аппарата ЦК ВКП(б), курировавших генетику, и ряд видных генетиков были арестованы, многие расстреляны или погибли в тюрьмах (в том числе, Н.И. Вавилов). После войны дебаты возобновились с новой силой. Генетики, опираясь на авторитет международного научного сообщества, снова попытались склонить чашу весов в свою сторону, однако с началом Холодной войны ситуация значительно изменилась. В 1948 году на августовской сессии ВАСХНИЛ Т.Д. Лысенко, пользуясь поддержкой И. В. Сталина, объявил генетику лженаукой. Лысенко воспользовался некомпетентностью партийного руководства наукой, «пообещав партии» быстрое создание новых высокопродуктивных сортов зерна («ветвистая пшеница») и др. С этого момента начался период гонений на генетику, который получил название лысенковщины и продолжался вплоть до снятия Н.С. Хрущева с поста генерального секретаря ЦК КПСС в 1964 г.
Лично Т.Д. Лысенко и его сторонники получили контроль над институтами отделения биологии АН СССР, ВАСХНИЛ и вузовскими кафедрами. Были изданы новые учебники для школ и вузов, написанные с позиций «Мичуринской биологии». Генетики вынуждены были оставить научную деятельность или радикально изменить профиль работы. Некоторым удалось продолжить исследования по генетике в рамках программ по изучению радиационной и химической опасности за пределами организаций, подконтрольных Т.Д. Лысенко и его сторонникам.
Сходные с лысенковщиной явления наблюдались и в других науках. Наиболее известные кампании прошли в цитологии (в связи с учением О.Б. Лепешинской о живом веществе), физиологии (борьба К. М. Быкова и его сторонников за «наследие» И.П. Павлова) и микробиологии (теории Г. М. Бошьяна).
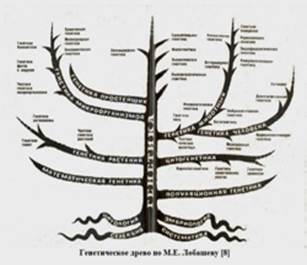
Генетика М. Е. Лобашёва, 1-е издание - учебник 1963 г., который вслед перерабатывает и в 1969 г. выходит его второе издание, дано древо жизни. Первый учебник генетики для вузов после периода лысенковщины.
С середины 1960-х г. началось восстановление генетики. В 1963 г. вышел в свет университетский учебник М. Е. Лобашёва Генетика, выдержавший впоследствии несколько изданий. В настоящее время исследования по генетике продолжаются в крупных научных центрах России.
Грегор Иоганн Мендель

Грегор Иоганн Мендель (нем. Gregor Johann Mendel) (1822-1884) — австрийский биолог и ботаник, сыгравший огромную роль в развитии представления о наследственности. Открытие им закономерностей наследования моногенных признаков (эти закономерности известны теперь как Законы Менделя) стало первым шагом на пути к современной генетике.
Иоганн Мендель родился 20 июля 1822 в крестьянской семье Антона и Розины Мендель в маленьком сельском городке Хейнцендорф (Австрийская империя, позже Австро-Венгрия, теперь Гинчице (часть села Вражне) у Нового Йичина, Чехия). Дата 22 июля, которая нередко приводится в литературе как дата его рождения, на самом деле является датой его крещения.
Интерес к природе он начал проявлять рано, уже мальчишкой работая садовником. Проучившись два года в философских классах института Ольмюца (в настоящее время Оломоуц, Чехия), в 1843 он постригся в монахи Августинского монастыря Св. Фомы в Брюнне (ныне Брно, Чехия) и взял имя Грегор. С 1844 по 1848 г. учился в Брюннском богословском институте. В 1847 году стал священником. Самостоятельно изучал множество наук, заменял отсутствующих преподавателей греческого языка и математики в одной из школ. Сдавая экзамен на звание преподавателя, получил, как ни странно, неудовлетворительные оценки по биологии и геологии. В 1849—1851 гг. преподавал в Зноймской гимназии математику, латинский и греческий языки. В период 1851—53 года, благодаря настоятелю, обучался естественной истории в Венском университете, в том числе под руководством Унгера — одного из первых цитологов мира.
Будучи в Вене, Мендель заинтересовался процессом гибридизации растений и, в частности, разными типами гибридных потомков и их статистическими соотношениями.
В 1854 году Мендель получил место преподавателя физики и естественной истории в Высшей реальной школе в Брюнне, не будучи дипломированным специалистом. Ещё две попытки сдать экзамен по биологии в 1856 году окончились провалом, и Мендель оставался по-прежнему монахом, а позже — аббатом Августинского монастыря.
Вдохновившись изучением изменений признаков растений, с 1856 по 1863 г. стал проводить опыты на горохе в экспериментальном монастырском саду, и сформулировал законы, объясняющие механизм наследования, известные нам как «Законы Менделя».
8 марта 1865 г. Мендель доложил результаты своих опытов брюннскому Обществу естествоиспытателей, которое в конце следующего года опубликовало конспект его доклада в очередном томе «Трудов Общества…» под названием «Опыты над растительными гибридами». Этот том попал в 120 библиотек университетов мира. Мендель заказал 40 отдельных оттисков своей работы, почти все из которых разослал крупным исследователям-ботаникам. Но работа не вызвала интереса у современников.
Мендель сделал открытие чрезвычайной важности, и сам сначала был, по-видимому, в этом убеждён. Но потом он предпринял ряд попыток подтвердить это открытие на других биологических видах, и с этой целью провёл серию опытов по скрещиванию разновидностей ястребинки — растения семейства астровых, затем — по скрещиванию разновидностей пчёл. В обоих случаях его ждало трагическое разочарование: результаты, полученные им на горохе, на других видах не подтверждались. Причина была в том, что механизмы оплодотворения и ястребинки, и пчёл, имели особенности, о которых в то время науке ещё не было известно, а теми методами скрещивания, которыми пользовался Мендель в своих опытах, эти особенности не учитывались. В конце концов великий учёный сам разуверился в том, что совершил открытие.
В 1868 г. Мендель был избран настоятелем монастыря и больше биологическими исследованиями не занимался. Только в начале XX века, с развитием представлений о генах, была осознана вся важность сделанных им выводов (после того, как ряд других учёных, независимо друг от друга, заново открыли уже выведенные Менделем законы наследования).
Мендель умер 6 января 1884 года и не был признан своими современниками. На его могиле установлена плита, на которой есть надпись «Мое время ещё придёт!».
Фридрих Мишер

Фридрих Мишер (нем. Friedrich Miescher, 1844-1895) — швейцарский физиолог, гистолог и биолог, учился в Базеле, Геттингене, Тюбингене и Лейпциге, в 1871 г. приват-доцент, в 1872 г. — профессор физиологии в Базеле. В 1869 году Фридрих Мишер открыл ДНК. Вначале новое вещество получило название нуклеин, а позже, когда Мишер определил, что это вещество обладает кислотными свойствами, вещество получило название нуклеиновая кислота. Фридрих Мишер проводил также исследования в области строения и состава ядер в желтке куриного яйца, физиологии спинного мозга, состава сперматозоидов лосося (открытие вещества протамин), образа жизни рейнского лосося (изменения в химическом и анатомическом составе разных органов во время образования оварий), движений при дыхании, отношения между высотой над морем и составом крови.
Фредерик Гриффит

Фредерик Гриффит (1879—1941) — английский генетик и врач. В 1928 г. поставил эксперимент, известный ныне как эксперимент Гриффита, которым показал существование «трансформирующиего принципа», позднее идентифицированного как ДНК.
Знаменитый эксперимент Гриффита был выполнен с целью разработки вакцины от пневмонии - обычного осложнения во время пандемии испанки, унесшей больше жизней, чем мировая война. Гриффит работал с двумя штаммами бактерии Streptococcus pneumoniae. Штамм, колонии которого на чашках с агаром были гладкими (S штамм), имел полисахаридную капсулу и был вирулентным, вызывая у подопытных мышей пневмонию, убивавшую их за 1-2 дня. Капсула предохраняла бактерии от воздействия иммунной системы больного. Колонии второго штамма имели неровную поверхность (R штамм) и не вызывали пневмонию, поскольку не имели капсулы, и после введении в кровоток мыши бактерии погибали. Бактерии S штамма, убитые нагреванием, также не вызывали заболевания. Но когда Гриффит смешивал убитый S штамм с живым R штаммом и вводил смесь мышам, животные погибали.
Когда Гриффит выделил болезнетворные бактерии из погибших мышей, он обнаружил, что R штамм приобрел капсулу, то есть превратился в вирулентный S штамм и сохранял новоприобретенный фенотип во многих поколениях, то есть передавал его по наследству. Гриффит предположил, что превращение осуществил некий «трансформирующий фактор», который R штамм получил от убитых бактерий S штамма.
К сожалению, Гриффит не дожил нескольких лет до того дня, когда «трансформирующий фактор» в 1944 г. был идентифицирован как ДНК Освальдом Эйвери и его сотрудниками. В 1941 г. он трагически погиб в своей лаборатории во время налета германской авиации на Лондон.
Николай Иванович Вавилов

Николай Иванович Вавилов (1887-1943) — российский генетик, растениевод, географ, автор закона гомологических рядов в наследственной изменчивости организмов, создатель учения о биологических основах селекции и центрах происхождения и разнообразия культурных растений, академик АН СССР и АН УССР (1929), академик и первый президент (1929-1935) ВАСХНИЛ.
Николай Вавилов организовал ботанико-агрономические экспедиции в страны Средиземноморья, Северной Африки, Северной и Южной Америки, установил на их территории древние очаги происхождения и разнообразия культурных растений. Собрал крупнейшую в мире мировую коллекцию семян культурных растений, заложил основы госсортоиспытания полевых культур. Обосновал учение об иммунитете растений, открыл закон гомологических рядов в наследственной изменчивости организмов (1920).
Н. Вавилов - автор концепции линнеевского вида как системы (1930). Инициатор создания многих научно-исследовательских учреждений. Член ЦИК СССР (1926-1935), президент Всесоюзного географического общества (1931-1940). Премия имени Владимира Ильича Ленина (1926). 6 августа 1940 арестован, обвинен в контрреволюционной вредительской деятельности и в июле 1941 года приговорен к расстрелу, замененному в 1942 году 20-летним заключением. Умер в больнице саратовской тюрьмы, посмертно реабилитирован в 1955 году.
Маршалл Ниренберг

Ниренберг (Nirenberg) Маршалл Уоррен родился 10 апреля 1927 года в Бруклине в семье выходцев из Российской империи, умер в 2010 году в Нью-Йорке.
Американский биохимик, член Национальной АН США (1967) и Американской академии искусств и наук (1966). Окончил университет штата Флорида (1952). Работал в Мичиганском университете (1952–57), институте артритов и болезней обмена веществ (с 1957); с 1962 заведующий лабораторией биохимической генетики Линговского национального института сердца.
Основные труды посвящены расшифровке генетического кода. Ниренберг показал, что полиуридиловая кислота служит матрицей синтеза полифенилаланина и что кодон УУУ (урацил-урацил-урацил) определяет включение аминокислоты фенилаланина в полипептидную цепь в процессе биосинтеза белка. В 1968 году Ниренберг вместе с Робертом Холли и Харом Гобиндом Кораной получили Нобелевскую премию «за расшифровку генетического кода и его функционирования в синтезе белков».
В начале 60-х годов они провели серию экспериментов, которая позволила им расшифровать генетический код. Сначала они синтезировали полиурацил, молекулу РНК, которая содержит только урацил (РНК в отличие от ДНК содержит урацил вместо тимина). Затем исследователи поместили полиурацил в бесклеточную экспериментальную систему, образованную осторожным размельчением бактерий, способствующим получению смеси аминокислот, РНК, рибосом, необходимых ферментов и других веществ. Полиурациловая РНК направляла синтез молекулы белка, состоящего из цепочки молекул аминокислоты фенилаланина. Следовательно, код для фенилаланина представлял собой триплет урацил-урацил-урацил (т. к. урацил является единственным азотистым основанием в полиурациле), или УУУ.
Поскольку ДНК содержит 4 азотистых основания, а генетический код образуется из триплетов азотистых оснований, то существует 64 (4х4х4) возможные триплетные комбинации для ДНК. Ниренбергу и его коллегам удалось синтезировать все возможные триплетные последовательности, повторив бесклеточные эксперименты с каждой из них и открыв таким путем коды триплетов азотистых оснований для всех 20 аминокислот. Некоторые из аминокислот кодируются более чем одним триплетом, а некоторые триплеты известны как "бессмысленные", т. к. они не кодируют ни одну аминокислоту. Ниренберг обнаружил, что "бессмысленные триплеты", как точка в предложении, могут сигнализировать об окончании процесса биосинтеза в клетке. Он и его коллеги провели позднее дополнительные эксперименты, чтобы определить последовательность азотистых оснований в каждом триплете.
Северо Очоа

Очоа - (Ochoa) Севере (1905-93), американский биохимик, родился в Испании. В 1959 г. разделил с Артуром Корнбергом Нобелевскую премию по медицине за работу над синтезом РНК, что имело огромное значение для исследований в области генетики.
Алфред Дей Херши


Алфред Дей Херши (англ. Alfred Day Hershey, 1908-1997) - американский бактериолог и генетик, лауреат Нобелевской премии по физиологии и медицине в 1969 году (совместно с Максом Дельбрюком и Сальвадором Лурией) «за открытия, касающиеся механизма репликации и генетической структуры вирусов».
В 1952г. появилась работа двух американских исследователей - Альфреда Херши и Марты Чейз, которые доказали проникновение фагов внутрь клетки. На поверхности клетки в электронный микроскоп фаги были видны. Но разглядеть их внутри клеток в те год никому не удавалось. Тем более нельзя было увидеть процесс проникновения фага в клетку. Стоило только подставить клетку с налипшими фагами под пучок электронов, как электроны убивали все живое, и то, что отражалось на экране микроскопа, было лишь посмертной маской некогда живых существ. Ученые использовали методы радиационной химии.
12.Кирпичников Валентин Сергеевич (1908–1991) — выдающийся российский биолог, генетик и эволюционист, доктор биологических наук, академик РАЕН, Герой Социалистического Труда, внесший большой вклад в изучение тихоокеанских лососей.
Еще студентом В. С. Кирпичников избрал своей специальностью генетику. Его учителями были Н. К. Кольцов и С. С. Четвериков, впоследствии он тесно сотрудничал с Н. И. Вавиловым, И. И. Шмальгаузеном и многими другими выдающимися отечественными биологами.
Первые работы по генетике и эволюционной теории В. С. Кирпичниковым были выполнены в Институте экспериментальной биологии. В 1935 году он предложил гипотезу о косвенном отборе, которая имела огромное значение для решения проблемы наследования приобретенных признаков.
С 1930-х годов своей непосредственной специальностью Валентин Сергеевич избрал генетику и селекцию рыб. Основными объектами исследований ему служили карповые и тихоокеанские лососи. На базе генетики и эволюционной теории в 1930–1960-х годах, работая в Центральном научном институте рыбного хозяйства и Институте прудового хозяйства (Москва), а также в Институте озерного и речного рыбного хозяйства (в настоящее время ГосНИИОРХ) и Зоологическом институте (Ленинград), В. С. Кирпичников разработал методы селекции, которые позволили создать новые породы рыб, в том числе знаменитого "ропшинского карпа", обладающего холодоустойчивостью и высокой продуктивностью. Это дало возможность существенно продвинуть карповодство на север.
В течение многих лет В. С. Кирпичников принимал активное участие в борьбе с "лысенковщиной".
С начала 1970-х годов В. С. Кирпичников работал в Институте цитологии Академии наук и ежегодно приезжал на Камчатку, где проводил исследования по генетике лососевых рыб. Здесь он со своими коллегами и учениками собрал данные об особенностях генетической структуры этого вида тихоокеанских лососей. Лабораторная обработка материала дала важные научные результаты. Были сформированы представления о приспособительном значении высокого уровня генетической изменчивости популяций. Данные В. С. Кирпичникова о связи географической изменчивости нерки с направленными изменениями концентрации аллелей, кодирующих ферменты с различным температурным оптимумом активности, сыграли важную роль в преодолении крайностей нейтралистской концепции молекулярной биологии. Было показано, что многие жизненные формы рыб, различающиеся по составу и структуре белков, отличаются по физиологическим особенностям — по устойчивости к температурам, болезням и т. д.
13.Николай Владимирович Тимофеев-Ресовский (7 (20) сентября 1900 года, Москва — 28 марта 1981 года, Обнинск) — биолог, генетик. Основные направления исследований: радиационная генетика, популяционная генетика, проблемы микроэволюции.
В 1917- 1922 гг. учился — в 1-м Московском государственном университете, но диплома об окончании университета не успел получить.
В годы гражданской войны воевал в составе Красной армии, болел тифом.
В 1922—1925 исследователь в институте экспериментальной биологии под руководством Н. К. Кольцова. Преподаватель зоологии на биотехническом факультете Практического института в Москве, ассистент на кафедре зоологии у проф. Н. К. Кольцова в Московском медико-педагогическом институте
С начала 20-х годов участвовал в работе неформального семинара, организованного группой С. С. Четверикова в институте Н. К. Кольцова («Дрозсоор», или «совместное орание по поводу дрозофилы»), из которого вышли многие советские генетики.
Через год работы в генетической лаборатории Института экспериментальной биологии Николай Владимирович получил интересные научные результаты: изучая механизмы проявления генов, он пришел к выводу, что единичная мутация может вызывать множественные изменения во внешнем облике организма.
Как талантливый и перспективный исследователь в 1925 году был рекомендован Н. К. Кольцовым и Н. А. Семашко Оскару Фогту для работы в созданной им в Берлине лаборатории исследования мозга.
В 1925 году переехал на работу в Берлин. Вначале он работал научным сотрудником, но вскоре стал руководителем отдела генетики и биофизики в Институте исследований мозга в пригороде Берлина Бухе.
В 1930-е годы совместно с будущим лауреатом Нобелевской премии Максом Дельбрюком Тимофеев-Ресовский создал первую биофизическую модель структуры гена и предлагал возможные способы его изменения.
Весной 1937 года советское консульство отказалось в очередной раз продлевать Тимофеевым-Ресовским паспорта — тем самым настоятельно предлагая им вернуться в СССР. Однако, по словам Тимофеева-Ресовского, Н. К. Кольцов предупредил его, что по возвращении их скорее всего ждут «большие неприятности». В 1934, 1937 и 1938 гг. двое братьев Николая Владимировича — Дмитрий и Владимир — были по разным делам арестованы и расстреляны в 1938 г. Тимофеев-Ресовский отказался вернуться в Советский Союз и продолжал жить и работать в гитлеровской Германии, за что после Второй мировой войны он был в сталинском СССР осуждён за измену Родине как невозвращенец.
Научно-исследовательская деятельность Тимофеева-Ресовского в предвоенной Германии внесла фундаментальный вклад в ряд областей современной биологии. Здесь он открыл и обосновал фундаментальные положения современной генетики развития и популяционной генетики. Он также принял участие в создании основ современной радиационной генетики.
13 сентября 1945 г. Тимофеев-Ресовский был задержан опергруппой НКВД города Берлина, этапирован в Москву и приговорен к 10 годам лишения свободы по обвинению в измене Родине.
Он отбывал срок в одном из уральских лагерей ГУЛага. Но в 1947 г. в связи с советскими работами по созданию атомной бомбы как специалиста по радиационной генетике Тимофеева-Ресовского перевели из лагеря на «Объект 0211» в Челябинской области (теперь — город Снежинск) для работы по проблемам радиационной безопасности. К этому времени он был при смерти от голода. С 1947 г. Тимофеев-Ресовский заведовал биофизическим отделом «Объекта 0211», в 1951 г. он был освобожден из заключения, а в 1955 г. с него была снята судимость. В 1955—1964 Тимофеев-Ресовский заведовал отделом биофизики в Институте биологии УФАН СССР в Свердловске. Одновременно он читал несколько циклов лекций по влиянию радиации на организмы и по радиобиологии на физическом факультете Уральского университета и работал на биостанции, основанной им на озере Большое Миассо́во в Ильменском заповеднике.
Докторскую диссертацию Тимофеев-Ресовский смог защитить в Свердловске только в 1963 году, а докторский диплом получил в 1964 году после смещения Хрущёва и реабилитации генетики.
Методы генетики
Генетика, как любая наука имеет свои методы исследований. В ходе развития и накопления знаний появляются новые способы изучения наследственности и изменчивости организмов. Многообразие методов генетики определяется разнообразием объектов и структур изучения. К классическим методам генетики можно отнести:
1.Гибридологический метод — скрещивание (гибридизация) организмов, отличающихся друг от друга по одному или нескольким признакам. Потомки от таких скрещиваний называются гибридами.
2.Генеалогический метод (метод родословных) — изучение наследования какого-либо признака у человека в ряде поколений. Позволяет прогнозировать вероятность передачи потомкам наследственных заболеваний.
3.Близнецовый метод — изучение проявления признаков у однояйцовых близнецов. Позволяет оценить роль внешней среды в формировании фенотипа.
4.Цитогенетический метод — изучение количества, формы и размеров хромосом. Позволяет обнаружить хромосомные и геномные мутации.
5.Биохимический метод — изучение наследственно обусловленных нарушений обмена веществ. Позволяет обнаружить генные мутации.
6.Популяционный метод — изучение частоты встречаемости генов и генотипов в популяциях. Дает информацию о степени гетерозиготности и полиморфизма (неоднородности) человеческих популяций.
На современном этапе развития успехи молекулярной генетики создали предпосылки для возникновения четырех новых направлений генетических исследований преимущественно прикладного характера, основная цель которых изменять геном организма в желаемую сторону. Наиболее быстро из этих направлений развивались: 1.генетическая инженерия и
2.генетика соматических клеток.
Генетическая инженерия подразделяется на генную (искусственный перенос отдельных генов) и хромосомную (искусственный перенос хромосом и их фрагментов). Методы генной инженерии, развитие которых началось в 1972 в США в лаборатории П. Берга, широко используются для промышленного производства высококачественных биопрепаратов, используемых в медицине (инсулин человека, интерферон, вакцины против гепатитов В, для диагностики СПИД и т. д.). С их помощью получены разнообразные трансгенные животные. Получены растения картофеля и подсолнечника, обогащенные запасным белком, кодируемым геном бобовых, растения подсолнечника, обогащенные белком, кодируемым геном кукурузы. Очень перспективны работы, ведущиеся во многих лабораториях мира, по переносу генов азотфиксации из почвенных бактерий в сельскохозяйственные растения. Делаются попытки излечения наследственных заболеваний путем введения в организм пациента «здорового» гена для замещения им мутантного, являющегося причиной болезни. Достижения в технологии рекомбинантных ДНК, сделавшие возможным выделение многих генов др. организмов, а также расширение знаний о регуляции их экспрессии позволяют надеяться на реализацию этой, казавшейся прежде фантастической, идеи.
Метод хромосомной инженерии позволяет пересадить в яйцеклетку млекопитающего с удаленным ядром диплоидное ядро соматической клетки и ввести такую яйцеклетку в матку самки, гормонально подготовленную к имплантации. В этом случае родится потомок, генетически идентичный особи, от которой взята соматическая клетка. Таких потомков можно получить от этой особи неограниченное число, т. е. генетически клонировать ее.
2.ГЕНЕТИКА СОМАТИЧЕСКИХ КЛЕТОК ЗАНИМАЕТСЯ исследованиями, проводимыми на соматических клетках растений, животных и человека. Селекциейклеток растений — продуцентов лекарственных алкалоидов (руты душистой, раувольфии), в сочетании с мутагенезом содержание этих алкалоидов в клеточной массе повышено в 10-20 раз. Селекцией клеток на питательных средах и последующей регенерацией целых растений из клеточного каллуса выведены сорта ряда возделываемых растений, устойчивые к различным гербицидам и засолению почвы. Гибридизацией соматических клеток разных видов и родов растений, половая гибридизация которых невозможна или очень затруднена, и последующей регенерацией из клеточного каллуса созданы разные гибридные формы (капуста — турнепс, культурный картофель — дикие его виды и т. п.).
Другое важное достижение генетики соматических клеток животных — создание гибридов, на основе которых получают моноклональные антитела, служащие для создания высокоспецифических вакцин, а также для выделения необходимого фермента из смеси ферментов.
Весьма перспективны для практики еще два молекулярно-генетических направления — 3. сайт-специфичный мутагенез и 4.создание антисмысловых РНК. Сайт-специфичный мутагенез (индукция мутаций определенного выделенного рестриктазами гена или его комплементарной ДНК, и затем включение мутировавшего гена в геном для замены им его немутантного аллеля) впервые позволил индуцировать желательные, а не случайные генные мутации, и уже успешно применяется для получения направленных генных мутаций у бактерий и дрожжей.
Антисмысловые РНК, возможность получения которых впервые была показана в 1981 работающим в США японским иммунологом Д. Томизавой, могут использоваться для целенаправленного регулирования уровня синтеза определенных белков, а также для направленного ингибирования онкогенов и вирусных геномов. Исследования, проведенные по этим новым генетическим направлениям, были нацелены преимущественно на решение прикладных задач. Вместе с тем они внесли фундаментальный вклад в представления об организации генома, структуре и функциях генов, взаимоотношениях генов ядра и клеточных органелл и др.
Основные этапы истории генетики
Зачатки генетики можно проследить ещё в доисторические времена, когда одомашнивались животные и культивировались растения. Уже на вавилонских глиняных табличках указывали возможные признаки при скрещивании лошадей.
Различные умозрительные представления о наследственности и изменчивости высказывались античными философами и врачами. В большинстве своем эти представления были ошибочными, но иногда среди них появлялись и гениальные догадки. Так, римский философ и поэт Лукреций Кар писал в своей знаменитой поэме «О природе вещей» о «первоначалах» (наследственных задатках), определяющих передачу из поколения в поколение признаков от предков к потомкам, о происходящем при этом случайном комбинировании («жеребьевке») этих признаков, отрицал возможность изменения наследственных признаков под влиянием внешних условий.
Однако подлинно научное познание наследственности и изменчивости началось лишь спустя много столетий, когда было накоплено множество точных сведений о наследовании различных признаков у растений, животных и человека. Число таких наблюдений, проведенных преимущественно практиками-растениеводами и животноводами, особенно возросло в период с середины 18 до середины 19 века. Наиболее ценные данные были получены И. Кельрейтером и А. Гертнером (Германия), О. Сажрэ и Ш. Ноденом (Франция), Т. Найтом (Англия). На основании межвидовых и внутривидовых скрещиваний растений они обнаружили ряд важных факторов, касающихся усиления разнообразия признаков в потомстве гибридов, преобладания у потомков признаков одного из родителей и т. п. Сходные обобщения сделал во Франции П. Люка (1847-1850), собравший обширные сведения о наследовании различных признаков у человека. Тем не менее, четких представлений о закономерностях наследования и наследственности вплоть до конца 19 века не было за одним существенным исключением. Этим исключением была замечательная работа Г. Менделя установившего в опытах по гибридизации сортов гороха важне
