Практическое занятие №2
1. Основные вопросы темы
2.1. Общая схема источников и путей использования глюкозы в организме.
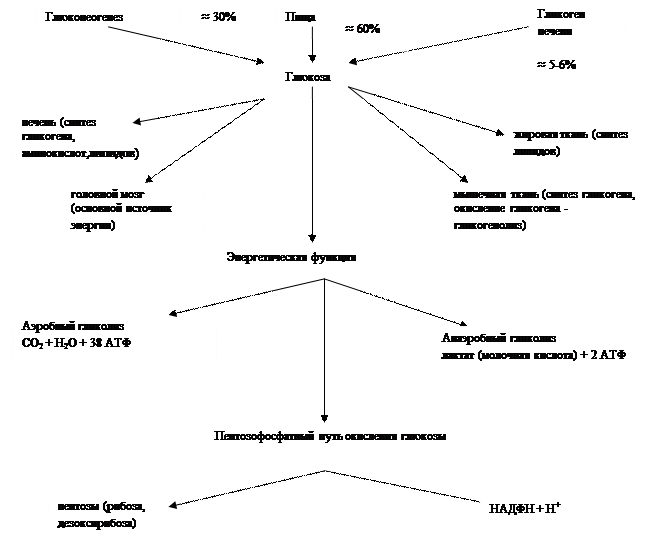
2.2. Гликоген – свойства, биосинтез и мобилизация гликогена.
Гликоген – животный крахмал, главный резервный гомополисахарид. Значительная часть глюкозы, поступающей в кровь, превращается в гликоген – запасный полисахарид, используемый в интервалах между приемами пищи в качестве источника глюкозы. Наибольшая концентрация гликогена обнаруживается в печени 2 – 6%, а в мышцах содержится 0,5 – 2%. В клетке гликоген находится не в растворенном состоянии, а в виде гранул. Гликоген имеет высокую молекулярную массу (1∙106 - 2∙108) и содержит до 1 млн. остатков глюкозы, соединенных 1,4 и 1,6 - гликозидными связями. Гликоген с йодом дает красно – бурое окрашивание.
Синтез гликогена.
Происходит тогда, когда после использования глюкозы остается её часть и она запасается в организме в виде
гликогена.
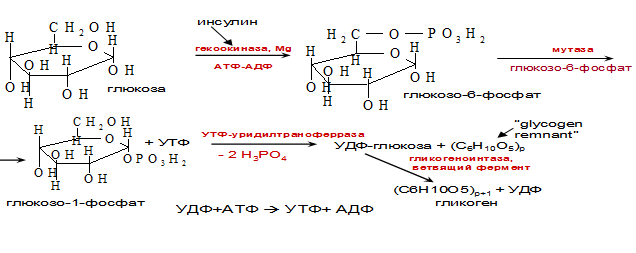
Фермент гликогенсинтаза участвует в образовании α-1,4-гликозидных связей, ветвящий фермент в образовании α-1,6-гликозидных связей. Образовавшиеся молекулы гликогена обладают низкой растворимостью и, следовательно, низким влиянием на осмотическое давление в клетке по сравнению с глюкозой, это объясняет то, что в клетке депонируется гликоген, а не глюкоза.
Распад гликогена.
Распад гликогена с образованием глюкозы происходит в период между приемами пищи, физической работе, при стрессе.
Пути мобилизации гликогена:
1. фосфоролитический.
2. амилолитический путь распада гликогена происходит при участии фермента амилазы.
Фосфоролитический путь – основной путь распада гликогена с образованием глюкозы:
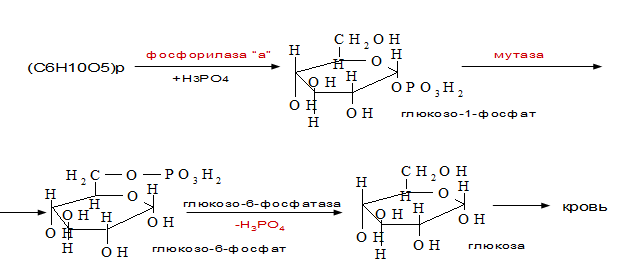 В мышечной ткани нет фермента глюкозо-6-фосфатазы, поэтому гликоген мышц не распадается с
В мышечной ткани нет фермента глюкозо-6-фосфатазы, поэтому гликоген мышц не распадается с
образованием глюкозы, а окисляется или аэробным или анаэробным путем с освобождением энергии. Через
10-18 часов после приема пищи запасы гликогена в печени значительно истощаются.
2.3. Гликогенозы и агликогенозы.
Гликогенозы (болезни накопления гликогена) обусловлены дефектом ферментов, участвующих в распаде гликогена. Например, болезнь Гирке связана с отсутствием фермента глюкозо-6-фосфатазы, при этом наблюдается избыточное накопление гликогена в печени, гипогликемия и ее последствия. Болезнь Мак-Ардла: причина - отсутствие фосфорилазы в мышечной ткани. При этом уровень глюкозы в крови в норме, но наблюдается слабость мышечной ткани и снижена способность выполнять физическую работу. Болезнь Андерсена связана с дефектом, ветвящего фермента, что приводит к накоплению гликогена в печени с очень длинными наружными и редкими точками ветвления, вследствие этого – желтуха, цирроз печени, печеночная недостаточность, летальный исход (неразветвленный гликоген разрушает гепатоциты).

Агликогенозы – заболевания, возникающие в результате дефекта гликогенсинтазы. В печени и других тканях больных наблюдают очень низкое содержание гликогена. Это проявляется резко выраженной гипокликемией в постабсорбтивном периоде. Характерный симптом – судороги по утрам.
2.4. Содержание глюкозы в крови. Гипо-, гипергликемия, глюкозурия и причины их возникновения.
Концентрация глюкозы в крови поддерживается в течение суток на постоянном уровне 3,3-5,5 ммоль/л. После приема пищи уровень глюкозы возрастает в течение часа до 8 ммоль/л, а затем возвращается к норме. В организме постоянный уровень глюкозы в крови поддерживается благодаря существованию нейрогуморальных механизмов. Основным показателем состояния углеводного обмена служит содержание глюкозы в крови и моче.
ГИПЕРГЛИКЕМИЯ- состояние, при котором уровень глюкозы выше нормы. Причины:
1. Физиологические - алиментарная, эмоциональная.
2. Патологические – сахарный диабет; стероидный диабет (Иценко-Кушинга) – гиперпродукция глюкокортикоидов коры надпочечников; гиперпродукция адреналина, глюкагона, СТГ тироксина.
ГИПОГЛИКЕМИЯ - состояние, при котором уровень глюкозы ниже нормы. Причины:
1. Сниженный выход глюкозы: заболевания печени, эндокринные заболевания (дефицит гормона роста, кортизола), наследственные метаболические нарушения (дефицит гликогенсинтетазы, галактоземия, непереносимость фруктозы, печеночные формы гликогенозов).
2. Увеличенная утилизации глюкозы: снижение запасов жиров (нарушение питания), нарушение окисления жирных кислот, гиперплазия β-кл. подж. железы, передозировка инсулина, болезнь Аддисона – гипопродукция глюкокортикоидов.
ГЛЮКОЗУРИЯ – появление сахара в моче. Если уровень глюкозы в крови составляет 8-10 ммоль/л, то нарушается
почечный порог для глюкозы и она появляется в моче. Причины:
1. физиологические:
- алиментарная глюкозурия
- глюкозурия беременных
- нейрогенная на почве стрессовых состояний
2. патологические:
- сахарный диабет
- острый панкреатит
- острые инфекционные заболевания
2.5. Регуляция уровня глюкозы в крови. Роль ЦНС, механизм действия инсулина, адреналина, глюкагона,
СТГ, глюкокортикоидов, тироксина и их влияние на состояние углеводного обмена.
Ведущее значение в регуляции углеводного обмена принадлежит центральной нервной системе. Снижение уровня глюкозы в крови приводит к повышенной секреции адреналина, глюкагона, которые, поступая в орган-мишень для этих гормонов (печень), узнаются рецепторами мембран клеток печени и активируют фермент мембраны аденилатциклазу, запуская механизм, приводящий к распаду гликогена с образованием глюкозы.
Схема механизма взаимодействия адреналина и глюкагона с клеткой:
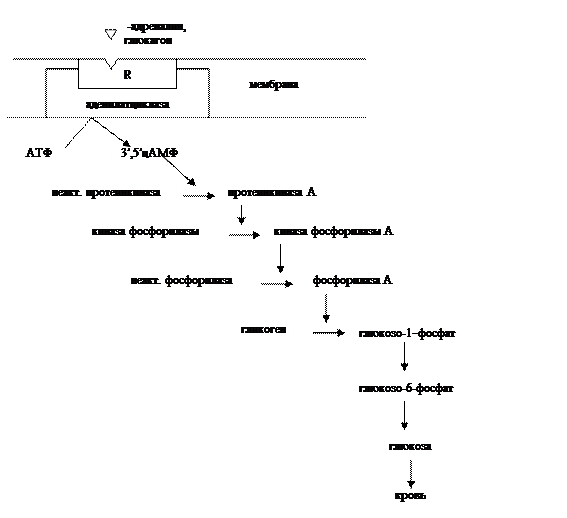

Адреналин – повышает уровень глюкозы за счет активации фермента фосфорилазы (аденилатциклазная система), которая приводит к распаду гликогена с образованием глюкозы, блокирует фермент гликогенсинтазу, т.е. синтез гликогена.
Глюкагон – действует подобно адреналину, но плюс к этому активирует ферменты глюконеогенеза.
Глюкокортикоиды – повышают уровень глюкозы крови, являясь индукторами синтеза ферментов глюконеогенеза.
СТГ актвирует глюконеогенез, тироксин активирует инсулиназу, расщепляющую инсулин, влияет на всасывание глюкозы в кишечнике.
Инсулин – единственный гормон, понижающий уровень глюкозы в крови, за счет:
1. повышает проницаемость клеточных мембран для глюкозы в клетках жировой и мышечной ткани, под его влиянием белки-транспортеры ГЛЮТ-4 перемешаются из цитоплазмы в мембрану клетки, где соединяются с глюкозой и транспортируют её во внутрь клетки.
2. активирует гексокиназу, фруктокиназу, пируваткиназу (стимулирует гликолиз).
3. активирует гликогенсинтетазу (стимулирует синтез гликогена).
4. активирует дегидрогеназу пентозо-фосфатного пути.
5. по механизму хронической регуляции является индуктором синтеза гексокиназы и репрессором синтеза ферментов глюконеогенеза (блокирует глюконеогенез).
6. 30% углеводов превращает в липиды.
7. стимулирует ЦТК, активируя фермент синтетазу, которая катализирует реакцию взаимодействия ацетил-КоА с ЩУК
| |
2. Основные вопросы темы
2.1. Аэробный распад – основной путь катаболизма глюкозы у человека. Физиологическое значение.
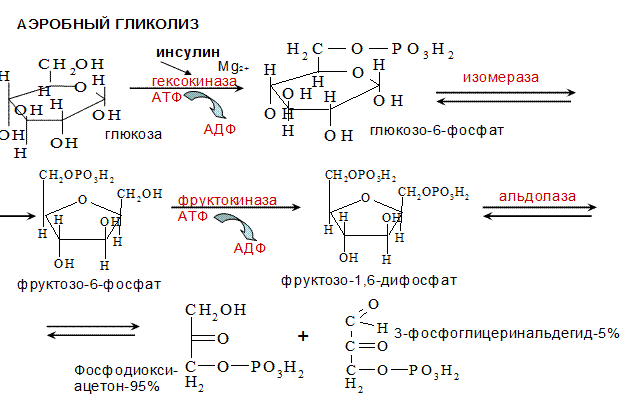
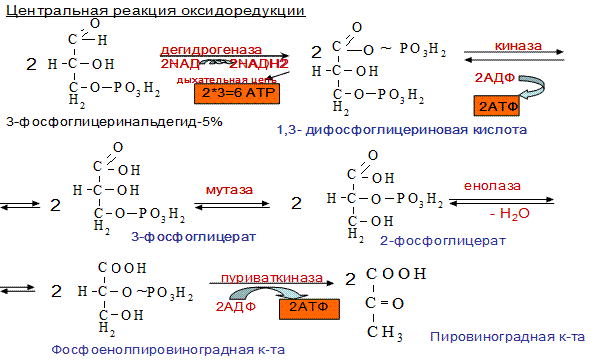
АЭРОБНЫЙ ГЛИКОЛИЗ – процесс окисления глюкозы до СО2 и Н2О, протекающий в присутствии кислорода. Все ферменты, катализирующие реакции находятся в цитозоле клетки.
Выделяют 2 этапа:
1. Подготовительный – глюкоза фосфорилируется и расщепляется на 2 молекулы фосфотриоз. Используются 2 молекулы АТФ.
2. Этап, сопряженный с синтезом АТФ. Фосфотриозы превращяются в ПВК, которая далее окисляется до СО2 и Н2О ( ЦТК). Таким образом, выход АТФ – 38 молекул.
Основное физиологическое значение – использование энергии, которая освобождается в этом процессе для синтеза АТФ. Метаболиты гликолиза используются для синтеза новых соединений (фр-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата – структурного компонента нуклеозидов; 3-фосфоглицерат включается в синтез аминокислот: серин, глицин, цистеин). Являются субстратами для НАД-зависимых дегидрогеназ дых. цепи (глицеральдегид -3-фосфат, пируват, изоцитрат, α-кетоглутарат, малат). В печени и жировой ткани ацетил-КоА, образующийся из ПВК, используется как субстрат при биосинтезе жирных кислот, холестерина.
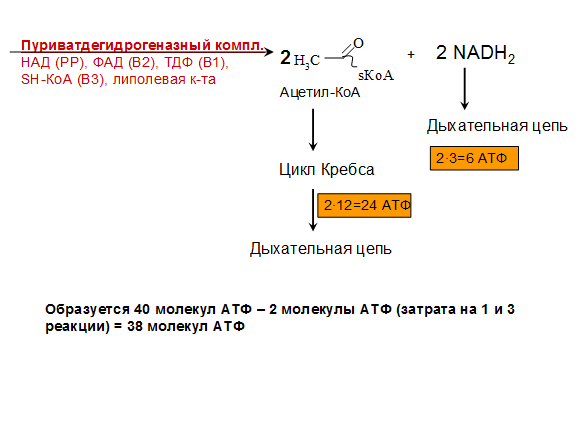
В1 недостаточность – известно что это водорастворимый витамин – тиамин – антиневритный, входит в состав как минимум 3 ферментов. Например, в виде ТДФ участвует в пируватдегидрогеназном комплексе (окисление ПВК до ацетил КоА). При его отсутствии из ацетил-КоА, в частности не образуется ацетилхолин, вследствии чего, возникают полиневриты, в основе которых лежат дегенеративные изменения нервов, затем паралич (Бери-бери), нарушения со стороны сердечно-сосудистой деятельности – нарушения ритма сердца, увеличения его размеров, боли, со стороны ЖКТ – снижение кислотности, потеря аппетита, атония кишечника.
2.2.Анаэробный распад глюкозы, авитаминоз В1. Биологическая роль. Эффект Пастера.
АНАЭРОБНЫЙ ГЛИКОЛИЗ – процесс расщепления глюкозы с образованием конечного продукта лактата. Он протекает без использования кислорода и поэтому не зависит от работы митохондриальной дыхательной цепи. АТФ образуется за счет субстратного фосфорилирования (2 АТФ). Протекает в мышцах, в первые минуты мышечной работы, в эритроцитах (в которых отсутствуют митохондрии), а также в разных органах в условиях ограниченного снабжения их кислородом, в том числе в опухолевых клетках. Этот процесс служит показателем повышенной скорости деления клеток при недостаточной обеспеченности их системой кровеносных сосудов.
Сходство анаэробного и аэробного гликолиза заключается в том, что до стадии образования ПВК эти процессы протекают одинаково при участии тех же ферментов.


 СН3 ЛДГ СН3
СН3 ЛДГ СН3



 Глюкоза С=О 2 Н-С-ОН
Глюкоза С=О 2 Н-С-ОН
СООН СООН
ПВК 2 НАДН2 2НАД лактат
Энергетический баланс анаэробного окисления глюкозы: образование 2 АТФ.
Основное физиологическое значение – использование энергии, которая освобождается в этом процессе для синтеза АТФ. Метаболиты гликолиза используются для синтеза новых соединений (фр-6-фосфат и глицеральдегид-3-фосфат участвуют в образовании рибозо-5-фосфата – структурного компонента нуклеозидов; 3-фосфоглицерат включается в синтез аминокислот: серин, глицин, цистеин).
ЭФФЕКТ ПАСТЕРА. Заключается в угнетении дыханием (О2) анаэробного гликолиза, т.е. происходит переключение с аэробного гликолиза на анаэробное окисление. Если ткани снабжены О2, то 2НАДН2, образовавшийся в процессе центральной реакции оксидоредукции, окислится в дыхательной цепи, поэтому ПВК не превращается в лактат, а в ацетил-КоА, который вовлекается в ЦТК.
2.3. Глюконеогенез и его значение.
Это процесс синтеза глюкозы из веществ неуглеводной природы. Процесс протекает в печени и менее интенсивно в корковом веществе почек, а также в слизистой кишечника. Эти ткани могут обеспечивать синтез 80-100 г глюкозы в сутки.
Первичные субстраты – лактат, аминокислоты, глицерол. Их включение в глюконеогенез зависит от физиологического состояния организма:
лактат – постоянно;
глицерол – высвобождается при гидролизе жиров в период голодания или при длительной физической нагрузке;
аминокислоты – образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
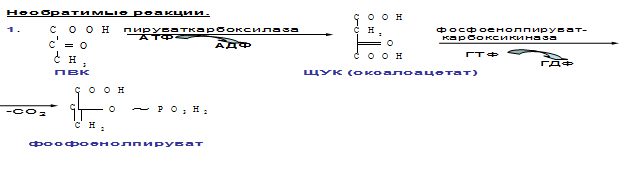
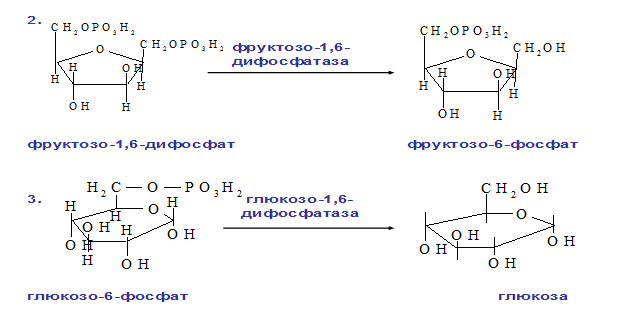
Если гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях. Процесс идет обратно анаэробному гликолизу за исключением 3-х необратимых реакций:
1. Пируваткиназная – образование фосфоенолпирувата из ПВК происходит в ходе 2-х реакций, первая из кот. протекает в митохондриях. ПВК транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалацетата (ЩУК). Фермент-пируваткарбоксилаза, коферментом которым является биотин. Реакция протекает с использование АТФ. Затем оксалацетат (в цитозоле) превращается в фосфоенолпируват входе реакции, катализируемой фосфоенолпируваткарбоксилазой – ГТФ-зависимым ферментом ( -СО2, ГТФ → ГДФ).
2. Фосфофруктокиназная: ФР-1,6-дифосфат →Фр-6-фосфат под действием фермента фруктозо-1,6-бифосфатаза.
3. Гексокиназная: Гл-6-фосфат→ Глюкоза под действием фермента Гл-6-фосфатазы.
ЗНАЧЕНИЕ – поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок.
РЕГУЛЯЦИЯ: инсулин – тормозит синтез ферментов; глюкокортикоиды – индуцируют синтез ферментов; СТГ – повышает активность ферментов глюконеогенеза.
2.4. Взаимосвязь гликолиза в мышцах и глюконеогенеза в печени (цикл Кори).
ЦИКЛ КОРИ.
(взаимосвязь гликолиза в мышцах и глюконеогенеза в печени).
Схема:

ЗНАЧЕНИЕ:
1. Регуляция постоянного уровня глюкозы в крови.
2. Обеспечивает утилизацию лактата.
3. Предотвращает накопление лактата (снижение рН - лактоацидоз).
4. Экономичное использование углеводов организмом.
5. Регуляция обмена углеводов осуществляется на уровне тканей – кровь, печень, мышцы.
2.5. Методы определения глюкозы в крови, диагностическое значение.
Существует огромное число методов исследования.
- Редуктометрические – основаны на свойствах сахаров восстанавливать соли тяжелых металлов в щелочной
среде (титрометрический).
- Колориметрические – основаны на определение интенсивности окраски соединений, образующихся при
взаимодействии глюкозы с определенными веществами (ортотолуидиновый).
- Самым современным является энзимотический – основанный на действии фермента глюкооксидазы,
окисляющий глюкозу до глюконовой кислоты. Данный метод лежит в основе определения уровня
глюкозы прибором «One Touch».
|
2.1. Взаимопревращения моносахаридов. Причины галактоземии, фруктоземии.
Метаболизм фруктозы и галактозы включает пути использования их для синтеза других веществ
(гетерополисахаридов, лактозы) и участие в энергообеспечении организма. Всосавшись в желудочно-кишечном
тракте, фруктоза в мышечной ткани, в почках, в жировой ткани проходит главный путь.
Фруктоза
 АТФ
АТФ
гексокиназа
АДФ

 Фруктозо-6-фосфат глюкозо-6-фосфат глюкоза
Фруктозо-6-фосфат глюкозо-6-фосфат глюкоза

 АТФ
АТФ
6-фруктокиназа Н2О Н3РО4
АДФ
Фруктозо-1,6-бисфосфат
 |
Глицеральдегидтрифосфат

Гликолиз
В печени же существует другой путь превращения фруктозы:
АТФ АДФ
 Фруктоза фруктозо-1-фосфат
Фруктоза фруктозо-1-фосфат
 |
фруктокиназа
расщепляется
 |  |
диоксиацетонфосфат + Д - глицероальдегид
 киназа
киназа
глицероальдегид-3-фосфат
 |
по пути гликолиза
Фруктозурия – отсутствует фермент фруктокиназа, которая в печени катализирует превращения фруктозы во фруктозо-1-фосфат. Это приводит к фруктоземии и очень быстро фруктоза появляется в моче – фруктозурия, т.к. для фруктозы почечный порог равен 0,73 ммоль/л. Вследствие того, что фруктоза входит в состав дисахарида сахарозы, то после приема пищи содержащей её также наблюдается тошнота, рвота, понос, боли в животе, приступы судорог.
Галактоза образуется в кишечнике в результате гидролиза лактозы. Всосавшаяся галактоза в печени проходит следующий путь:
Галактоза

 АТФ
АТФ
галактокиназа
АДФ
Галактозо-1-фосфат
+ УДК-глюкоза 

 УДФ-галактоза уридилтрансфераза
УДФ-галактоза уридилтрансфераза
Глюкозо-1-фосфат
 УДФ-глюкоза
УДФ-глюкоза

 Глюкозо-6-фосфат гликолиз
Глюкозо-6-фосфат гликолиз
Гликоген - Н3РО4
Глюкоза
Галактоземия – наследственное заболевание, связанное с отсутствием фермента – галактозо-1-фосфатуридилтрансферазы, который катализирует превращения галактозо-1-фосфат в глюкозо-1-фосфат. Это приводит к накоплению в крови, в моче галактозы и галактозо-1-фосфат, галактитола, которые оказывают токсическое действие на клетки печени, головного мозга, глаз. После приема молока (галактоза входит в состав лактозы) у ребенка наблюдаются: рвота, тошнота, понос, боли в животе. Если не исключить молоко из рациона ребенка это приводит к катаракте, циррозу печени и селезенки, замедлению психического развития.
Лечение галактоземии и фруктозурии: исключить из рациона ребенка продукты, содержащие галактозу и
фруктозу.
2.2.Пентозофосфатный путь превращений глюкозы. Окислительные реакции (до стадии рибулозо-5-фосфата).
Распространение и физиологическое значение.
Пентозофосфатный путь является альтернативным путем окисления глюкозы. Это путь окисления глюкозы путем укорочения углеродной цепочки на один углеродный атом. Пентозофосфатный путь не приводит к синтезу АТФ.
В пентозофосфатном пути различают два этапа:
1. Окислительный путь включает две реакции дегидрирования с участием кофермента НАДФ и реакцию декарбоксилирования. В результате образуется НАДФН2 и пентозы (рибозро-5-фосфат).
2. Неокислительный путь служит для синтеза пентоз. Реакции этого пути обратимы, поэтому из пентоз могут образовываться гексозы. Промежуточные продукты (фруктозо-6-фосфат, глицеро-альдегид-3-фосфат) могут включаться в пути аэробного и анаэробного окисления. Знать химизм окислительного этапа.
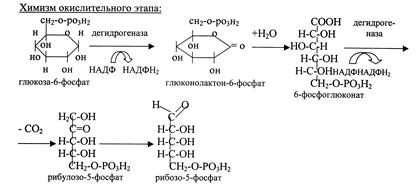
Таким образом, в результате пентозофосфатного пути окисления глюкозы образуются пентозы, необходимые для синтеза нуклеиновых кислот (ДНК, РНК), коферментов (НАД, НАДФ, ФМН, ФАД), а также восстановленная форма НАДФ, водороды которого необходимы для восстановительных синтезов (синтез высших жирных кислот, холестерола, гормонов коры надпочечников, половых гормонов, провитаминов группы Д, желчных кислот), участвует в обезвреживании лекарственных веществ и ядов в печени. Этот путь окисления функционирует в печени, в жировой ткани, молочной железе, коре надпочечников, а также в быстро растущих, регенерирующихся тканях.
2.3. Влияние этилового спирта на углеводный обмен.
Катаболизм этанола осуществляется главным образом в печени (75-98%). Основную роль в метаболизме этанола играет цинксодержащий фермент НАД+- зависимый фермент – алкогольдегидрогеназа, локализующийся в цитозоле и митохондриях печени (95%). В ходе реакции происходит дегидрирование этанола, образуются ацетальдегид и восстановленный НАДН. Алкогольдегидрогеназа катализирует обратимую реакцию, направление которой зависит от концентрации ацетальдегида и соотношения НАДН/НАД+ в клетке.
дегидрогеназа дегидрогеназа
С2Н5ОН → Н3С-СОН → СН3СООН → Н3СОSKoA → ЦТК
НАД → НАДН2 НАД → НАДН2
этанол ацетальдегид уксусная кислота ацетил КоА
При употреблении большого количества спирта количество НАД уменьшается, а НАДН2 увеличивается. Это приводит к уменьшению ПВК – основной предшественник образования глюкозы → гипогликемия, особенно когда запасы гликогена в печени и мышцах невелики (употребление алкоголя натощак, после физической нагрузки, у хронических алкоголиков); блокируется синтез глюкозы из лактата и аминокислот (глюконеогенез). Гипогликемия сказывается на функции мозга и может быть причиной потери сознания при алкогольном отравлении. Алкоголь не содержит витаминов. Алкоголики получают основную массу калорий со спиртом, в котором нет витамина В1. Характерная для них недостаточность тиамина проявляется в синдроме Вернике - Корсакова, сопровождается расстройствами функций нервной системы, психозами, потерей памяти (причина – сочетание недостатка тиамина и снижение активности тиаминзависимого фермента транскетолазы).
2.4. Сахарный диабет, биохимическая характеристика патогенеза.
Это заболевание, возникающее вследствие абсолютного или относительного дефицита инсулина. Сахарный диабет (СД) классифицируют с учетом различия генетических факторов и клинического течения на две основные формы: диабет I типа – инсулинзависимый (ИЗСД), и диабет II типа – инсулиннезависимый (ИНСД).
ИЗСД – заболевание, вызванное разрушением β-клеток островков Лангерханса поджелудочной железы, вследствие аутоиммунных реакций, вирусных инфекций (вирус оспы, краснухи, кори, эпидемический паротит, аденовирус). При СД снижено соотношение инсулин/глюкагон. При этом ослабевает стимуляция процессов депонирования гликогена и жиров, и усиливается мобилизация энергоносителей. Печень, мышцы и жировая ткань даже после приема пищи функционируют в режиме постабсорбтивного состояния.
Гипергликемия – повышение конц. глюкозы в крови.
Она обусловлена снижением скорости использования глюкозы тканями вследствие недостатка инсулина или снижения биологического действия инсулина в тканях-мишенях. При дефиците инсулина уменьшается количество белков-переносчиков глюкозы (ГЛЮТ-4) на мембранах инсулинзависимых клеток (жировой ткани мышц). В мышцах и печени глюкоза не депонируется в виде гликогена. В жировой ткани уменьшается скорость синтеза и депонирования жиров. Активируется глюконеогенез из аминокислот, глицерола и лактата.
Глюкозурия – выделение глюкозы с мочой.
В норме проксимальные канальцы почек реабсорбируют всю глюкозу, если ее уровень не превышает 8,9 ммоль/л. Повышение концентрации глюкозы в крови превышает концентрационный почечный порог, что становится причиной появления ее в моче.
Кетонемия – повышение концентрации в крови кетоновых тел.
Жиры не депонируются, а ускоряется их катаболизм. Повышается концентрация неэтерифицированных жирных кислот, которые захватывает печень и окисляет их до ацетил – КоА. Ацетил-КоА превращается в β-гидроксимасляную и ацетоуксусную кислоты. В тканях происходит декарбоксилирование ацетоацетата до ацетона, поэтому от больных исходит его запах. Увеличение концентрации кетоновых тел в крови (выше 20 мг/л) приводит к кетонурии. Накопление кетоновых тел снижает буферную емкость крои и вызывает ацидоз.
Дефицит инсулина приводит к снижению скорости синтеза белков и усилению их распада. Это вызывает повышение концентрации аминокислот в крови, которые дезаминируются в печени. Образующийся при этом аммиак вступает в орнитиновый цикл, что приводит к увеличению концентрации мочевины в крови и моче – азотемия.
Полиурия – повышенное мочеотделение (3-4л в сутки и выше), т.к. глюкоза повышает осмотическое давление.
Полидипсия – постоянная жажда, сухость во рту, вследствие потери воды.
Полифагия – испытывают голод, часто едят, но теряют в массе тела, т.к. глюкоза не является источником энергии - «голод среди изобилия».
ИНСД – возникает в результате относительного дефицита инсулина вследствие:
- нарушения секреции инсулина
- нарушения превращения проинсулина в инсулин
- повышения катаболизма инсулина
-дефекта рецептора инсулина, повреждения внутриклеточных посредников инсулинового сигнала.
Поражает людей старше 40 лет, характеризуется высокой частотой семейных форм. Главная причина поздних осложнений сахарного диабета – гипергликемия, которая приводит к повреждению кровеносных сосудов и нарушению функций различных тканей и органов. Одним из основных механизмов повреждения тканей при сахарном диабете является гликозилирование белков, приводящее к изменению их конформации и функций. Макроангиопатии проявляются в поражении крупных и средних сосудов сердца, мозга, нижних конечностей (гангрена). Микроангиопатия является результатом повреждения капилляров и мелких сосудов и проявляется в форме нефро-, нейро- и ретинопатии. В возникновении микроангиопатий определенную роль играет гликозилирование белков, что приводит к возникновению нефропатии (нарушение функции почек) и ретинопатии (вплоть до потери зрения).
Коллаген составляет основу базальных мембран капилляров. Повышенное содержание гликозилированного коллагена ведет к уменьшению его эластичности, растворимости, к преждевременному старению, развитию контрактур. В почках такие изменения приводят к запустению клубочков и хронической почечной недостаточности.
Гликозилированные липопротеины, накапливаясь в сосудистой стенке, приводят к развитию гиперхолестеринемии и липидной инфильтрации. Они служат основой атером, происходит нарушение сосудистого тонуса, что приводит к атеросклерозу.
2.5.Проба на толерантность к глюкозе.
После приема пищи концентрация глюкозы может достигать 300-500 мг/дл и сохраняется на высоком уровне в постабсорбтивном периоде, т.е. снижается толерантность к глюкозе и наблюдается в случаях скрытой формы сахарного диабета. В этих случаях у людей отсутствуют клинические симптомы, характерные для СД, а концентрация глюкозы натощак соответствует норме.
Для выявления скрытой формы сахарного диабета проводится оральный тест на толерантность к глюкозе. Для этого определяют натощак содержание глюкозы в крови. После этого исследуемый получает нагрузку глюкозой из расчета 1г на кг массы, затем каждые 30 минут в течение 3-х часов определяют уровень глюкозы в крови. Результаты представляют в виде кривой.
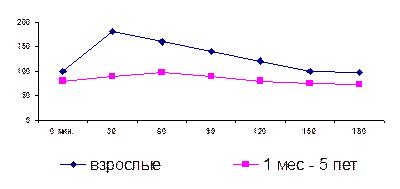 |
| |
