Функции белков плазмы крови
1. Белки поддерживающие коллоидно-осмотическое (онкотическое)давление и тем самым постоянный объем крови.
2. Белки определяют вязкость крови и сохраняют устойчивость эритроцитов и лейкоцитов в кровотоке.
3. Белки участвуют в регуляции кислотно-щелочного равновесия (белковая буферная система).
4. Белки выполняют транспортную функцию. Они транспортируют углеводы, липиды, гормоны, лекарства.
5. Белки удерживают в связанном состоянии и транспортируют катионы Са2+, Fe2+, Mg2+, Сu2+, препятствуют их потере с мочой.
6. Специализированные белки участвуют в свертывании крови (фибриноген, протромбин).
7. Белки выполняют защитную функцию. Иммуноглобулины участвуют в реакциях гуморального иммунитета.
8. Белки являются резервом аминокислот.
Альбумины.
На долю альбуминов приходится 55 – 60% белков плазмы крови. Молекулярная масса 70 тыс Да. Содержание альбуминов в крови – 40 – 50 г/л. Период полураспада 7 дней.
Альбумины поддерживают коллоидно-осмотическое давление и регулируют обмен жидкостей между кровью и тканями.
Снижение концентрации альбумина в сыворотке крови ниже 30 г/л сопровождается уменьшением онкотичекого давления крови и возникновением онкотического давления крови и возникновением отеков.
Функции альбуминов: транспорт неэстерифицированных жирных кислот, желчных кислот, желчных пигментов (билирубин), стероидные гормоны, ионы Са2+, многие лекарства – сульфаниламиды, пенициллин, дикумарин, аспирин.
Глобулины.
Глобулины делят на 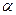 1,
1, 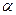 2,
2, 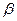 и
и 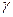 -глобулины.
-глобулины.
Фракция 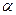 1-глобулинов.
1-глобулинов.
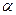 1 – гликопротеин кислый – орозомукоид, М.М. 40 кД, концентрация 55 – 100 мг/100 мл.
1 – гликопротеин кислый – орозомукоид, М.М. 40 кД, концентрация 55 – 100 мг/100 мл.
Функция – неспецифический транспорт гормонов.
Концентрация возрастает при воспалении, травле, ревматоидном артрите, некоторых опухолях.
Ретинолсвязывающий белок – транспорт витамина А. М.М. 21 кД, концентрация 3 – 6 мг/100 мл. синтезируется в гепатоцитах, [конц.] 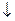 при патологии почек и печени.
при патологии почек и печени.
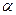 1-антитрипсин – альфа1-глобулин, синтезируется в печени, М.М. 54 кД, ингибитор протеолитических ферментов.
1-антитрипсин – альфа1-глобулин, синтезируется в печени, М.М. 54 кД, ингибитор протеолитических ферментов.
Концентрация 200 – 400 мг/ 100 мл = 2 – 4 г/л.
Врожденная недостаточность сопровождается легочной эмфиземой, циррозом печени у детей.
Альфа - 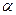 1 – антитрипсин инактивирует элластазу (элластаза – это фермент расщепляющий эластин, этого белка много в легочной ткани). Когда
1 – антитрипсин инактивирует элластазу (элластаза – это фермент расщепляющий эластин, этого белка много в легочной ткани). Когда 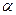 1-антипротеазы неактивны, повышается активность элластазы. У таких людей развивается эмфизема легких. Такое бывает в старости, у музыкантов. При генетическом дефекте такое заболевание бывает у детей.
1-антипротеазы неактивны, повышается активность элластазы. У таких людей развивается эмфизема легких. Такое бывает в старости, у музыкантов. При генетическом дефекте такое заболевание бывает у детей.
Увеличение концентрации 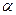 1-антитрисина наблюдается при остром гепатите, циррозе печени, гематоме, беременности.
1-антитрисина наблюдается при остром гепатите, циррозе печени, гематоме, беременности.
Тироксинсвязывающий белок – связывает и транспортирует гормон щитовидной железы – тироксин. М.М. 58 кД, концентрация 1 – 2 мг/100 л.
Транскортин – связывает и транспортирует кортикостероиды. М.М. 52 кД, концентрация 3 – 3,5 мг/100 мл.
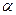 1-фетоглобулин =
1-фетоглобулин = 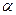 1-фетопротеин – белок плода. Синтезируется в печени, концентрация 8 – 9 г/л. функция – поддержание онкотического давления крови. В норме здоровых людей не содержится. Содержание увеличивается при остром гепатите, циррозе печени, гепатоме, беременности. Повышение концентрации – ранний признак рака печени.
1-фетопротеин – белок плода. Синтезируется в печени, концентрация 8 – 9 г/л. функция – поддержание онкотического давления крови. В норме здоровых людей не содержится. Содержание увеличивается при остром гепатите, циррозе печени, гепатоме, беременности. Повышение концентрации – ранний признак рака печени.
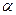 2 - глобулины
2 - глобулины
Гаптоглобин составляет 25% от всех 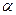 2-глобулинов. Гаптоглобины синтезируются в печени, состоят из двух легких и двух тяжелых цепей. М.М. 200 – 250 кД, концентрация 1 – 3 г/л.
2-глобулинов. Гаптоглобины синтезируются в печени, состоят из двух легких и двух тяжелых цепей. М.М. 200 – 250 кД, концентрация 1 – 3 г/л.
Разновидности Нр 1-1 (азиаты)
2-1
2-2
отличаются по набору полипептидных цепей и последовательности аминокислот.
Функция – гаптоглобин образует стабильный комплекс с гемоглобином, появляющимся в плазме крови в результате внутрисосудистого гемолиза эритроцитов. Гаптоглобин – гемоглобиновый комплекс поглощается клетками РЭС, где глобин и гем подвергаются распаду, а освободившееся железо используется для синтеза гема. Такой механизм предотвращает повреждение почек гемоглобином и потерю железа с мочой. Ингибитор протеаз, транспорт В12.
Низкий уровень гаптоглобина приводит к гемолитической анемии.
Концентрация увеличивается при воспалении, инфекции, ревматической лихорадке, метастазирующем раке.
Церулоплазмин – белок голубого цвета из-за содержания меди. М.М. 150 кД, концентрация 2 – 3 г/л, синтезируется гепатоцитами. Церулоплазмин участвует в обмене меди, регулирует уровень меди в печени, участвует в обмене витамина С, адреналина, диоксифенилаланина, серотонина, мелатонина. Уменьшение содержания цероплазмина при гепатоцеребральной дистрофии (болезнь Вильсона-Коновалова) сопровождается накоплением меди в нервной ткани и печени (врожденное нарушение). Увеличение содержания церулоплазмина специфично для меланомы и шизофрении.
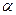 2-макроглобулин – ингибитор протеаз (эндопептидаз). М.М. 725 кД, концентрация 152 – 420 мг/100мл, синтезируется в печени. Протеазы появляются в крови при гибели клеток.
2-макроглобулин – ингибитор протеаз (эндопептидаз). М.М. 725 кД, концентрация 152 – 420 мг/100мл, синтезируется в печени. Протеазы появляются в крови при гибели клеток.
Три белка: 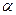 1-антитрипсин,
1-антитрипсин, 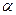 2-макроглобулин и интер-
2-макроглобулин и интер- 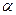 -трипсиновый ингибитор называют ингибиторами протеаз или антипротеазами. Эти белки ингибируют протеазы, т.е. регулируют их активность. Антипротеазы ингибируют ферменты свертывающей системы крови, а также протеазы (трипсин, химотрипсин), поступающие в кровь после гибели и разрушения клеток.
-трипсиновый ингибитор называют ингибиторами протеаз или антипротеазами. Эти белки ингибируют протеазы, т.е. регулируют их активность. Антипротеазы ингибируют ферменты свертывающей системы крови, а также протеазы (трипсин, химотрипсин), поступающие в кровь после гибели и разрушения клеток.
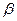 -глобулины.
-глобулины.
Трансферрин – связывает и транспортирует железо в различные ткани, регулирует концентрацию. М.М. 90 кД, концентрация – 2 – 3 г/л, синтезируется в печени и в макрофагальной системе. Имеет 2 активных центра, связывает 2 атома железа. Связывает и переносит Zn, Cu и витамин D.
Трансферрин предотвращает избыточное накопление Fe3+ в тканях и потерю его с мочой.
Уменьшение содержания трансферрина отмечается при гепатитах, опухолях, нефротическом синдроме. Повышение содержания связано с усиленным распадом эритроцитов.
Гемопексин – связавает гем и предотвращает его выведение почками. Комплекс гем-гемопексин улавливается из крови печенью, где железо освобождается и используется для образования гема. М.М. 57 кД, концентрация 50 – 100 мг/100мл.
Концентрация уменьшается при гемолизе, болезнях печени и почек. Концентрация увеличивается при воспалении.
Ферменты крови.
Ферменты крови делят на 3 группы:
1. Секреторные, плазмоспецифические или собственно сывороточные или собственные ферменты крови. Синтезируются где-то, чаще в печени, но поступают в кровоток и там выполняют функцию.
Относятся белки – ферменты свертывающей, антисвертывающей, кининовой, ренинангиотензиновой систем.
К этой группе относятся лецитин-холестеринацилтрансфераза (ЛХАТ), липопротеидлипаза, холинэстераза.
Диагностическое значение определения активности ферментов этой группы невелико. Снижение их активности указывает на повреждение продуцирующего эти ферменты органа – чаще всего печени.
2. Экскреторные
К этой группе относятся ферменты поджелудочной железы, желудка. Относятся трипсин, химотрипсин.
3. Тканевые (клеточные), индикаторные ферменты. Попадают в кровь из тканей, где они выполняют определенные внутриклеточные функции.
Активность этих ферментов определяют с целью выявления поврежденного органа. При поражении тех или иных тканей ферменты из клеток «вымываются» в кровь и их активность в сыворотке резко возрастает, что является индикатором степени и глубины повреждения тканей.
Начальные стадии повреждений, на которых целостность клеток еще не нарушена, но проницаемость клеточных мембран уже увеличелась, сопровождается выходом в кровь растворимых ферментов цитозоля (альдолаза, аланинаминотрансфераза, лактатдегидрогеназа, гексокиназа, пируваткиназа).
При более глубоких повреждениях, когда происходит разрушение клеток вплоть до некроза, в плазме крови появляются ферменты, связанные с клеточными органеллами – митохондриями, лизосомами.
Активность ферментов определяют с целью энзимодиагностики.
Ферментные тесты обладают определенной информативностью:
1. Показывают наличие патологии.
2. Показывают на локализацию процесса.
3. Определяют глубину повреждения клеток.
4. Позволяют решить вопрос о лечении, его эффективности. Необходимо сочетание с другими методами диагностики.
В клинике с целью диагностики определяют:
1. Креатинкиназу (фосфокреатинкиназу). Отностися к фосфотрансферазам, катализирует реакцию переноса остатка фосфорной кислоты на креатин с образованием креатин-фосфата. Играет важную роль в поддержании соотношения АТФ/АДФ в клетке. Специфична для мышечной ткани. Среди различных типов мышц активность креатинкиназы распределяется следующим образом: поперечнополосатые мышцы > сердечные мышцы > мышцы беременной матки > мышцы матки > гладкие мышцы.
Креатинкиназа представлена несколькими изоферментами, обладающими тканевой специфичностью. Молекула фермента состоит из 2 типов полипептидных цепей: М и В. Образует 3 изофермента: I тип (ВВ) – мозг, II тип (МВ) – сердце, III тип (ММ) – скелетная мускулатура.
У больных инфарктом миокарда активность креатинкиназы в сыворотке возрастает уже через 3-4 часа после начала заболевания, максимальная активность фермента отмечается к концу первых суток, в 5 0 20 раз (возможно до 100 раз).
У больных прогрессирующей мышечной дистрофией активность креатинкиназы возрастает в 50 раз, в мышцах появляются МВ и ВВ изоформы, отсутствующие у здоровых людей.
Различные заболевания центральной нервной системы – шизофрения, маниакально-депрессивный синдром, синдромы, вызываемые психотропными средствами сопровождаются возрастанием в крови активности креатинкиназы.
Повышение активности кратковременное, что обусловлено высокой активностью фермента и вызывает выработку антител и выведение из организма.
Для диагностики повреждения миокарда определяют активность аспартатаминотрансферазы. Активность фермента повышается у 98% больных. Повышение активности коррелирует с величиной очага поражения: повышение в 25-30 раз – крупный инфаркт, в 50-60 раз – трансмуральный инфаркт. Повышение активности фермента отмечается через 5 – 6 часов, максимум – через 15 – 20 часов.
Для диагностики инфаркта определяют изоверменты лактатдегидрогеназы: ЛДГ1 и ЛДГ2. Активность ферментов повышается через 1 – 2 суток после возникновения инфаркта. Повышение в 25 – 30 раз. Активность снижается в период исчезновения ресорбционекротического синдрома.
Повышение активности фермента позволяет дифференцировать стенокардию и инфаркт. При стенокардии активность фермента повышается редко и незначительно. Повторный инфаркт приводит к повышению активности фермента. При первичном инфаркте выбрасываются белки, на которые образуются АТ, которые могут стать причиной болевых синдромов (синдром Дреслера) и этим отличаются от вторичного инфаркта. При синдроме Дреслера активность фермента не повышена.
С целью диагностики заболеваний печени определяют активность аланинаминотрансферазы. Активность повышается за 1 – 1,5 недели до появления желтухи. Выявляют гепатит любой этимологии. Через 1 – 3 дня после появления желтухи активность АлТ увеличивается в 10 – 20 раз, четкой корреляции между повышением активности и величиной очага поражения нет. Нормализация АлТ – признак клинического выздоровления.
При заболеваниях печени незначительно повышается активность АсТ, возвращение к норме идет постепенно, но активность фермента может расти и на фоне лечения, т.е. в кровоток может проникать митохондриальный фермент, т.е. лечение неэффективно. Активность фермента характеризует выраженность цитолитического синдрома, т.е. повышение проницаемости мембран гепатоцитов.
Щелочная фосфотаза – катализирует гидролиз сложноэфирных связей в моноэфирах фосфорной кислоты и органических соединений. Активность фермента повышается у больных с механической желтухой, циррозе. Щелочная фосфотаза характеризует развитие внутрипеченочного холестаза – нарушение оттока по печеночным капиллярам.
Активность щелочной фосфатазы повышается у больных саркоидозом, туберкулезом, амилоидозом, лимфогрануломатозом.
При заболевании печени определяют изоферменты лактатдегидрогеназы, о заболевании судят по ЛДГ5, где есть связь между активностью фермента и величиной очага поражения, активность повышается одновременно с появлением желтухи.
Альдолаза – первый определенный в клинике фермент. Фермент гликолиза, активируется при злокачесвенных новообразованиях в печени.
Сорбитолдегидрогеназа – органоспецифичен для печени. В норме в крови не определяется, наличие свидетельствует о патологии.
Алкагольдегидрогеназа – окисляет этиловый спирт. С помощью этого фермента пытались дифференцировать алкогольный гепатит от других видов гепатита. Уровень АДГ не соответствует выраженности процесса.
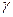 -глутамилтрансфераза – переносит остаток глу. Активность растет при алкогольном гепатите в 20 – 30 раз.
-глутамилтрансфераза – переносит остаток глу. Активность растет при алкогольном гепатите в 20 – 30 раз.
Белки острой фазы
Под этим термином объединяют белки содержание, которых увеличивается или белки обнаруживаются при воспалительных процессах.
К белкам острой фазы относятся: С-реактивный белок, 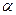 1-гликопротеин кислый,
1-гликопротеин кислый, 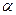 1-антитрипсин,
1-антитрипсин, 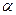 2-макроглобулин, церулоплазмин, гаптоглобин.
2-макроглобулин, церулоплазмин, гаптоглобин.
Для белков острой фазы характерны 2 общих признака:
1. Белки острой фазы являются гликопротеидами.
2. Синтезируются в печени.
Важное клиническое значение имеет определение содержания в сыворотке крови – С-реактивного белка. Название С-реактивный белок получил за способность вступать в реакцию преципитации с С-полисахаридом пневмококов.
С-реактивный белок синтезируется в печени, М.М.138 кД, 6 субъединиц по 23 кД. С-реактивный белок способствует фагоцитозу, активирует иммунные реакции, связывание комплемента.
Содержание белков острой фазы изменяется при остром течении заболевания, а также при обострении хронических процессов и понижается при выздоровлении. Белки острой фазы естественные ингибиторы иммунной системы, не дают развиться иммунопатологической реакции.
