Обмен белков и аминокислот
Белки являются источником N2 для организма, поступающий с белками азот выводится в виде конечных продуктов азотистого обмена, который характеризуется понятием азотистый баланс.
Азотистый баланс – разница между поступающими в организм N2 и выводимым из организма.
Различают три вида:
Ø Азотистое равновесие
Ø Положительный азотистый баланс
Ø Отрицательный азотистый баланс
При положительном азотистом балансе поступление N2 преобладает над выделением. Различают «+» азотистый баланс (беременность). Для детей 1 года жизни - +30%, в 4 года - +25%, в подростковом (14 лет) +14%. Ложный «+» азотистый баланс, при котором происходит задержка в организме конечных продуктов азотистого обмена. Это наблюдается при заболевании почек.
«-» азотистый баланс – преобладает выделение над поступлением. Это при тяжелых заболеваниях, туберкулез, ревматизм, онкологических заболеваний.
Азотистое равновесие – поступление N2=его выделению. Характерно для здоровых взрослых людей.
Азотистый обмен характеризуется коэффициентом изнашивания – то количество белка, которое теряется из организма в условиях полного белкового голодания. Для взрослого – 53 мг/1 кг, 24 г/сут. У новорожденных коэффициент изнашивание выше и составляет 120мг/кг. Азотистое равновесие обеспечивается белковым питанием. Этот белковый рацион должен иметь определенное количество и начальными характеристиками.
Количественный критерий:
Для взрослых существует 2 нормы:
Белковый минимум – то количество белка, которое обеспечивает азотистое равновесие при условии, что все энергетические затраты обеспечиваются углеводами и жирами. 40-45 г/сут.
Белковый оптимум – если долго использовать белковый минимум, то постепенно при ограниченном доступе страдают иммунные процессы, процессы кроветворения, репродуктивная система, поэтому оптимально для взрослых является более высокая норма – оптимум (оно обеспечивает выполнение всех его функций без ущерба для здоровья). 100 – 120 г/сут.
Для детей: В настоящее время норма потребления пересматривается в сторону их снижения. Для новорожденного ≈ 2 г/кг, к концу 1 года до 1 г/сут (при естественном вскармливании). 1,5 – 2 г/сут (при искусственном вскармливании.
Качественный критерий:
Все белки делятся на полноценные и неполноценные. Полноценные белки должны отвечать следующим требованиям:
Ø Содержать набор всех незаменимых аминокислот (валин, лейцин, изолейцин, тропин, метионин, лизин, аргенин, гистидин, триптофан, фенилаланин).
Ø Соотношение между аминокислотами должно быть близким к соотношению в тканевых белках
Ø Хорошо перевариваться в ЖКТ
Полноценные жиры – животные. Для новорожденных все белки должны быть полноценными (белки грудного молока). В возрасте 3-4 года ≈ 70-75% должны быть полноценными. Для взрослых ≈ 50%.
ПЕРЕВАРИВАНИЕ БЕЛКОВ
Ø Протеолитические ферменты выделяются в неактивном состоянии (защитный механизм от переваривания тканевых белков)
Ø Их активирование происходит в просвете ЖКТ путем частичного протеолиза
Ø Протеазы ЖКТ могут относится либо к эндопептидам или экзопептидазам (концевые аминокислоты отрываются) они отличаются субстратной специфичностью.
Переваривание белков происходит в желудке и в тонком кишечнике. Основной фермент расщепляющий белок является пепсин. Он выделяется в неактивном состоянии в виде профермента – пепсиногена. Под действием HCl идет частичный протеолиз и превращение его в активную форму пепсин.
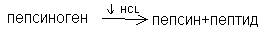
Это обнажает активный центр, меняет структуру белка. Пепсин относится к эндопептидазам (разрывает внутри пептидные связи) тирозин – фенлиаланин действует после этих аминокислот.
Роль HCl:
Ø Специфичный активатор пепсиногена
Ø Обеспечивает оптимум рН для пепсина (рН = 1-2)
Ø Вызывает частичную денатурацию белка
Ø Бактерицидный барьер
Слизистая желудка имеет целый ряд защитных механизмов:
a) выработка слизи (основной компонент ТАГ)
b) выделение пепсина в неактивном состоянии
c) выделение бикарбонатов
У детей процессы переваривания менее активны, чем у взрослых так как менее активный пепсин, более щелочная среда в желудке у маленьких детей в желудке кроме пепсина есть хемозин (фермент створаживающий молоко), гастриксин (рН 4-5), протеазы грудного молока, катепсины. В желудке происходит частичное перевариваривание белков до пептидов. Дальнейшее переваривание в тонком кишечнике под действием ферментов поджелудочной железы и собственные ферменты.
Ферменты поджелудочной железы:
Ø трипсин
Ø хемотрипсин
Ø эластаза
Ø карбоксипептидазы
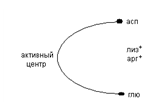 трипсин – выделяется поджелудочной железой в неактивном состоянии в виде трипсиногена, активируется ферментом энтеропептидазой (киназой) вырабатываемой слизистой кишечника. Активация путем частичного протеолиза ( 6 аминокислот)→освобождается активный центр. В активном центре в зоне связывания преобладают кислые кислоты (глю, асп), поэтому трипсин расщепляет пептидную связь образованную лизином и аргинином. Он активирует и другие ферменты и себя.
трипсин – выделяется поджелудочной железой в неактивном состоянии в виде трипсиногена, активируется ферментом энтеропептидазой (киназой) вырабатываемой слизистой кишечника. Активация путем частичного протеолиза ( 6 аминокислот)→освобождается активный центр. В активном центре в зоне связывания преобладают кислые кислоты (глю, асп), поэтому трипсин расщепляет пептидную связь образованную лизином и аргинином. Он активирует и другие ферменты и себя.
Хемотрипсин – вырабатывается в неактивном состоянии - хемотрипсиноген, активируется трипсином путем частичного протеолиза, относится к эндопептидазам, содержат в активном центре гидрофобной аминокислоты, расщепляет связи ароматических кислот (фен, тир)
Эластаза – активирует проэластаза, трипсином (частичный протеолиз), в активном центре эластазы преобладает ГЛИ, действует на пептидные связи.
Карбоксилазы – относятся к эндопептидазам, отщепляет концевые аминокислоты, тип А-отщепляют С-конец аминокислоты, ароматические (фен, тир) тип В – отщепления С-концевой от лизина и аргинина.
Ферменты поджелудочной железы:
Ø аминопептидазы
Ø дипептидазы
Аминопептидазы – эйкопептидазы, отщепляют N-конец аминокислоты среди аминопептидаз активной является лейкоаминопептидаза (ЛАГ). Дипептидазы расщепляет дипептидазы. В тонком кишечнике происходит полная гидролитическое расщепление пищевых белков до аминокислот. Образовавшиеся аминокислоты подвергаются всасыванию. У детей снижена активность ферментов слизистой кишечника и поджелудочной железы.
ВСАСЫВАНИЕ АМИНОКИСЛОТ
Na-зависимый активный процесс, нужна АТФ; перенос отдельных аминокислот осуществляется специальными переносчиками. Среди транспортных систем наиболее важной является система, предполагающая участие:
Ø трипептидаза глютадиона (глю-гли-цис) и глю имеет свободные СООН группы
Ø γ-глютамин-транс-пептидаза
Суть:
Аминакислота связана с глютаминовой кислотой и образует комплекс→подвергается всасыванию, глю-возвращается. Эта активно для ЦНС, сер, треонина.
У детей могут всасываться не только аминокислоты, но и пептиды и низкомолекулярными белками. Эта способность имеет 2 следствия:
Ø могут поступать Jg, антитела из грудного молока
Ø вызывают аллергическую реакцию
ГНИЕНИЕ БЕЛКОВ В ТОНКОМ КИШЕЧНИКЕ
Процессу гниения подвергаются не полностью расщепляющиеся белки и отдельные аминокислоты. Оно под действием ферментов гнилостной микрофлоры. При гниении образуется большое количество газообразного и негазообразного нередко токсичные веществ. К продуктам гниения относится: CO2, CH4, NH3, H2S, меркаптаны, альдегиды, кетоны, карболовые кислоты, диамины.
Диамины образуются из аминокислот (лизин, орнитин). При их декарбоксилировании образуется:
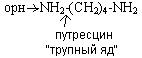
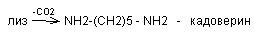
Могут выводится из кишечника или обезвреживаться в печени, могут обезвреживать токсичные циклические продукты.
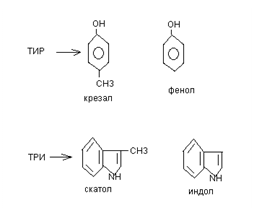 Чрезвычайно токсичные, их всасывание происходит по системе vena porta, обезвреживание в печени.
Чрезвычайно токсичные, их всасывание происходит по системе vena porta, обезвреживание в печени.
ОБЕЗВРЕЖИВАНИЕ В ПЕЧЕНИ ПРОДУКТОВ ГНИЕНИЯ БЕЛКОВ
Выделяют:
- синтез мочевины из NН3
-
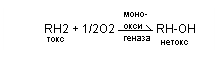 микросомальное окисление токсичных веществ – участвуют мооксидазы, в результате гидроксилирования идет снижение токсичности, повышается водорастворимость, повышается реакционная способность.
микросомальное окисление токсичных веществ – участвуют мооксидазы, в результате гидроксилирования идет снижение токсичности, повышается водорастворимость, повышается реакционная способность. - образование парных нетоксичных соединений – образующихся путем присоединения к обезвреживанию продуктами Н2SО4 в процессах обезвреживания участвует в активной форме ФАДС (фосфо-аденозил-фосо-сульфат), которая обезвреживает индоксил:
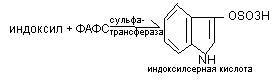
Калиевая соль этой кислоты выводится через почки. Его количество в моче свидетельствует об антитоксической функции почек и усилении гнилостных процессов.
Гиалуроновая кислота-активная форма это УДФ-глюкозовая кислота (урацил-рибоза-ф-ф-глюкуроновая кислота)
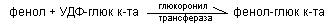
Глицин – бензойная кислота + глицерин→гиалуроновая кислота, используется для оценки антитоксической функции печени.
Проба Квина – вводят бензойную кислоту. Антипириновая проба – аптипириновое вещество, которое в печени подвергается микросомальное окисление.
Гнилостные процессы у детей отсутствуют. У взрослых усиление гнилостных процессов при снижении активности протеолитических ферментов желудка и кишечника при снижении моторики ЖКТ, дизбактериозах.
ДИНАМИЧЕСКОЕ ОСОТОЯНИЕ БЕЛКОВ В ОРГАНИЗМЕ.
Белки тканей организма постоянно обновляются, то есть подвергается распаду и постепенно замещаются вновь синтезированными. В таких тканях как кровь, слизистая кишечника, печень приблизительно за 10 дней, Белки обмениваются на ½ - период полуобмена. В других тканях – кожа, мышцы период полуобмена >. Распад тканевых белков (катаболизм) осуществляют особые тканевые протеолитические ферменты катепсины. Выделяют несколько видов, которые обозначают: А, В, Д, Н, N. Катепсины локализованы как в лизосомах так и в цитозоле. Лизосомальные называются кислыми катепсинами так как оптимум рН= 4,5-5,5. Катепсины могут быть как эндопептидазами, так и экзопептидазами. В активном центре катепсинов могут присутствовать цистеин, аспарагиновая кислота, серин. Например катепсин Д по эффекту аналогичен катепсину желудочного сока, катепсин Н – печени, катепсин N – обладает калогенолитической активностью.
Биороль:
Ø участвует в обновлении тканевых белков
Ø разрушает дефективный денатуриновый белок. Обычно эти белки вначале соединяются в особый белок убиквинтин и после этого начинается разрушение дефективных белков катепсинами
Ø реконструктивная функция – катепсины переводят неактивные формы белки в активные.
Ø При голодании, кровопотери, интоксикации катепсины обеспечивают мобилизацию белков из условных депо белков (плазма крови, мышцы, печень).
В ткани всегда существует определенный запас аминокислот. Он поддерживается на достаточно постоянном уровне благодаря сбалансированности путей образования и использования аминокислот.
Пути образования тканевых аминокислот
- Аминокислоты всосавшиеся из кишечника в результате переваривания пищевых белков (1/3 фонда)
- Аминокислоты, образовавшиеся при распаде белков
- Синтез в тканях заменимых кислот
Пути расходования
- Синтез тканевых белков из пепетидов
- образование небелковых N-содержащих веществ (пуриновые основания, креатинин, биогенные амины)
- с энергитической целью
- на синтез углеводов (глюконеогенез)
- образование некоторых метаболитов липидного обмена
Катаболизм условно делят на: общие реакции (происходят в отношении радикала, аминогрупп, СООН-групп), специфические реакции.
