Ферментативные (биохимические) свойства и принципы идентификации микроорганизмов
Цель занятия.Ознакомить студентов с методами изучения ферментативной активности и принципами идентификации микроорганизмов.
Оборудование и материалы. Засеянные среды Гисса (глюкоза, лактоза, сахароза и т.д.) с признаками кислото- и газообразования, культуры Е. coli на МПБ в пробирках, реактив Эрлиха, культуры В. subtilis на молоке, МПЖ, культуры S. aureus на МПА в пробирках, 3%-й раствор перекиси водорода и другие тесты, результаты определения ферментативной активности культур Е. coli и S. typhimurium на ПБДЭ-пластинах, карточки с описанием свойств отдельных видов бактерий для работы с определителями.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Изучение ферментативной активности микроорганизмов. В пределах семейства у представителей разных родов можно обнаружить как общие для семейства, так и специфические для родов наборы ферментов. У микроорганизмов разных видов в пределах одного рода есть общие (родовые) и специфические для отдельных видов ферменты. Таким образом, каждый вид микроорганизмов характеризуется специфическим набором ферментов, поэтому определение ферментного спектра — важнейший этап идентификации микроорганизмов.
О наличии того или иного фермента судят по способности микроорганизмов воздействовать на известный субстрат. Присутствие фермента регистрируют по изменению физического состояния субстрата (разжижение желатины), закислению питательной среды (среды Гисса с углеводами), образованию определенных продуктов метаболизма (индол, сероводород, аммиак) и т.д.
Наиболее распространены следующие методы регистрации ферментативной активности микроорганизмов.
Выявление сахаролитической активности микроорганизмов. В состав дифференциально-диагностических углеводных сред (среды Гисса — см. тему 7) входят различные соединения, которые можно условно назвать сахарами: моносахариды, полисахариды, многоатомные спирты. При утилизации углеводов в качестве конечных продуктов образуются кислоты и газообразные продукты. Соответственно расщепление углевода регистрируют по изменению рН среды и выделению газообразных продуктов. Закисление питательной среды улавливают при помощи различных индикаторов.
Индикатор BP, входящий в состав сухих сред Гисса, меняет цвет от розового в щелочной среде через серый при нейтральном рН до голубого или ярко-синего в кислой среде.
Индикатор Андрэдэ (кислый фуксин —0,5 г, 1%-й раствор гидроксида натрия — 16 мл, дистиллированная вода — 84 мл) при закислении дает покраснение среды. В жидких средах Гисса образование газов при утилизации субстрата улавливают при помощи поплавков («газовок») — стеклянных трубочек, запаянных в верхнем конце и помещенных в пробирки. В «газовках» скапливаются газы, вытесняющие жидкую питательную среду; в полужидких средах Гисса газообразные продукты остаются в толще среды в виде пузырьков.
Ферментация углеводов иногда происходит медленно, поэтому предварительный учет результатов проводят через 24...48 ч, а окончательный — через 10...14 сут инкубирования посевов. Тест с метиловым красным показывает степень закисления среды при расщеплении глюкозы. Метилрот как индикатор срабатывает в диапазоне рН 4,4...6,0. Исследуемую культуру выращивают 2...5 сут в жидкой среде Кларка с глюкозой. Затем на 5 мл среды добавляют пять-шесть капель раствора метилрота. Положительный результат — покраснение среды после внесения индикатора (рН 4,0...5,0).
Среда Кларка: пептон — 5 г, гидрофосфат калия — 5 г, глюкоза — 5 г, вода дистиллированная — 1000 мл. Ингредиенты растворяют в воде, кипятят 2...3мин, фильтруют через бумажный фильтр, устанавливают рН 6,9...7,0, разливают по пробиркам и стерилизуют при 112º С 20 мин.
Тест Фогес-Проскауера выявляет промежуточный продукт расщепления глюкозы — ацетоин (ацетилметилкар-бинол, диметилкетон). Исследуемую культуру выращивают на среде Кларка. К 1 мл культуры добавляют 0,6 мл 5%-го раствора а-нафтола, перемешивают, вносят 0,2 мл 40%-го раствора гидроксида калия и инкубируют 1 ч. Положительная реакция — красное окрашивание среды.
Выявление протеолитических и других ферментов микроорганизмов.Протеолитические ферменты расщепляют белки питательной среды до промежуточных (пептоны, полипептиды, аминокислоты) или конечных (сероводород, индол, аммиак) продуктов.
Характер роста микроорганизма на молоке: при посеве исследуемой культуры бактерий на стерильное обезжиренное молоко можно выявить фермент, расщепляющий молочный сахар (лактозу), и протеолитические ферменты, действующие на молочный белок (казеин). Расщепление лактозы приводит к закислению и свертыванию молока, при выделении протеолитических ферментов казеин постепенно растворяется — пептонизируется, в результате чего молоко просветляется, приобретает легкий кремовый оттенок, а на дне пробирки формируется осадок. Свертывание молока может также происходить под влиянием выделяемого некоторыми бактериями «сычужного» фермента, в этом случае реакция молока бывает щелочной. Иногда возможна пептонизация казеина без свертывания молока.
Тест на гидролиз казеина в плотных питательных средах: обезжиренное молоко диализуют для удаления лактозы, которая ингибирует гидролиз казеина. В расплавленный питательный агар с двойной концентрацией агар-агара добавляют равный объем стерилизованного автокла-вированием диализованного молока. Исследуемую культуру бактерий засевают «штрихом» на поверхность питательной среды, разлитой в чашки Петри. Посевы инкубируют до 14 сут. Перед учетом результатов поверхность среды заливают 10%-м раствором соляной кислоты. Положительный результат — просветление среды вокруг колоний.
Тест на желатиназу: культуру микроорганизма засевают уколом в столбик питательного бульона, содержащего 12 % желатины. После культивирования опытную и контрольную (незасеянную) пробирки охлаждают под холодной водой и по «текучести» желатины делают заключение о наличии фермента.
Тест на сероводород: узкие полоски фильтровальной бумаги смачивают в 5%-м растворе ацетата свинца, высушивают, стерилизуют. Культуру микроорганизма засевают в питательную среду в пробирке, после чего индикаторную бумагу помещают в пробирку (не должна касаться среды) и закрепляют пробкой. Выделяющийся сероводород реагирует с ацетатом свинца, и образующийся сульфид свинца вызывает почернение бумаги (положительный результат). Описанный метод выявления сероводорода при помощи индикаторных бумажек считают одним из наиболее чувствительных, разработаны и другие методы.
Тест на индол: исследуемую культуру целесообразно выращивать на средах, богатых триптофаном, при расщеплении которого образуется индол (бульон Хоттингера, бульон с 0,1% Z-триптофана). К выращенной культуре добавляют 1...3мл эфира, встряхивают, отстаивают и вносят 0,5 мл реактива Эрлиха (парадиметиламинобензоальдегид — 1 г, 96%-й этанол — 95 мл, соляная кислота —20 мл). Через 5 мин учитывают результат. Появление на границе эфира и питательной среды красно-фиолетового окрашивания свидетельствует о наличии индола.
Тест на аммиак: исследуемую культуру засевают в жидкую питательную среду в пробирке. Между пробкой и стенкой пробирки закрепляют полоску розовой лакмусовой индикаторной бумажки. Посевы инкубируют в термостате 1...5сут. Посинение лакмусовой бумажки свидетельствует о выделении аммиака.
Тест на уреазу: исследуемую культуру микроорганизма засевают на среду Кристенсена (пептон — 1 г, хлорид на трия — 5 г, дигидрофосфат калия — 2 г, агар — 20 г, глюкоза — 1 г, 0,2%-й раствор фенолрота — 6 мл, 20%-й раствор мочевины — 100 мл, вода дистиллированная — 1000 мл) и выращивают 1...4сут. Положительный результат — покраснение среды в результате ее защелачивания.
Тест на редукцию нитратов выявляет восстановление нитратов до нитритов. Культуру микроорганизма засевают в МПБ, содержащий 0,2 % нитрата калия, инкубируют 48...72 ч, затем в опытную и контрольную пробирки добавляют по 1 мл реактива с крахмалом (растворимый крахмал — 1 г, вода дистиллированная — 100 мл, йодид калия —0,5 г). К этому раствору перед постановкой реакции добавляют несколько капель 10%-го раствора соляной кислоты. Положительный результат— темно-синее окрашивание.
Тест на общую фосфатазу: исследуемую культуру микроорганизма засевают «штрихом» на поверхность питательного агара с натриевой солью .дифосфата фенолфталеина, инкубируют 4...5 сут. Чашки переворачивают вниз крышкой, на внутреннюю поверхность которой наносят каплю 28...30%-го раствора нашатырного спирта. При наличии фосфатазы колонии приобретают красный цвет.
Тест на каталазу: бактериальную массу снимают с поверхности агара бактериологической петлей и суспендируют в капле 3%-го раствора перекиси водорода на предметном стекле. Положительный результат — образование пузырьков газа.
Тест на оксидазу: фильтровальную бумагу пропитывают 1%-м раствором тетраметилпарафенилендиамина дигид-рохлорида. Бактериальную массу петлей наносят на поверхность бумажной полоски. Положительный результат — фиолетовое или пурпурное окрашивание через 10...60 с.
Тест на редуцирующую способность бактерий (в метиленовом молоке) основан на следующей особенности: при окислительно-восстановительных реакциях у бактерий акцептором водорода может быть кроме молекулярного кислорода ряд органических красителей, которые, присоединяя водород, восстанавливаются и обесцвечиваются. Такие свойства отмечены у лакмусовой настойки, метиленового синего, малахитового зеленого и т. д. Например, молоко с метиленовым синим готовят так: молоко подщелачивают 10%-м раствором карбоната натрия до рН 7,2 и добавляют 20 мл 1%-го водного раствора метиленового синего на 1000 мл. Готовая среда голубого цвета. Результат учитывают через сутки инкубирования посевов. В случае редукции красителя среда окрашена в кремовый цвет.
Тест-системы для быстрой идентификации бактерий по группе специально отобранных биохимических признаков обычно представляют собой пластмассовые пластины с лунками (микропробирками), заполненными различными сухими средами (субстратами). В эти среды вносят суспензию исследуемой культуры и после инкубирования учитывают результат. К тест-системам прилагают таблицы для учета результатов и идентификации микроорганизмов в зависимости от спектра выявленных ферментов.
За рубежом разработаны тест-системы для идентификации энтеробактерий, анаэробов, несбраживающих бактерий и т. д. В России Нижегородский институт микробиологии и эпидемиологии выпускает тест-систему подобного типа — биохимические пластины для идентификации энтеробактерий (ПБДЭ), кроме того, разработаны тест-системы для санитарно-микробиологи-ческих целей.
Принципы идентификации микроорганизмов. Основная задача бактериологического диагностического исследования — это определение таксономического положения выделенного микроорганизма путем сравнения его свойств со свойствами известных видов.
В рутинной бактериологической практике микроорганизм идентифицируют, изучая его фенотипические признаки (морфологические, тинкториальные, культуральные, биохимические, патогенные). Стали получать распространение некоторые методы идентификации по генотипическим признакам (см. тему 12), которые ранее в основном применяли в научной работе для классификации микроорганизмов с неясным таксономическим положением.
В бактериологии для идентификации используют определители микроорганизмов. Наиболее популярный — определитель бактерий Берджи — включает в себя описание свойств известных видов микроорганизмов. Бактерии в этом руководстве по ограниченному числу морфологических и физиологических признаков объединены в большие группы, например группа № 20 «Грамположительные неспорообразующие палочки неправильной формы» или группа № 5 «Факультативно-анаэробные грам-отрицательные палочки». В пределах этих групп при помощи нескольких дифференцирующих признаков бактерии подразделены на семейства, роды и виды. Распределение микроорганизмов в этом определителе не отражает иерархической классификации, а преследует сугубо практическую цель — как можно быстрее и экономичнее установить таксономическое положение изучаемого микроорганизма.
Идентификация неизвестного микроорганизма представляет собой процесс последовательного его отождествления с той или иной большой группой микробов, характеризующихся общими свойствами, затем с семейством в пределах группы, далее с тем или иным родом в пределах установленного семейства, и на конечном этапе исследуемый микроорганизм отождествляют (идентифицируют) по совокупности морфологических, тинкто либо видом в пределах рода. В случае необходимости внутри вида устанавливают принадлежность культуры к био-, серо-, фаговару. Работа с определителем Берджи предполагает использование достаточно большого количества тестов, характеризующих различные свойства микроорганизма. В практических диагностических лабораториях, исходя из эпизоотологических, клинических и патологоанатомических данных, обычно проводят бактериологические исследования, заранее ориентированные на обнаружение возбудителя определенной инфекционной болезни, по схеме, предусмотренной официальной инструкцией.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Ознакомиться с тестами, характеризующими ферментативные свойства бактерий (ферментация углеводов в средах Гисса, образование индола, сероводорода; тесты на каталазу, оксидазу, желатиназу и т. д.).
. 2. Используя карточки с описанием свойств бактериальной культуры, при помощи определителя микробов установить ее видовую принадлежность.
3. Оценить результаты изучения ферментативной активности двух бактериальных культур семейства Enterobacteriaceae на ПБДЭ-пластинах и определить их вид при помощи прилагаемой дифференциальной таблицы.
Контрольные вопросы
1.Какое таксономическое значение имеет определение набора ферментов у микроорганизмов?
2.Что представляют собой современные тест-системы для изучения ферментативной активности микроорганизмов?
3.Что такое определители бактерий?
Тема 10
БАКТЕРИОФАГИ
Цель занятия. Ознакомить студентов с действием бактериофагов и их практическим использованием.
Оборудование и материалы. Культура вакцинного штамма L. monocytogenes, набор листериозных бактериофагов, стерильный МПБ, содержащий 0,5 % глюкозы, 2%-й МПА в чашках Петри, стерильные пипетки Пастера, лечебно-профилактический бактериофаг против паратифа и колибактериоза телят, чувствительная к фагу культура Е. coli.
МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Бактериофаги представляют собой вирусы, адаптировавшиеся в процессе эволюции к паразитированию в прокариотических клетках (рис. 47). Репродукция многих бактериофагов в клетке приводит к ее лизису. На специфической адаптации фагов к строго определенным видам (штаммам) бактерий и внешнем проявлении поражения бактериальных клеток (лизис) основано практическое использование бактериофагов: при помощи известного (диагностического) фага можно обнаружить и идентифицировать бактерии. Кроме того, биологическая промышленность выпускает лечебно-профилактические бактериофаги.
Определение литической активности бактериофага. У диагностических и лечебно-профилактических фагов должна быть выражена литическая активность, которую определяют путем титрования фагов, например, в жидкой питательной среде.
В бактериологические пробирки разливают по 4,5 мл стерильного МПБ; в первую пробирку вносят 0,5 мл исследуемого фага, затем готовят его десятикратные разведения от 10~' до Ю-'0. К разведениям бактериофага добавляют по капле суточной бульонной культуры чувствительного к данному фагу вида бактерий, инкубируют при 37 °С 24 ч. За титр фага принимают его максимальное разведение, еще способное вызвать лизис бактерий — среда в пробирке прозрачна. Фаг считают активным при титре 10-7, 10-8
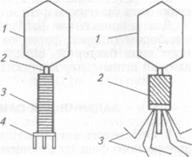
| Рис. 47. Схема строения фага Т2 по данным электронной микроскопии: а — с нуклеиновой кислотой в головке: 1 — головка; 2— полая центральная часть; 3 — оболочка (расправленная); 4— базальная пластинка; б —без нуклеиновой кислоты в головке: I — головка; 2 — оболочка (сокрашенная); 3 — хвостовые нити |
Определение количества бактериофага (по методу Грациа). Готовят десятикратные разведения исследуемого фага в физиологическом растворе (10-1…10-2 и т.д.), затем из последнего разведения, например 10-7 или 10-8, берут 0,5 мл жидкости, смешивают с равным объемом чувствительной к данному бактериофагу бульонной культуры бактерий. Полученную смесь добавляют к 4 мл расплавленного 0,7%-го МПА (температура 45 °С), перемешивают и выливают на поверхность подсушенного питательного агара в чашку Петри. Аналогичным образом поступают со всеми разведениями бактериофага (10-5, 10-5 и т.д.). Чашки инкубируют в термостате при 37 ºС 24 ч.
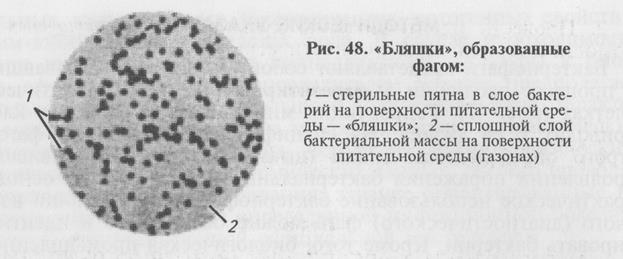
Учет результатов: не пораженные бактериофагом бактерии растут и образуют сплошной газон на поверхности питательного агара. Клетки, пораженные фагом, лизируются, и в этой зоне можно видеть «стерильные» пятна на сплошном бактериальном газоне. Количество этих пятен («бляшек») соответствует количеству фаговых частиц в суспензии (рис. 48).
Применение фагов для идентификации бактерий. Фаги применяют для видовой идентификации бактерий (возбудитель сибирской язвы, листериоза и др.) или внутривидовой — установление фаговара конкретного бактериального штамма.
Для идентификации неизвестной культуры бактерий при помощи диагностического бактериофага обычно используют плотную питательную среду. Например, исследуемую 18-часовую культуру, предположительно листерий, засевают в МПБ с глюкозой, инкубируют при 37 °С 4 ч до легкой опалесценции среды и затем засевают газоном (0,1мл) на подсушенный 2%-й МПА в чашку Петри. Через 1... 1,5 ч инкубирования посевов при 37 ºС при слегка приоткрытой крышке на одну половину газона наносят каплю листериозного бактериофага 2А и на вторую половину помещают каплю фага 4А. Посевы инкубируют при 22...25 °С 16...24ч.
Учет результатов: если культура листериозная, то на месте нанесения хотя бы одного фага можно видеть прозрачную зону лизиса.
Для установления фаговара исследуемую культуру проверяют с набором типовых фагов, охватывающих все фаговарианты данного вида бактерий, определяют, к какому фагу чувствителен данный штамм, что и служит его маркером.
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Определить активность лечебно-профилактического коли-па-ратифозного фага по отношению к исследуемой культуре Е. coli.
2. Провести идентификацию культуры L. monocytogenes при помощи листериозных диагностических фагов.
Контрольные вопросы
1.Что такое бактериофаг?
2.Как используют бактериофаги?
3.Какими методами титруют бактериофаги?
Тема 11
